
| A. | ①②④⑤ | B. | ①②③⑤ | C. | ①②③④ | D. | ①②③④⑤ |
分析 两种短周期元素X和Y可组成化合物XY3,则X为ⅢA族元素时,Y为ⅤⅡA族元素;或X、Y均为ⅥA族元素;还有可能为X在ⅤA族,Y为ⅤⅡA族或H,以此来解答.
解答 解:两种短周期元素X和Y可组成化合物XY3,则X为ⅢA族元素时,Y为ⅤⅡA族元素;或X、Y均为ⅥA族元素;还有可能为X在ⅤA族,Y为ⅤⅡA族或H,
①若Y为Cl,X为Al,则X的原子序数为m-4,故①正确;
②若Y为F,X为Al,则X的原子序数为m+4,故②正确;
③若Y为S,X为O,则X的原子序数为m+8,故③正确;
④若Y为Cl,X为P,则X的原子序数为m-2,故④正确;
⑤若Y为H,X为N,则X的原子序数为m+6,故⑤错误;
故选C.
点评 本题考查常见的化合物XY3,熟悉元素在周期表中的位置及元素的原子序数的关系即可解答,难度不大.


 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | 加热,用湿润的红色石蕊试纸置于试管口检验 | |
| B. | 加强碱溶液后加热,再滴入无色酚酞试液 | |
| C. | 加热,用蘸有浓盐酸的玻璃棒置于试管口检验 | |
| D. | 加烧碱溶液后加热,再用湿润的红色石蕊试纸置于试管口检验 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②④ | C. | ③⑥ | D. | ⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
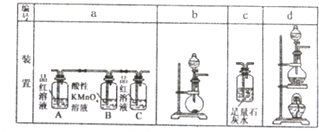 盐酸、硫酸和硝酸是常见应用于广泛的三种强酸,理解掌握酸的氧化性十分重要.请回答下列有关问题:
盐酸、硫酸和硝酸是常见应用于广泛的三种强酸,理解掌握酸的氧化性十分重要.请回答下列有关问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| ⅠA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 | |
| 第2周期 | ⑤ | ⑦ | ⑨ | |||||
| 第3周期 | ① | ③ | ⑥ | ④ | ⑧ | ⑩ | ||
| 第4周期 | ② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
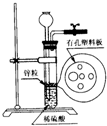 图为实验室制氢气的简易装置.若在加稀硫酸时,发现锌粒与稀硫酸没有接触而稀硫酸又不够了,为使该反应顺利进行,则可以从长颈漏斗中加入的试剂是( )
图为实验室制氢气的简易装置.若在加稀硫酸时,发现锌粒与稀硫酸没有接触而稀硫酸又不够了,为使该反应顺利进行,则可以从长颈漏斗中加入的试剂是( ) | A. | ①③⑤ | B. | ②⑥ | C. | ①②③⑤⑦ | D. | ①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
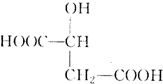 )广泛存在于水果中,尤以苹果、葡萄、西瓜、山楂为多.
)广泛存在于水果中,尤以苹果、葡萄、西瓜、山楂为多.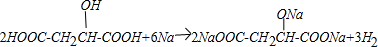 .
.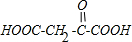 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
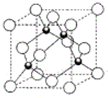 原子序数小于36的X、Y、Z、W四种元素,其中X是宇宙中最丰富的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29.
原子序数小于36的X、Y、Z、W四种元素,其中X是宇宙中最丰富的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com