
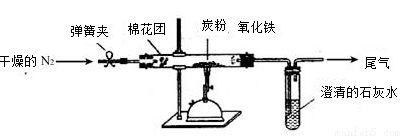
(14分)某研究性学习小组对过量炭粉与氧化铁反应的气体产物成分进行研究。设计方案如图,将一定量的氧化铁在隔绝空气的条件下与过量炭粉完全反应,测定参加反应的碳元素与氧元素的质量比。
TiCl4 | Mg | MgCl2 | Ti | |
熔点/℃ | -25.0 | 648.8 | 714 | 1667 |
沸点/℃ | 136.4 | 1090 | 1412 | 3287 |
(1)查阅资料:
①氮气不与炭粉、氧化铁发生反应。实验室可以用氯化铵饱和溶液和亚硝酸钠(NaNO2)饱和溶液混合加热制得氮气。写出该反应的离子方程式: 。
②使上述制得的气体通过___________装置方能获得干燥的N2
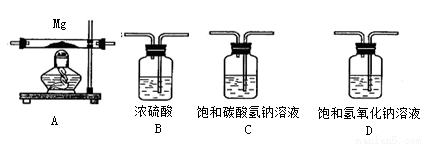
(2)实验步骤:
①按图连接装置,并检查装置的气密性,称取3.20g氧化铁、2.00g炭粉混合均匀,放入48.48g的硬质玻璃管中;
②加热前,先通一段时间纯净干燥的氮气;
③停止通入N2后,夹紧弹簧夹,加热一段时间,澄清石灰水(足量)变浑浊;
④待反应结束,再缓缓通入一段时间的氮气。冷却至室温,称得硬质玻璃管和固体总质量为52.24g;
⑤过滤出石灰水中的沉淀,洗涤、烘干后称得质量为2.00g。步骤②、④中都分别通入N2,其作用分别为 。
(3)数据处理:
①试根据实验数据分析,该反应的气体产物是CO2和CO,理由是____________________
②写出该实验中氧化铁与炭粉发生反应的化学方程式: 。
(4)实验优化:
学习小组有同学认为应对实验装置进一步完善。
①甲同学认为:应将澄清石灰水换成Ba(OH)2溶液,其理由是 。
②pC类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值。如某溶液溶质的浓度为:1×10-3mol/L,则该溶液中该溶质的pC=-lg1×10-3=3。现向0.2mol/LBa(OH)2溶液中通入CO2气体,沉淀开始产生时,溶液中CO32-的PC值为_________(已知:lg2=0.2;Ksp(BaCO3)=5.0×10-9)
③从环境保护的角度,请你再提出一个优化方案将此实验装置进一步完善: 。
 初中暑期衔接系列答案
初中暑期衔接系列答案科目:高中化学 来源:2014-2015学年广东茂名市高三第二次高考模拟考试理综化学试卷(解析版) 题型:填空题
(15分)二甲醚具有优良的燃烧性能,被称为21世纪的“清洁能源”,以下为其中一种合成二甲醚的方法:在一定温度、压强和催化剂作用下,在同一反应器中进行如下反应:
①CO2(g)+3H2(g) CH3OH(g) +H2O(g) △H1=-49.1 kJ·mol-1
CH3OH(g) +H2O(g) △H1=-49.1 kJ·mol-1
②2CH3OH(g) CH3OCH3(g)+H2O(g) △H2=-24.5 kJ·mol-1
CH3OCH3(g)+H2O(g) △H2=-24.5 kJ·mol-1
③CO2(g)+H2(g) CO(g)+H2O(g) △H3=+ 41.2 kJ·mol-1
CO(g)+H2O(g) △H3=+ 41.2 kJ·mol-1
(1)写出CO2(g)加H2(g)转化为CH3OCH3(g)和H2O(g)的热化学方程式是 。
(2)一定条件下,原料气中n(H2)/n(CO2)比值和温度对CO2转化率影响的实验数据如下图。
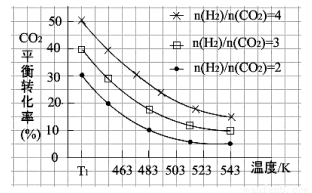
①温度为T1 K时,在1 L反应容器中投入2mol CO2 和8mol H2进行反应,试计算达到平衡时CO2的浓度为 。
②结合数据图,归纳CO2平衡转化率受外界条件影响的变化规律:
a 。
b 。
(3)为研究初始投料比与二甲醚产率关系,在一定温度和压强下,投入一定物质的量的H2、CO、CO2进行试验,实验发现二甲醚的平衡产率随原料气中n(CO)/〔n(CO)+n(CO2)〕比值增大而增大,试分析其原因 。
(4)下图是科学家现正研发的,以实现反应①在常温常压下进行的装置。
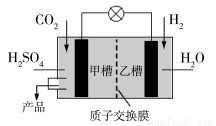
写出甲槽的电极反应 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年天津市河北区高三总复习质量检测一化学试卷(解析版) 题型:选择题
生活中的一些问题常涉及到化学知识,下列叙述不正确的是
A.维生素C具有还原性,在人体内起抗氧化作用
B.“加碘食盐”、“含氟牙膏”、“富硒营养品”、“高钙牛奶”、“加铁酱油”等等,这里的碘、氟、硒指的是分子,钙、铁则分别是钙离子和铁离子
C.日本大地震后,防疫人员在震区周围撒石灰,进行环境消毒,防止灾后出现疫情
D.为防止中秋月饼等富脂食品氧化变质,常在包装袋中放入硫酸亚铁
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省常德市高三模拟考试理综化学试卷(解析版) 题型:填空题
2015年3月,全国“两会”代表委员就我国“雾霾”治理积极建言献策。科学家研究表明氮氧化物与悬浮在大气中的盐粒子相互作用时能产生“二次雾霾”,涉及的反应有:
2NO2(g)+NaCl(s) NaNO3(s)+ClNO(g) K1 (Ⅰ)
NaNO3(s)+ClNO(g) K1 (Ⅰ)
2NO(g)+Cl2(g) 2ClNO(g) K2 (Ⅱ)
2ClNO(g) K2 (Ⅱ)
回答下列问题:
(1)写出反应(Ⅰ)的平衡常数表达式K1 = 。
(2)恒温恒容条件下,反应(Ⅱ)达到平衡的标志是 。
a.体系压强保持不变
b.混合气体颜色保持不变
c.NO和ClNO的物质的量相等
d.每消耗0.1 mol NO的同时消耗0.05 mol Cl2
(3)为研究不同条件对反应(Ⅱ)的影响,恒温时向2 L密闭容器中加入 0.2 mol NO和0.1mol Cl2:
①在恒容条件下反应10 min达到平衡,测得10 min内v(ClNO)=7.5×10-3 mol·L-1·min-1,
则NO的平衡转化率α1= 。
②在恒压条件下建立平衡时NO的转化率为α2,则α2 α1(填“>”“<”
或“=”),平衡常数K2 (填“增大”、“减小”或“不变”)。
(4)工业上可通过电解NO制备NH4NO3,其工作原理如图所示,阴极反应式为 ;为使电解产物全部转化为NH4NO3,需补充气体物质A,A的化学式是_________。

(5)NO2可助偏二甲肼(C2H8N2)燃烧,产生的巨大能量能把火箭送入太空。已知6.0g液态偏二甲肼与液态NO2完全反应生成N2、CO2、H2O(g)放出225.0kJ的热量。写出该反应的热化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省常德市高三模拟考试理综化学试卷(解析版) 题型:选择题
分子式为C5H11Br且含有两个甲基的同分异构体共有(不考虑立体结构)
A.3种 B.4种 C.5种 D.6种
查看答案和解析>>
科目:高中化学 来源:2014-2015学年内蒙古鄂尔多斯市高三模拟化学试卷(解析版) 题型:选择题
已知:2H2(g)+O2(g)=2H2O(l) △H=-571.6kJ/mol
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) △H=-2220 kJ/mol
7molH2与C3H8混合物完全燃烧,共放热5869kJ,则二者的体积比V(H2):V(C3H8)为
A.1:1 B.2:5 C.3:4 D.5:2
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省邛崃市高二下学期第一次月考化学试卷(解析版) 题型:实验题
(10分)利用下图装置测定中和热的实验步骤如下:
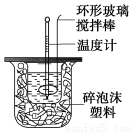
①用量筒量取50 mL 0.25 mol/L硫酸倒入小烧杯中,测出硫酸温度;
②用另一量筒量取50 mL 0.55 mol/L NaOH溶液,并用另一温度计测出其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测出混合液最高温度。
回答下列问题:
(1)写出稀硫酸和稀氢氧化钠溶液反应表示中和热的热化学方程式(中和热数值为57.3 kJ/mol): ___________________________________________________________。
(2)倒入NaOH溶液的正确操作是________(从下列选出)。
A.沿玻璃棒缓慢倒入
B.分三次少量倒入
C.一次迅速倒入
(3)使硫酸与NaOH溶液混合均匀的正确操作是________(从下列选出)。
A.用温度计小心搅拌
B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯
D.用套在温度计上的环形玻璃棒轻轻地搅动
(4)实验数据如下表:
①请填写下表中的空白:
温度 实验次数 | 起始温度t1℃ | 终止温度t2/℃ | 温度差平均值(t2-t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 29.5 | ____________________ |
2 | 27.0 | 27.4 | 27.2 | 32.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.2 | |
4 | 26.4 | 26.2 | 26.3 | 29.8 | |
②近似认为0.55 mol/L NaOH溶液和0.25 mol/L硫酸溶液的密度都是1 g/cm3,中和后生成溶液的比热容c=4.18 J/(g·℃)。则中和热ΔH=___(取小数点后一位)。
③上述实验数值结果与57.3 kJ/mol有偏差,产生偏差的原因可能是(填字母)___。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省邛崃市高二下学期第一次月考化学试卷(解析版) 题型:选择题
下列离子的检验不能达到预期目的是
A.向待测液里加入NaOH溶液,加热,将湿润的红色石蕊试纸放在试管口变蓝,则待测液中肯定含有NH4+
B.用铂丝蘸取待测液在火焰上灼烧,若火焰呈黄色,则表明待测液中肯定含有Na+
C.向待测液里加入过量硝酸无现象,再加入硝酸银溶液,若无沉淀生成,则表明待测液中肯定不含Cl-
D.向待测液里加入BaCl2溶液,若产生白色沉淀,再加入过量稀硝酸白色沉淀不溶解,则表明待测液中肯定含有SO42-
查看答案和解析>>
科目:高中化学 来源:2014-2015江西省宜春市高二下学期第一次月考化学试卷(解析版) 题型:填空题
有机物A的结构简式如图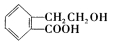 ,它可通过不同的化学反应分别制得B、C和D(下图)三种物质。
,它可通过不同的化学反应分别制得B、C和D(下图)三种物质。

(1)A~D中互为同分异构体的是 。
(2)由AB的化学方程式是 ;
(3)C在一定条件下发生加聚反应的化学方程式是: ;
(4)写出AD的化学方程式 ;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com