
| A. | X与Z两种元素形成的化合物一定是离子化合物,有且只有离子键 | |
| B. | RX2、WX2、Z2X2都能使品红溶液褪色,且褪色原理相同 | |
| C. | R、W所形成的氧化物的水化物的酸性强弱为W>R | |
| D. | X、Y、R、W四种元素形成的气体氢化物中最稳定的是 Y 的气态氢化物 |
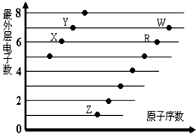
分析 都是短周期元素,由最外层电子数与原子序数关系可知,X、Y处于第二周期,X的最外层电子数为6,故X为O元素,Y的最外层电子数为7,故Y为F元素;Z、R、W处于第三周期,最外层电子数分别为1、6、7,故Z为Na元素、R为S元素、W为Cl元素,据此进行解答.
解答 解:都是短周期元素,由最外层电子数与原子序数关系可知,X、Y处于第二周期,X的最外层电子数为6,故X为O元素,Y的最外层电子数为7,故Y为F元素;Z、R、W处于第三周期,最外层电子数分别为1、6、7,故Z为Na元素、R为S元素、W为Cl元素.
A.X、Z形成的化合物为氧化钠、过氧化钠,均属于离子化合物,但过氧化钠中含有共价键,故A错误;
B.SO2、ClO2、Na2O2都能使品红溶液褪色,SO2u与有色物质化合为不稳定的无色物质,而ClO2、Na2O2将有色物质氧化为无色物质,故B错误;
C.应是最高价氧化物的水化物的酸性强弱为W>R,不是最高价的则不一定,如HClO为弱酸,而硫酸为强酸,故C错误;
D.O、F、S、Cl四种元素中F元素非金属性最强,形成的气体氢化物中最稳定的是氟的气态氢化物,故D正确.
故选:D.
点评 本题考查结构性质位置关系、元素周期律等,难度不大,根据最外层电子数及原子序数的关系确定元素是解题的关键,注意整体把握元素周期表的结构,C选项为易错点,学生容易忽略最高价.


科目:高中化学 来源: 题型:选择题
| A. | 8.15 | B. | 9.3 | C. | 10.15 | D. | 11.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④⑦ | B. | ②④⑥ | C. | ①③⑤ | D. | ④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 压减燃煤、严格控车、调整产业是治理雾霾的有效措施 | |
| B. | 铝及其合金使用广泛,是因为铝比铁更耐酸、碱的腐蚀 | |
| C. | 海水淡化的方法主要有蒸馏法、电渗析法、离子交换法等 | |
| D. | 通常所说的三大合成材料是指塑料、合成橡胶和合成纤维 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3$→_{催化剂△}^{O_{2}}$NO$→_{H_{2}O}^{O_{2}}$HNO3 | |
| B. | 浓HCl$→_{△}^{MnO_{2}}$Cl2$\stackrel{石灰乳}{→}$漂白粉 | |
| C. | Al2O3$\stackrel{HCl(aq)}{→}$AlCl3(aq)$\stackrel{△}{→}$无水AlCl3$\stackrel{电解}{→}$Al | |
| D. | 淀粉$→_{△}^{H_{2}SO_{4}(aq)}$葡萄糖$\stackrel{酒化酶}{→}$C2H5OH$→_{Ag,△}^{O_{2}}$CH3CHO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
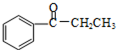 +H2N-NH2$→_{△}^{NaOH/(HOCH_{2}CH_{2})_{2}O}$
+H2N-NH2$→_{△}^{NaOH/(HOCH_{2}CH_{2})_{2}O}$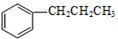 +X(g)+Y(l)
+X(g)+Y(l)| A. | 肼作还原剂 | B. | X是N2 | ||
| C. | Y是H2O | D. | 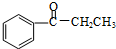 在酸性条件下水解为苯甲酸和乙醇 在酸性条件下水解为苯甲酸和乙醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原混合物中CuO与Fe2O3物质的量的比为1:2 | |
| B. | 原混合物中CuO与Fe2O3的质量比为2:1 | |
| C. | 吸收CO2后的溶液中一定有Ba(HCO3)2 | |
| D. | 反应中生成的CO2体积为1.792L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com