
【题目】某暗紫色化合物A在常温和干燥的条件下,可以稳定存在,但它在水溶液中不稳定,一段时间后转化为红褐色沉淀,同时产生一种气体单质.为探究其成分,某化学兴趣小组的同学取化合物A粉末进行实验.经组成分析,该粉末仅含有O、K、Fe三种元素,另取3.96g化合物A的粉末溶于水,滴加足量的稀硫酸,向反应后的溶液中加入含有0.08mol KOH的溶液,恰好完全反应.过滤,将洗涤后的沉淀充分灼烧,得到红棕色固体粉末1.60g;将所得滤液在一定条件下蒸发可得到一种纯净的不含结晶水的盐10.44g.
(1)化合物A的化学式为化合物A与H2O反应的离子方程式为: .
(2)化合物A可作为一种“绿色高效多功能”水处理剂,可由FeCl3和KClO在强碱性条件下反应制得,其反应的离子方程式为
(3)化合物A还可以作为高容量电池材料,与MnO2﹣Zn电池类似,A﹣Zn也可以组成碱性电池,A在电池中作为正极材料,其电极反应式为 , 该电池总反应的离子方程式为 .
(4)目前,人们针对化合物A的稳定性进行了大量的探索,并取得了一定的进展.下列物质中有可能提高化合物A水溶液稳定性的是
A.醋酸钠
B.醋酸
C.Fe(NO3)3
D.KOH
(5)请设计一个实验方案,研究温度对化合物A水溶液稳定性的影响: .
【答案】
(1)K2FeO4;4FeO42﹣+10H2O=4Fe(OH)3↓+3O2↑+8OH﹣
(2)2Fe3++3ClO﹣+10OH﹣=2FeO42﹣+3Cl?+5H2O
(3)FeO42﹣+3eˉ+4H2O=Fe(OH)3+5OH﹣;3Zn+2FeO42﹣+8H2O=3Zn(OH)2+2Fe(OH)3+4OH﹣
(4)AD
(5)取少量的样品放入试管加水溶解,分成两等份于两试管中,分别放在冷水和热水中,观察生成红褐色沉淀的快慢
【解析】解:(1)3.96g化合物A含铁: ![]() ×2=0.02mol,含钾:
×2=0.02mol,含钾: ![]() ×2﹣0.08mol=0.04mol, 含氧:
×2﹣0.08mol=0.04mol, 含氧: ![]() =0.08mol,钾、铁、氧的个数比为:0.04mol:0.02mol:0.08mol=2:1:4,故A的化学式为:K2FeO4;高铁酸钾与水反应生成氧气和Fe(OH)3、氢氧化钾,反应方程式为4K2FeO4+10H2O=4Fe(OH)3+8KOH+3O2↑,离子方程式为4FeO42﹣+10H2O=4Fe(OH)3↓+3O2↑+8OH﹣ ,
=0.08mol,钾、铁、氧的个数比为:0.04mol:0.02mol:0.08mol=2:1:4,故A的化学式为:K2FeO4;高铁酸钾与水反应生成氧气和Fe(OH)3、氢氧化钾,反应方程式为4K2FeO4+10H2O=4Fe(OH)3+8KOH+3O2↑,离子方程式为4FeO42﹣+10H2O=4Fe(OH)3↓+3O2↑+8OH﹣ ,
所以答案是:K2FeO4;4FeO42﹣+10H2O=4Fe(OH)3↓+3O2↑+8OH﹣;(2)三价铁离子被次氯酸钾氧化为高铁酸钾,次氯酸钾被还原为氯化钾,同时生成H2O,反应的离子方程式为2Fe3++3ClO﹣+10OH﹣=2FeO42﹣+3Cl+5H2O;所以答案是:2Fe3++3ClO﹣+10OH﹣=2FeO42﹣+3Cl+5H2O; (3)原电池的负极发生氧化反应,正极电极反应式为:①FeO42﹣+3eˉ+4H2O=Fe(OH)3+5OH﹣;负极电极反应为:②Zn﹣2e﹣+2OH﹣=Zn(OH)2;依据电极反应的电子守恒,①×2+②×3合并得到电池反应为:3Zn+2FeO42﹣+8H2O=3Zn(OH)2+2Fe(OH)3+4OH﹣ , 所以答案是:FeO42﹣+3eˉ+4H2O=Fe(OH)3+5OH﹣;3Zn+2FeO42﹣+8H2O=3Zn(OH)2+2Fe(OH)3+4OH﹣;(4)A.高铁酸钾在水溶液中不稳定,醋酸钠溶液显碱性可以温度存在,故A正确;B.亚硫酸钠具有还原性,会被高铁酸钾氧化,故B错误;C.在常温和干燥的条件下,高铁酸钾可以稳定的存在,但它在水溶液中不稳定,故C错误;D.高铁酸钾在碱性条件下生成,故D正确;所以答案是:AD;(5)固定其他条件,改变温度,看析出沉淀的快慢,则设计实验为取少量的样品放入试管加水溶解,分成两等份于两试管中,分别放在冷水和热水中,观察生成红褐色沉淀的快慢,所以答案是:取少量的样品放入试管加水溶解,分成两等份于两试管中,分别放在冷水和热水中,观察生成红褐色沉淀的快慢.


 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:高中化学 来源: 题型:
【题目】用系统命名法命名或写出结构简式:
(1)3-甲基-2-丙基-1-戊烯的结构简式为______________________________
(2)![]() 名称为_______________________________________
名称为_______________________________________
(3)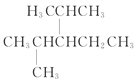 名称为:________________________________
名称为:________________________________
(4)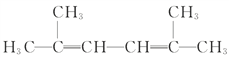 名称为:_______________
名称为:_______________
(5)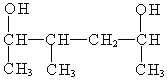 名称为:___________________________
名称为:___________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意填空
(I)甲烷在一定条件下可生成以下微粒:
A.碳正离子(CH3+ ) B.碳负离子(CH3﹣) C.甲基 (﹣CH3) D.碳烯(:CH2)
①四种微粒中,键角为120°的是(填序号).
②碳负离子(CH3﹣)的空间构型为 , 与CH3﹣互为等电子体的一种分子是(填化学式).
(II )在制取合成氨原料气的过程中,常混有一些杂质,如CO会使催化剂中毒.除去CO的化学方程式为(HAc表示醋酸):Cu(NH3)2Ac+CO+NH3=Cu(NH3)3(CO)Ac.请回答下列问题:
①C、N、O的电负性由大到小的顺序为 .
②写出Cu的核外电子排布式 .
③化合物Cu(NH3)3(CO)Ac中,金属元素的化合价为 .
④在一定条件下NH3和CO2能合成尿素CO(NH2)2 , 尿素中C原子轨道的杂化类型为;1mol尿素分子中,σ 键的数目为 .
⑤Cu2O晶体的晶胞结构如图所示,若阿伏伽德罗常数为NA , 晶胞的边长为apm,则晶体的密度为gcm﹣3 . 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在0.5L某浓度的NaCl溶液中含有0.5mol Na+ , 下列对该溶液的说法中,不正确的是( )
A.该溶液的物质的量浓度为1molL﹣1
B.该溶液中含有58.5g NaCl
C.配制100mL该溶液需用5.85g NaCl
D.量取100mL该溶液倒入烧杯中,烧杯中Na+的物质的量为0.1mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】PHB是一种树脂,有机物K是一种抗惊厥药物,它们的合成路线如图: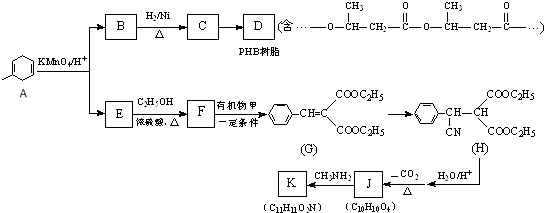
已知:R、R′、R″代表烃基
①RCN ![]() RCOOH
RCOOH
② ![]()
![]() RCOOH+
RCOOH+ ![]()
③ 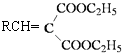
![]()
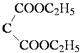 +H2O
+H2O
(1)B→C的反应类型是 .
(2)写出一定条件下C→D的化学方程式: .
(3)有机物甲的结构简式为 .
(4)写出E→F的化学方程式: .
(5)已知1mol J最多与2mol NaHCO3反应;K分子结构中含有一个五元环与一个六元环.写出一定条件下J→K的化学方程式: .
(6)S是A的一种同分异构体,分子中没有环状结构,S的核磁共振氢谱有三个峰,峰面积之比为6:3:1,则S的结构简式为(写出一种即可).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】柠檬烯是一种食用香料,其结构简式为: ![]() 有关柠檬烯的分析正确的是( )
有关柠檬烯的分析正确的是( )
A.分子式为C10H14
B.一定条件下,柠檬烯可以发生加成、取代、氧化、还原反应
C.柠檬烯有属于苯的同系物的同分异构体
D.柠檬烯的分子中所有碳原子可能处在同一个平面上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一无色未知溶液中检验出有Ba2+、Ag+ , 同时又测得其酸性很强.某学生还要鉴定此溶液中是否大量存在①Cu2+ ②Fe3+ ③Cl﹣ ④NO ![]() ⑤S2﹣ ⑥CO
⑤S2﹣ ⑥CO ![]() ⑦NH
⑦NH ![]() ⑧Mg2+ ⑨Al3+ , 而事实上有部分离子不用鉴定就能加以否定,你认为不必鉴定的是( )
⑧Mg2+ ⑨Al3+ , 而事实上有部分离子不用鉴定就能加以否定,你认为不必鉴定的是( )
A.③⑤⑥⑦⑨
B.①②⑤⑥⑧
C.③④⑦⑧⑨
D.①②③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( ) ①将金属Na投入水中:2Na+2H2O=2Na++2OH﹣+H2↑
②在硫酸溶液中加入氢氧化钡溶液至中性:Ba2++OH﹣+H++SO ![]() =BaSO4↓+H2O
=BaSO4↓+H2O
③碳酸氢钙溶液中滴加盐酸:HCO ![]() +H+=CO2↑+H2O
+H+=CO2↑+H2O
④碳酸钙中滴加盐酸:CO ![]() +2H+=CO2↑+H2O.
+2H+=CO2↑+H2O.
A.①③④
B.①③
C.②④
D.①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,近来发现了一种新的星际分子氰基辛炔,其结构简式为HC≡C—C≡C—C≡C—C≡C—C≡N。下列对该物质的判断正确的是( )
A.属于不饱和烃
B.不能使酸性KMnO4溶液褪色
C.所有原子都在同一条直线上
D.可由乙炔和含氮化合物加聚制得
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com