
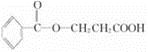 或
或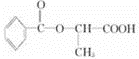 .
. 分析 先根据A和B的相对分子质量都小于200及A+H2O=C7H6O2+B推断出B的相对分子质量小于96,再根据B的化学性质推断其含有的官能团类型,再根据B中碳、氢元素总的质量分数为46.67%计算出氧元素的质量分数,通过讨论判断B分子中氧原子数目及从而计算出B的分子量,然后根据反应A+H2O=C7H6O2+B得出A的分子量,最后结合A的化学性质判断其可能的 结构简式,以此解答该题.
解答 解:(1)因为1molA水解生成1mol苯甲酸和1molB,根据反应A+H2O=C7H6O2+B可知:A与B相对分子质量之差为:122-18=104,
故答案为:104;
(2)因为A和B的相对分子质量都小于200,所以B的相对分子质量小于96,
B中碳、氢元素总的质量分数为46.67%,所以氧原子的质量分数为:1-46.67%=53.33%,
B不发生银镜反应,但跟NaHCO3溶液反应放出CO2,故B中含有羧基,又因为B是A的水解产物,所以B中至少含有3个氧原子,
故答案为:3;
(3)由于B的相对分子质量小于96,故B中氧原子的个数最多为:$\frac{96×0.5333}{16}$=3.2,
即:B中只能含有3个氧原子,其相对分子质量为:$\frac{3×16}{0.5333}$=90,
因为B燃烧时消耗的氧气与生成的二氧化碳的物质的量相等,所以根据有机物的燃烧通式为:CnHmOz+(n+$\frac{m}{4}$-$\frac{z}{2}$)O2→nCO2+$\frac{m}{2}$H2O可知:n+$\frac{m}{4}$-$\frac{z}{2}$=n,
即:m=2z.由于B中含有3个氧原子,即z=3,则m=6,
再根据B的相对分子质量小于96可知:12n+6+16×3=90,解得:n=3,
所以B的分子式C3H6O3,其结构简式可能为:HOCH2CH2COOH或CH3CHOHCOOH,
根据质量守恒定律知A的分子式为:C10H10O4,且A溶液具有酸性,但遇FeCl3溶液不显色,则A中含有酯基、羧基,不含酚羟基,
所以A可能的结构简式为: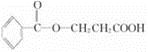 或
或 ,
,
故答案为: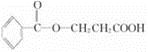 或
或 .
.
点评 本题考查有机物的推断,侧重有机物分子式、结构简式的计算,题目难度中等,熟练掌握常见有机物结构与性质为解答关键,注意明确计算有机物分子式、结构简式的方法,试题充分考查了学生的分析、理解能力及灵活应用所学知识的能力.


科目:高中化学 来源: 题型:填空题
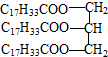 .从酯的性质看,油脂A在酸性条件下和碱性条件下均能发生水解,水解的共同产物是
.从酯的性质看,油脂A在酸性条件下和碱性条件下均能发生水解,水解的共同产物是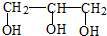 (写结构简式).
(写结构简式).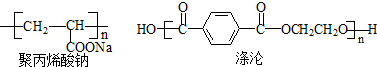
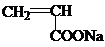 ,反应类型是加聚反应;
,反应类型是加聚反应;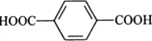 ,其核磁共振氢谱的峰面积比是1:2(或2:1).
,其核磁共振氢谱的峰面积比是1:2(或2:1).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 凡是含有碳元素的化合物都属于有机物 | |
| B. | 大多数有机物都是由分子构成的 | |
| C. | 有机物都很容易燃烧 | |
| D. | 易溶于汽油、酒精、苯等有机溶剂中的物质,一定是有机物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④⑥⑦ | B. | ②③⑤⑦ | C. | ②⑤⑦ | D. | ②④⑤⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ②③ | C. | ①③ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
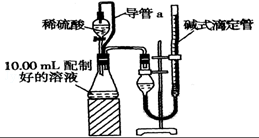 实验室测定碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数W(Na2CO3),称取此混合物5.0g,溶于水中,配成250mL溶液
实验室测定碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数W(Na2CO3),称取此混合物5.0g,溶于水中,配成250mL溶液查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ①②③⑤ | C. | ①④⑤ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ①③④ | C. | ②③④ | D. | ①②③ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com