
| ŹµŃéÄæµÄ | ²Ł×÷ | ŹµŃéĻÖĻó | ½įĀŪ |
| 1£®¼ģŃéCl- | ȔɣŠķĀĖŅŗÓŚŹŌ¹ÜÖŠ£¬¼ÓČėĻõĖįĖį»ÆµÄĻõĖįŅųČÜŅŗ | ²śÉś°×É«³Įµķ | ŗ¬ÓŠCl- |
| 2£®¼ģŃéNH4+ | ȔɣŠķĀĖŅŗÓŚŹŌ¹ÜÖŠ£¬¼ÓČėÅØĒāŃõ»ÆÄĘČÜŅŗ²¢¼ÓČČ£¬½«ČóŹŖµÄŗģÉ«ŹÆČļŹŌÖ½ÖĆÓŚŹŌ¹ÜæŚø½½ü | ŹÆČļŹŌÖ½±äĄ¶É« | ŗ¬ÓŠNH4+””k |
| 3£®¼ģŃéZn2+ | ȔɣŠķĀĖŅŗÓŚŹŌ¹ÜÖŠ£¬¼ÓČėĻ”°±Ė® | ĻČ²śÉś°×É«³Įµķ£¬¼ĢŠų¼ÓČė°±Ė®£¬³ĮµķÓÖČܽā | ŗ¬ÓŠZn2+ |
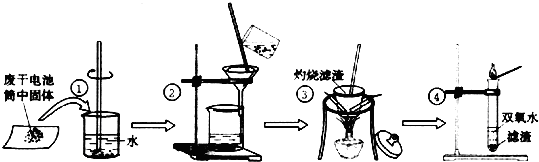
·ÖĪö £Ø1£©¹ĢĢåĪļÖŹ¼ÓČėĖ®ÖŠŹĒĪļÖŹµÄČܽā¹ż³Ģ£¬·ÖĄė¹ĢĢåŗĶŅŗĢåÓĆ¹żĀĖµÄ·½·Ø£»
£Ø2£©øł¾Ż¶ŌĪļÖŹ½ųŠŠ×ĘÉÕ¹ż³ĢŠčŅŖµÄŅĒĘ÷£ŗ¾Ę¾«µĘ”¢²£Į§°ō”¢ÄąČż½ĒŗĶČż½Å¼Ü”¢ŪįŪöĄ“»Ų“š£¬Ģ¼µ„ÖŹ×ĘÉÕ»į²śÉś¶žŃõ»ÆĢ¼£»
£Ø3£©ÄÜŹ¹Ė«ŃõĖ®ŃøĖŁ²śÉśŃõĘųµÄŗŚÉ«ĪļÖŹŹĒ¶žŃõ»ÆĆĢ£®
£Ø4£©ĀČĄė×ӵļģŃéŹĒÓĆĻõĖįĖį»ÆµÄĻõĖįŅųČÜŅŗ£¬Čō²śÉś°×É«³Įµķ£¬¾ĶÖ¤Ć÷ŗ¬ÓŠĀČĄė×Ó£»
ļ§øłĄė×ӵļģŃéŹĒÓĆÅØĒāŃõ»ÆÄĘČÜŅŗ²¢¼ÓČČ£¬Č»ŗóÓĆŹŖČóµÄŗģÉ«ŹÆČļŹŌÖ½¼ģŃ飬°±ĘųÄÜŹ¹ŹŖČóµÄŗģÉ«ŹÆČļŹŌÖ½±äĄ¶É«£®
½ā“š ½ā£ŗ£Ø1£©¹ĢĢåĪļÖŹ¼ÓČėĖ®ÖŠŹĒĪļÖŹµÄČܽā¹ż³Ģ£¬·ÖĄė¹ĢĢåŗĶŅŗĢåÓĆ¹żĀĖµÄ·½·Ø£»¹Ź“š°øĪŖ£ŗČܽā£»¹żĀĖ£»
£Ø2£©¶ŌĪļÖŹ½ųŠŠ×ĘÉÕ¹ż³ĢŠčŅŖµÄŅĒĘ÷£ŗ¾Ę¾«µĘ”¢²£Į§°ō”¢ÄąČż½ĒŗĶČż½Å¼Ü”¢ŪįŪöŹ¹³ĪĒåŹÆ»ŅĖ®±ä»ė×ĒµÄĘųĢåÓŠ¶žŃõ»ÆĢ¼ŗĶ¶žŃõ»ÆĮņ£¬¶žŃõ»ÆĢ¼æÉÓÉŗŚÉ«µÄĢ¼µ„ÖŹ×ĘÉÕÖĘµĆ£¬¶žŃõ»ÆĮņæÉÓɵ»ĘÉ«µÄĮņµ„ÖŹ×ĘÉÕÖĘµĆ£¬ĖłŅŌøĆŗŚÉ«ĪļÖŹŹĒĢ¼µ„ÖŹ£®
¹Ź“š°øĪŖ£ŗŪįŪö£»ÄąČż½Ē£»C£ØĢ¼£©£»
£Ø3£©ÄÜŹ¹“ų»šŠĒµÄľĢõø“Č¼µÄĘųĢåŹĒŃõĘų£¬ÄÜŹ¹Ė«ŃõĖ®ŃøĖŁ²śÉśŃõĘųµÄŗŚÉ«¹ĢĢåĪļÖŹŹĒ¶žŃõ»ÆĆĢ£¬¹Ź“š°øĪŖ£ŗMnO2£»
£Ø4£©ĀČĄė×ӵļģŃé£ŗȔɣŠķĀĖŅŗÓŚŹŌ¹ÜÖŠ£¬¼ÓČėĻõĖįĖį»ÆµÄĻõĖįŅųČÜŅŗ£¬ŅųĄė×ÓŗĶĀČĄė×Ó·“Ӧɜ³É²»ČÜÓŚĖ®µÄ°×É«³ĮµķĀČ»ÆŅų£»Čē¹ūÓŠ°×É«³ĮµķÉś³É£¬¾ĶĖµĆ÷ÓŠĀČĄė×Ó£®
ļ§øłĄė×ӵļģŃé£ŗļ§øłĄė×ÓÄÜŗĶĒæ¼īŌŚ¼ÓČČĢõ¼žĻĀ·“Ӧɜ³É°±Ęų£¬°±ĘųÄÜŹ¹ŹŖČóµÄŗģÉ«ŹÆČļŹŌÖ½±äĄ¶É«£»Čē¹ūŹŖČóµÄŗģÉ«ŹÆČļŹŌÖ½±äĄ¶É«£¬¾ĶĖµĆ÷ÓŠļ§øłĄė×Ó“ęŌŚ£®
¹Ź“š°øĪŖ£ŗ
| ŹµŃéÄæµÄ | ²Ł×÷ | ŹµŃéĻÖĻó | ½įĀŪ |
| 1”¢¼ģŃéCl- | ȔɣŠķĀĖŅŗÓŚŹŌ¹ÜÖŠ£¬¼ÓČėĻõĖįĖį»ÆµÄĻõĖįŅųČÜŅŗ | ÓŠ°×É«³ĮµķÉś³É | ŗ¬ÓŠCl- |
| 2”¢¼ģŃéNH4+ | ȔɣŠķĀĖŅŗÓŚŹŌ¹ÜÖŠ£¬¼ÓČėÅØĒāŃõ»ÆÄĘČÜŅŗ²¢¼ÓČČ£¬½«ČóŹŖµÄŗģÉ«ŹÆČļŹŌÖ½ÖĆÓŚŹŌ¹ÜæŚø½½ü | ŹÆČļŹŌÖ½±äĄ¶É« | ŗ¬ÓŠNH4+ |
µćĘĄ ±¾Ģāæ¼²éĪļÖŹµÄ·ÖĄė”¢Ģį“æµÄ×ŪŗĻ²Ł×÷£¬ĪŖøßĘµæ¼µć£¬²ąÖŲӌѧɜµÄ·ÖĪöÄÜĮ¦ŗĶŹµŃéÄÜĮ¦µÄ漲飬ĢāÄæ²ąÖŲæ¼²é»ł±¾ŹµŃé²Ł×÷¼°Ąė×ӵļģŃ飬ÄŃ¶Č²»“ó£¬ŹģĻ¤ÖŠŃ§½×¶Ī³£¼ūŅõŃōĄė×ӵļģŃé·½·Ø£¬ČēĀČĄė×Ó”¢ĮņĖįøłĄė×Ó”¢ÄĘĄė×Ó”¢¼ŲĄė×Ó”¢ļ§øłĄė×ÓµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÉŁĮ潚ŹōÄʱ£“ęŌŚĆŗÓĶÖŠ | |
| B£® | ŹŌ¼ĮĘæÖŠµÄŅŗäåæÉÓĆĖ®·ā“ę£¬·ĄÖ¹äå»Ó·¢ | |
| C£® | ±£“ęĮņĖįŃĒĢśČÜŅŗŹ±£¬ŅŖĻņĘäÖŠ¼ÓČėÉŁĮæĮņĖįŗĶĢś·Ū | |
| D£® | ÅØĻõĖįÓĆ“ųĻš½ŗČūµÄĻøæŚ”¢×ŲÉ«ŹŌ¼ĮĘæŹ¢·Å£¬²¢Öü“ęŌŚŅõĮ¹“¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
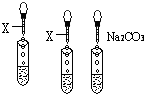 ŹµŃéŹŅÓŠČżĘæŹ§Č„±źĒ©µÄĪŽÉ«ČÜŅŗ£ŗĀČ»Æ¼Ų”¢ĒāŃõ»ÆøĘŗĶĻ”ĮņĖį£¬æÉÓĆŅ»ÖÖ³£¼ūĖį¼īÖøŹ¾¼ĮX »ņNa2CO3Ņ»“Ī¼ų±šĖüĆĒ£®øł¾ŻÓŠ¹Ų²Ł×÷¼°Ėł¼ÓŹŌ¼ĮĢīæÕ£®
ŹµŃéŹŅÓŠČżĘæŹ§Č„±źĒ©µÄĪŽÉ«ČÜŅŗ£ŗĀČ»Æ¼Ų”¢ĒāŃõ»ÆøĘŗĶĻ”ĮņĖį£¬æÉÓĆŅ»ÖÖ³£¼ūĖį¼īÖøŹ¾¼ĮX »ņNa2CO3Ņ»“Ī¼ų±šĖüĆĒ£®øł¾ŻÓŠ¹Ų²Ł×÷¼°Ėł¼ÓŹŌ¼ĮĢīæÕ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Fe+2 H+=Fe3++H2”ü | B£® | Fe3++Cu=Cu2++Fe2+ | ||
| C£® | Cu+2H+=Cu2++H2”ü | D£® | 2Fe3++Fe=3Fe2+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ${\;}_{\;}^{13}$OŗĶ14O»„³ĘĶ¬ĖŲŅģŠĪĢå | B£® | ±ūĶéŗĶŅģ¶”Ķ黄³ĘĶ¬ĻµĪļ | ||
| C£® | ½šøÕŹÆŗĶŹÆÄ«»„³ĘĶ¬Ī»ĖŲ | D£® | 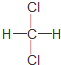 ŗĶ ŗĶ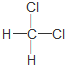 »„³ĘĶ¬·ÖŅģ¹¹Ģå »„³ĘĶ¬·ÖŅģ¹¹Ģå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ĪļÖŹ | æŖŹ¼³Įµķ | ³ĮµķĶźČ« |
| Fe£ØOH£©2 | 7.6 | 9.6 |
| Fe£ØOH£©3 | 2.7 | 3.7 |
| Cu£ØOH£©2 | 4.4 | 8.0 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com