
实验室用KClO3和浓盐酸反应也可以制备氯气。某研究性学习小组利用如图所示装置在实验室中制取Cl2并探究其相关性质:
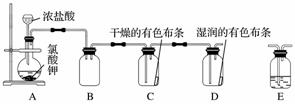
(1)装置A中存在一处错误,请改正这处错误:________________________。
(2)写出装置A中发生反应的化学方程式:________________________________________________________________________
________________________________________________________________________。
(3)为了除去氯气中的氯化氢,需要在装置A、B之间添加装置E,装置E中所盛装的试剂为________________。为了探究使有色布条褪色的是氯气还是氯气与水反应的生成物,需要在整套装置中添加装置E,其中加入浓硫酸,装置E在整套装置中的添加位置为________(填字母)。
a.A、B之间 b.B、C之间
c.C、D之间 d.D之后
(4)取下集气瓶B,将铁丝加热至红热状态,伸入集气瓶B中,可以观察到的现象是______________________,能检验该反应产物中铁元素价态的试剂是________(填字母)。
a.氯水 b.蒸馏水和铁粉
c.氢氧化钠溶液 d.KSCN溶液
(5)另外一个化学学习小组就环境保护方面指出了上述装置的缺陷,并给出了改进措施,该改进措施是________________________________________________________________________
__________________________。
答案 (1)长颈漏斗换为分液漏斗
(2)KClO3+6HCl(浓)===KCl+3Cl2↑+3H2O
(3)饱和食盐水 b
(4)集气瓶内有棕褐色烟产生 bcd
(5)在装置D后增加一个盛装碱液的装置,用碱液吸收剩余的氯气
解析 (1)长颈漏斗与分液漏斗的结构不同,前者无控制活塞,不能控制液体的添加量,而且制备的气体会从“长颈”中逸出。(2)该反应中,氯酸钾是氧化剂,将HCl氧化,氧化产物即氯气。(3)干燥的氯气没有漂白作用,而制备的氯气中往往含有水蒸气,为了排除水蒸气对探究氯气不具备漂白作用的干扰,需要对氯气进行干燥。(4)铁丝在氯气中的燃烧产物为氯化铁。氯水与氯化铁不反应;氯化铁溶液与铁粉可以发生反应,生成氯化亚铁;氯化铁与氢氧化钠溶液反应生成红褐色的氢氧化铁沉淀;铁离子与KSCN溶液反应,现象为溶液变血红色。(5)氯气有毒,实验中需要对尾气进行处理。


 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:
近日国内知名山茶油品牌“金浩茶油”被多家媒体曝光致癌物苯并(a)芘含量超标。苯并(a)芘是一种致癌物、致畸原及诱变
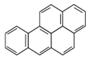
剂,也是多环芳烃中毒性最大的一种强致癌物。苯并(a)芘的结构简式如图所示,下列有关苯并(a)芘的说法中不正确的是( )
A.苯并(a)芘的分子式为C20H12,属于稠环芳香烃
B.苯并(a)芘与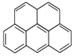 互为同分异构体
互为同分异构体
C.苯并(a)芘在一定条件下可以发生取代反应,能使酸性KMnO4溶液褪色
D.苯并(a)芘不易溶于水,易溶于苯、氯仿等有机溶剂
查看答案和解析>>
科目:高中化学 来源: 题型:
二氧化氯(ClO2)是一种高效、广谱、安全的杀菌消毒剂。
(1)氯化钠电解法是一种可靠的工业生产ClO2的方法。
①用于电解的食盐水需先除去其中的Ca2+、Mg2+、SO 等杂质。除杂操作时,往粗盐水中先加入过量的________(填化学式),至沉淀不再产生后,再加入过量的Na2CO3和NaOH,充分反应后将沉淀一并滤去。经检测发现滤液中仍含有一定量的SO
等杂质。除杂操作时,往粗盐水中先加入过量的________(填化学式),至沉淀不再产生后,再加入过量的Na2CO3和NaOH,充分反应后将沉淀一并滤去。经检测发现滤液中仍含有一定量的SO ,其原因是________________________________________________________________________。
,其原因是________________________________________________________________________。
[已知:Ksp(BaSO4)=1.1×10-10,Ksp(BaCO3)=5.1×10-9]
②该法工艺原理如下图。其过程是将食盐水在特定条件下电解得到的氯酸钠(NaClO3)与盐酸反应生成ClO2。

工艺中可以利用的单质有________(填化学式),发生器中生成ClO2的化学方程式为________________________________________________________________________。
(2)纤维素还原法制ClO2是一种新方法,其原理是:纤维素水解得到的最终产物D与NaClO3反应生成ClO2。完成反应的化学方程式:
 __(D)__+24NaClO3+12H2SO4===
__(D)__+24NaClO3+12H2SO4=== ClO2↑+
ClO2↑+ CO2↑+18H2O+
CO2↑+18H2O+ ________
________
(3)ClO2和Cl2均能将电镀废水中的CN-氧化为无毒的物质,自身被还原为Cl-。处理含CN-相同量的电镀废水,所需Cl2的物质的量是ClO2的________倍。
查看答案和解析>>
科目:高中化学 来源: 题型:
a mol Cu与含b mol HNO3的溶液恰好完全反应,被还原的HNO3的物质的量一定是( )
A.(b-2a) mol B.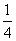 b mol
b mol
C.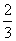 a mol D.2a mol
a mol D.2a mol
查看答案和解析>>
科目:高中化学 来源: 题型:
与Cl2相比较,ClO2处理水时被还原成Cl-,不生成有机氯代物等有害物质。工业上可用亚氯酸钠和稀盐酸为原料制备ClO2,反应如下:
NaClO2+HCl—→ClO2↑+________(没有配平)
(1)上述方程式中,缺项物质是________,配平方程式,并在下面补全反应物系数。
 NaClO2+
NaClO2+ HCl—→
HCl—→
(2)该反应中氧化剂和还原剂的物质的量之比是________________________________________________________________________。
生成0.2 mol ClO2转移电子的物质的量为________ mol。
(3)ClO2对污水中的Fe2+、Mn2+、S2-和CN-等有明显的去除效果。某污水中含CN- a mg·L-1,现用ClO2将CN-氧化,只生成两种无毒气体。处理100 m3这种污水,至少需要ClO2________ mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
某实验小组用工业上废弃固体(主要成分Cu2S和Fe2O3)混合物制取粗铜和Fe2(SO4)3晶体,设计的操作流程如下:

(1)③实验操作中用到的玻璃仪器有__________________。
(2)③④操作中会有一种气体生成,若在实验室制备该气体,可选择下列哪些装置________(填字母)。
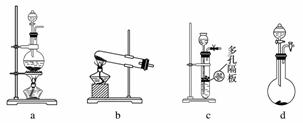
(3)溶液B在空气中放置有可能变质,如何检验溶液B是否变质:__________________。
(4)溶液B加稀硫酸酸化后加强氧化剂X,试剂X最好选择下列哪种试剂______________(填字母)。
a.Cl2 b.H2O2 c.KMnO4
试剂X在酸性条件下与溶液B反应的离子方程式为________________________。
(5)由溶液C经________、________、过滤等操作得Fe2(SO4)3晶体。
(6)某同学用实验制得的Fe2(SO4)3晶体配制0.1 mol·L-1的Fe2(SO4)3溶液,在称量出Fe2(SO4)3晶体后,溶解该晶体的具体操作为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
对比以下几个反应式:
Cl+Cl―→Cl2,ΔH=-247 kJ·mol-1;
O+O―→O2,ΔH=-493 kJ·mol-1;
N+N―→N2,ΔH=-946 kJ·mol-1。
可以得出的结论是( )
A.在常温下氮气比氧气和氯气稳定
B.氮、氧和氯的单质常温下为气体
C.氮、氧和氯都是双原子分子
D.氮气、氧气和氯气的密度不同
查看答案和解析>>
科目:高中化学 来源: 题型:
中华人民共和国国家标准(GB27602011)规定葡萄酒中SO2最大使用量为0.25 g·L-1。某兴趣小组用题图1装置(夹持装置略)收集某葡萄酒中SO2,并对其含量进行测定。
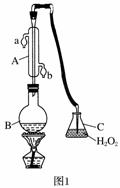

(1)仪器A的名称是______________,水通入A的进口为________。
(2)B中加入300.00 mL葡萄酒和适量盐酸,加热使SO2全部逸出并与C中H2O2完全反应,其化学方程式为________________________________。
(3)除去C中过量的H2O2,然后用0.090 0 mol·L-1NaOH标准溶液进行滴定,滴定前排气泡时,应选择题图2中的________;若滴定终点时溶液的pH=8.8,则选择的指示剂为________;若用50 mL滴定管进行实验,当滴定管中的液面在刻度“10”处,则管内液体的体积(填序号)________(①=10 mL,②=40 mL,③<10 mL,④>40 mL)。
(4)滴定至终点时,消耗NaOH溶液25.00 mL,该葡萄酒中SO2含量为________g·L-1。
(5)该测定结果比实际值偏高,分析原因并利用现有装置提出改进措施________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
H3PO2也可用电渗析法制备。“四室电渗析法”工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过):
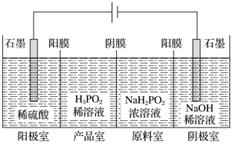
①写出阳极的电极反应式______________________________________________。
②分析产品室可得到H3PO2的原因__________________________________________
________________________________________________________________________。
③早期采用“三室电渗析法”制备H3PO2:将“四室电渗析法”中阳极室的稀硫酸用H3PO2稀溶液代替。并撤去阳极室与产品室之间的阳膜,从而合并了阳极室与产品室。其缺点是产品中混有____________杂质。该杂质产生的原因是________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com