
| A. | ②是化合反应 | B. | ①②③是氧化还原反应 | ||
| C. | ①③是置换反应 | D. | ①③是复分解反应 |
分析 化合反应的特点为“多变一”,分解反应的特点为“一变多”,置换反应的特点为“单质+化合物═单质+化合物”,复分解反应的特点为“化合物+化合物═化合物+化合物,且两种反应物相互交换成分”,氧化还原反应即有化合价变化的反应,然后根据具体的化学方程式进行分析、判断,从而得出正确的结论.
解答 解:由化学方程式可知,①③反应中的反应物和生成物都是一种单质和一种化合物,属于置换反应;②中的反应物是两种,生成物是一种,属于化合反应,①②③都有有化合价变化,则都是氧化还原反应,所以ABC正确,D错误;
故选:D.
点评 本题考查化学基本反应类型,题目难度不大,解答本题要掌握反应类型的判断方法,只有这样才能对各种反应类型做出正确的判断.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cs+、K+、Mg2+、Al3+ | B. | F、F-、Cl-、Br- | ||
| C. | Ca2+、K+、S2-、Cl- | D. | Al、Al3+、Mg、K |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将作物秸秆通过化学反应转化为乙醇用作汽车燃料 | |
| B. | 大力研发新型有机溶剂替代水作为萃取剂 | |
| C. | 利用CO2合成聚碳酸酯类可降解塑料,实现“碳”的循环利用 | |
| D. | 使用资源节约型、环境友好型的生物降解塑料包装袋 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
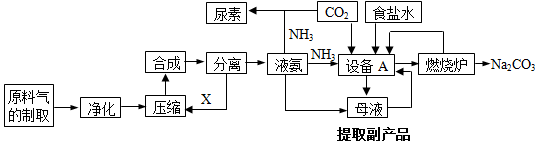
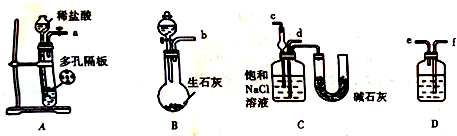
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,48gO3含有的氧原子数为3NA | |
| B. | 1 mol OH-所含的电子数为9NA | |
| C. | 常温常压下,11.2 L氧气所含的原子数为NA | |
| D. | 物质的量浓度为1mol/L MgCl2溶液,含有Cl-离子数为2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com