
分析 先根据n=cV计算出硫酸、一水合氨的物质的量,然后判断反应后溶质组成;得到的溶液能使酚酞显红色,说明混合液显示碱性,然后根据溶质组成及盐的水解原理判断NH4+、NH3•H2O、SO42-三种微粒的物质的量浓度大小.
解答 解:100mL 1.6mol/L稀氨水中含有溶质一水合氨的物质的量为:1.6mol/L×0.1L=0.16mol,
10mL 4.0mol/L稀硫酸中含有硫酸的物质的量为:4.0mol/L×0.01L=0.04mol,
0.04mol硫酸与氨水完全反应生成硫酸铵消耗一水合氨0.04mol,一水合氨还剩余0.08mol,
即:反应后的溶液为0.04mol硫酸铵和0.08mol一水合氨,说明铵根离子和一水合氨的浓度相等,
得到的溶液能使酚酞显红色,说明混合液显示碱性,则一水合氨的电离程度大于铵根离子的水解程度,故:[NH4+]>[NH3?H2O],
由于硫酸根离子的物质的量为0.04mol,溶质一水合氨的物质的量为0.08mol,且一水合氨为弱电解质,电离程度较小,则[NH3?H2O]>[SO42-],
混合液中NH4+、NH3•H2O、SO42-的浓度大小为:[NH4+]>[NH3?H2O]>[SO42-],
故答案为:[NH4+]>[NH3?H2O]>[SO42-].
点评 本题考查了粒子浓度大小比较,题目难度中等,明确混合液中溶质组成为解答关键,注意掌握盐的水解原理及其应用方法,试题培养了学生的分析、理解能力及灵活应用基础知识的能力.


科目:高中化学 来源: 题型:选择题
| A. | 7:1 | B. | 7:2 | C. | 7:3 | D. | 7:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 8种 | B. | 7种 | C. | 6种 | D. | 5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1H2、2H2--同位素 | B. | HCOOCH3、CH3OCHO--同分异构体 | ||
| C. | S2-、S22---同素异形体 | D. | 甲基丙烯酸、油酸--同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
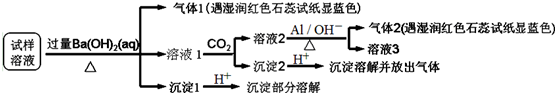
| A. | 试样中肯定存在NH4+、SO42-和NO3-,可能有Mg2+ | |
| B. | 试样中不一定存在Na+、Cl-、HCO3- | |
| C. | 沉淀2中可能含碳酸钡、碳酸镁和氢氧化铝 | |
| D. | 该雾霾中可能存在NaNO3、NH4HCO3和MgSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,2.8gN2与C2H4的混合气体中含有的电子数为1.4NA | |
| B. | 标准状况下,1.12L NO与1.12LO2的混合物中含有的原子数为0.2NA | |
| C. | 25℃时,pH=13的Ba(OH)2溶液中含有的OH-数目为0.1NA | |
| D. | 常温下,1L0.1mol•L-1的NH4NO3溶液中氧原子数为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
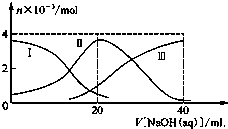 常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图所示(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-),根据图示判断,下列说法正确的是( )
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图所示(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-),根据图示判断,下列说法正确的是( )| A. | 当V[NaOH(aq)]=20 mL时,溶液中离子浓度大小关系:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) | |
| B. | 等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水大 | |
| C. | H2A第一步电离的方程式为H2A→HA-+H+ | |
| D. | 向NaHA溶液加入水稀释的过程中,pH可能增大也可能减少 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 用分液的方法分离乙醇和乙酸 | |
| B. | 用NaOH溶液除去溴苯中的溴 | |
| C. | 用NaAlO2溶液和过量盐酸制备Al(OH)3 | |
| D. | 用足量铁粉除去FeCl2溶液中的FeCl3杂质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该温度下,0.005mol/L H2A溶液中水电离出的c(H+)=10-12mol/L | |
| B. | H2A在水溶液中的电离方程式为:H2A?H++HA-,HA-?A2-+H+ | |
| C. | (NH4)2A溶液中存在离子浓度关系:(NH4+)>(A2-)>(H+)>(OH-) | |
| D. | 等体积等浓度的盐酸与H2A溶液分别与5.6gFe反应,H2A产生的H2多 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com