
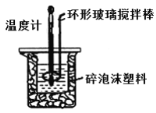
����Ŀ��ijͬѧ��50 mL 0.50mol��L-l������50 mL 0.55 mol��L-1NaOH��Һ������ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������������к��ȣ��ش��������⣺
��1����ʵ��С����������ʵ�飬ÿ��ȡ��Һ��50 mL������ʵ�����ݼ�¼���£�
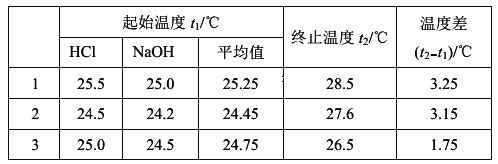
��֪���ᡢNaOH��Һ���ܶ���ˮ��ͬ���кͺ����ɵ���Һ�ı�����c=4. 2��10-3kJ��(g����)����÷�Ӧ���к�����H=__________��
��2������50 mL 0.55 mol��L-1�İ�ˮ(NH3��H2O)����NaOH��Һ��������ʵ�飬ͨ����õķ�Ӧ���������к��ȣ���õ��к�����H��____������ƫС������ƫ��������������������ԭ����___________________________________��
��3����ͨ��ʵ��ⶨ�к��ȵ���H�ľ���ֵ����С��57.3kJ/mol����ԭ�������_____________
A��ʵ��װ�ñ��¡�����Ч����
B���ֶ�ΰ�NaOH��Һ����ʢ�������С�ձ���
C����ȡNaOH��Һ�����ʱ���Ӷ���
���𰸡�-53.76 kJ.mol-1ƫ��һˮ�ϰ�Ϊ������ʣ���Ӧ�����е�����Ҫ�����������ʷų�������ƫ�٣���Hƫ��ABC
��������
��1��50 mL 0.50mol��L-l������50 mL 0.55 mol��L-1NaOH��Һ��Ӧ����ˮ�����ʵ���Ϊ:
0.05L��0.5mol/L=0.0025mol����Һ������Ϊ100g,�¶ȱ仯��ֵΪ��(t2t1)�棬������������ǰ�����������ϴ���ʱ���ܳ��ִ��������ƽ��ֵʱֻ��ǰ���ߣ���ƽ��ֵΪ��![]() ���ų�������ΪQ=mc��T=100g��4.2��103kJ/(g��)��3.20��,����ʵ���õ��к�����H=100g��4.2��103kJ/(g��)��3.20��/0.0025mol= -53.76 kJ.mol-1��
���ų�������ΪQ=mc��T=100g��4.2��103kJ/(g��)��3.20��,����ʵ���õ��к�����H=100g��4.2��103kJ/(g��)��3.20��/0.0025mol= -53.76 kJ.mol-1��
��2��һˮ�ϰ�Ϊ������ʣ�������ʵ�����Ҫ���ȣ���˷ų�������ƫ�٣���Hƫ��
��3��A��ʵ��װ�ñ��¡�����Ч����������ɢʧ���ᵼ�²������ƫС����A��ȷ��
B���ֶ�ΰ�NaOH��Һ����ʢ�������С�ձ��У�����ʱ�䳤���������ɢʧ���ᵼ�²������ƫС����B��ȷ��
C����ȡNaOH��Һ�����ʱ���Ӷ�����������Һ��Һ������ᵼ���¶Ȳ�������ƫС���������ս��ƫС����C��ȷ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��W��X��Y��Z��ԭ���������ε�����a��b��c��d��e��f������ЩԪ����ɵĻ����dΪ���ӻ������ṹ�л����Ǽ��Թ��ۼ���mΪԪ��Y�ĵ��ʣ�ͨ��Ϊ��ɫ��ζ�����塣�������ʵ�ת����ϵ��ͼ��ʾ������˵����ȷ����

A. ԭ�Ӱ뾶:W<X<Y<Z
B. �����ӵĻ�ԭ�ԣ�Y>W
C. a������W��X����Ԫ�����
D. ͼ��ת������d��������Ϊ��Ӧ��ʱ����Ϊ���������ǻ�ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��HCN(aq)��NaOH(aq)��Ӧ����H=��12.1kJ /mol��HCl(aq)��NaOH(aq)��Ӧ����H =��55.6kJ/ mol����HCN��ˮ��Һ�е������H����
A. ��67.7 kJ /mol B. ��43.5kJ /mol C. +43.5 kJ/ mol D. +67.7 kJ/ mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ���������ֵ������˵����ȷ����
A. 24gMg������N2��Ӧ����Mg3N2,ת�Ƶĵ�����Ϊ6NA
B. lmolNa218O2��������������Ϊ42NA
C. 9.8g��H2SO4��H3PO4��ɵĻ�����к��е���ԭ����Ϊ0.4NA
D. 1mol�������к��еĹ��ۼ���Ϊ12NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����ʱ��0.1 mol/LijһԪ��HA��ˮ����0.1%�������룬���������������( )
A. ����Һ��pH=4 B. �����¶ȣ���Һ��pH�͵���ƽ�ⳣ������С
C. ����ĵ���ƽ�ⳣ��ԼΪ1��10-7 D. ����������HA������̶ȼ�С����ƽ�ⳣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������仯������;�dz��㷺���ش���������:
��1����̬��ԭ�ӵļ۵����Ų�ʽΪ_________________��
��2��C2F4�����ںϳɾ��ķ���ϩ,HBF4������ʴ�̲�����NO2F����������ƽ����е���������NaAlF6��������ұ�����������
��C2F4�������������ۼ���������_____��C2F4������̼ԭ�ӵ��ӻ����������____�����ķ���ϩ��һ�����壬֤�������Ǿ�����õ�ʵ�鷽����_______________��
��HF��BF3���Ͽɵõ�HBF4���Ӽۼ��γɽǶȷ���HF��BF3�ܻ��ϵ�ԭ��_______________��
����NO2F���ӻ�Ϊ�ȵ��ӵķǼ��Է�����__________(дһ������Ҫ��Ļ�ѧʽ����)��
��3��CaF2�ľ���ṹ��ͼ��ʾ��
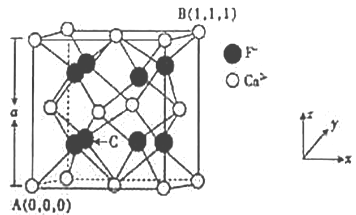
��CaF2�����У�Ca2+����λ��Ϊ_____��F-����λ��Ϊ_____��
��ԭ����������ɱ�ʾ�����ڲ���ԭ�ӵ����λ�ã���֪A��B�����ԭ�����������ͼ��ʾ����C���ԭ���������Ϊ______________��
�۾������������������Ĵ�С����״��CaF2�����ľ���������A=546.2pm�������ܶ�Ϊ_____(�г�����ʽ����)g/cm3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������̶����ܱ������н��п��淴Ӧ2NO2![]() 2NO+O2����������Ϊ��Ӧ�ﵽƽ��״̬��־����( )
2NO+O2����������Ϊ��Ӧ�ﵽƽ��״̬��־����( )
����λʱ��������nmol O2��ͬʱ����2n mol NO2
����λʱ��������n mol O2 ��ͬʱ����2n mol NO
����NO2 ��NO��O2��ʾ�ķ�Ӧ����֮��Ϊ2��2��1
������������ɫ���ٸı� �����������ܶȲ��ٸı�
����������ѹǿ���ٸı� ����������ƽ����Է����������ٸı�
A���٢ܢޢ� B���ڢۢݢ� C���٢ۢܢ� D��ȫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������H3AsO4��Һ�и��������ӷֲ�����(ƽ��ʱ�����ӵ�Ũ�������������Ũ��֮�͵ı�)��pH�Ĺ�ϵ����ͼ��ʾ������˵����ȷ����
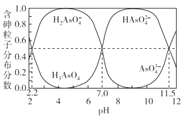
A. H3AsO4�ĵ�һ�����볣��Ka1>0.01
B. pH=7.0ʱ����Һ��c(AsO43-)=c(H3AsO4)=0
C. 0.1mol��L-1H3AsO4��Һ��pH<2
D. pH=12ʱ��c(H+)=3c(AsO43-)+2c(HAsO42-)+c(H2AsO4-)+c(OH-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��������У�ǰ�߸պ��Ǻ�����������
A. 2 molˮ��Ħ��������1 molˮ��Ħ������
B. 200 mL 1 mol��L��1�Ȼ�����Һ��c(Cl��)��100 mL 2 mol��L��1�Ȼ�����Һ��c(Cl��)
C. ��״���£�22.4 Lһ����̼����ԭ������16 g������������ԭ����
D. 2 mol��L��1H2SO4��Һ�е�H��������1 mol��L��1HCl��Һ�е�H������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com