
 为测定镁铝合金(不含其它元素)中铝的质量分数,甲、乙、丙三个学习小组设计了下列三种不同的实验方案进行探究.请回答下列问题:
为测定镁铝合金(不含其它元素)中铝的质量分数,甲、乙、丙三个学习小组设计了下列三种不同的实验方案进行探究.请回答下列问题:| 足量NaOH溶液 |
| 足量盐酸 |
| 足量盐酸 |
| 足量NaOH溶液 |
| 操作1 |
| 1.45g |
| 58g/mol |
| 12-0.6 |
| 12 |


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:
| A、反应①中a的值为5,b的值为8 |
| B、该滴定过程中选择的指示剂是酚酞 |
| C、样品中w(FeSO4?7H2O)=2.78V×100% |
| D、反应②是为了消除Fe3+的棕黄色对终点判断的干扰 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
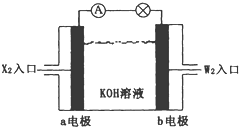 有X、Y、Z、W四种短周期元素,原子序数依次增大.X的阳离子就是一个质子.Z、W在周期表中处于相邻位置,它们的单质在通常状况下均为无色气体.Y原子的最外层电子数是次外层电子数的2倍.请回答:
有X、Y、Z、W四种短周期元素,原子序数依次增大.X的阳离子就是一个质子.Z、W在周期表中处于相邻位置,它们的单质在通常状况下均为无色气体.Y原子的最外层电子数是次外层电子数的2倍.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:

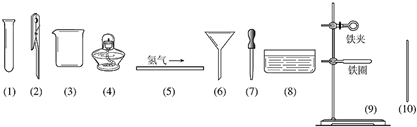
| A、浓硫酸和铜粒 |
| B、浓氨水和氧化钙 |
| C、浓盐酸和浓硫酸 |
| D、水和电石 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、可能三种气体都存在 |
| B、可能只有氢气 |
| C、可能是甲烷和一氧化碳的混合气体 |
| D、可能只有甲烷 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com