
 ��R������
��R������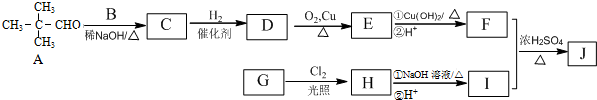
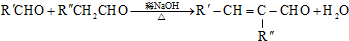
 ��
�� ���� D�����õ�E��E�����õ�F����D�д���-CH2OH�ṹ��E����-CHO��F����-COOH��F��I��Ӧ�õ�J��J�ķ���ʽΪC15H22O4�����J�Ľṹ�ص㣬��֪FΪC6H13COOH��A��B��EΪͬϵ�A�Ľṹ��ʽΪ��CH3��3CCHO�����F�ķ���ʽ��֪BΪCH3CHO����CΪ��CH3��3CCH=CHCHO��DΪ��CH3��3CCH2CH2CH2OH��EΪ��CH3��3CCH2CH2CHO��FΪ��CH3��3CCH2CH2COOH��G���������շ�������������ȡ����Ӧ����H��H����±����ˮ�ⷴӦ�õ�I����֪IΪ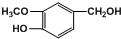 ��GΪ
��GΪ ��HΪ
��HΪ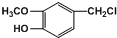 ��JΪ
��JΪ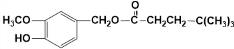 ���ݴ˽��
���ݴ˽��
��� �⣺D�����õ�E��E�����õ�F����D�д���-CH2OH�ṹ��E����-CHO��F����-COOH��F��I��Ӧ�õ�J��J�ķ���ʽΪC15H22O4�����J�Ľṹ�ص㣬��֪FΪC6H13COOH��A��B��EΪͬϵ�A�Ľṹ��ʽΪ��CH3��3CCHO�����F�ķ���ʽ��֪BΪCH3CHO����CΪ��CH3��3CCH=CHCHO��DΪ��CH3��3CCH2CH2CH2OH��EΪ��CH3��3CCH2CH2CHO��FΪ��CH3��3CCH2CH2COOH��G���������շ�������������ȡ����Ӧ����H��H����±����ˮ�ⷴӦ���ữ�õ�I����֪IΪ ��GΪ
��GΪ ��HΪ
��HΪ ��JΪ
��JΪ ��
��
��1��C�Ľṹ��ʽΪ��CH3��3CCH=CHCHO���ʴ�Ϊ����CH3��3CCH=CHCHO��
��2��DΪ��CH3��3CCH2CH2CH2OH��ϵͳ����Ϊ��4��4-����-1-�촼���ʴ�Ϊ��4��4-����-1-�촼��
��3��GΪ ������������Ϊ�Ѽ����ǻ����ʴ�Ϊ���Ѽ����ǻ���
������������Ϊ�Ѽ����ǻ����ʴ�Ϊ���Ѽ����ǻ���
��4��I�Ľṹ��ʽΪ ��
��
A�����ǻ����������Ʒ�Ӧ��1mol I����1mol NaOH��ȫ��Ӧ����A����
B�����ǻ���̼���Ʒ�Ӧ�õ�̼�����ƣ�1mol I����1mol Na2CO3��ȫ��Ӧ����B��ȷ��
C�������Ȼ��������ǻ�������̼�����Ʒ�Ӧ����C����
D�����ǻ������ǻ������Ʒ�Ӧ����������1mol I����Na��Ӧ�õ�1mol����������һ���DZ���£��õ����������һ����22.4L����D����
��ѡ��B��
��5��H��NaOH��Һ��Ӧ�Ļ�ѧ����ʽ�� ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼���л����ƶ���ϳɣ�������÷�Ӧ������J�Ľṹ�ص������ʽ�����ƶϣ���Ҫѧ���������չ����ŵ�������ת�������ؿ���ѧ�����������������Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ҵ��������ʱ��ʹ���Ƚ��������Գ�����÷�Ӧ�����ų������� | |
| B�� | ��ҵ�Ϻϳɰ�û�в��ø����ѹǿ�Ǵ��豸�Ͷ���Ҫ���濼�ǵ� | |
| C�� | ��ҵ�������ӽ���Ĥ����ⱥ��ʳ��ˮ���ռ� | |
| D�� | ��ҵ�ϲ��õ�⣨ʡ����30%����AlCl3-KCl������ķ�����ȡ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ԫ�����ԭ���������ε��� | |
| B�� | Ԫ��ԭ�Ӱ뾶�������Ա仯 | |
| C�� | Ԫ��ԭ�Ӻ�������Ų��������Ա仯 | |
| D�� | Ԫ�ؽ����Ի�ǽ����Գ������Ա仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����̼Ԫ����ɵ�����һ���Ǵ����� | |
| B�� | ���ʯ��ʯī������ϩ��C60����Ϊͬ�������� | |
| C�� | ͬ��������֮���ת�����������仯 | |
| D�� | ���ʯ��ʯī��������ȫ��ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ����������ѧ��Ӧԭ��֪ʶ����������⣺
����������ѧ��Ӧԭ��֪ʶ����������⣺| �� | ���뷽��ʽ | ����ƽ�ⳣ��K |
| CH3COOH | CH3COOH?CH3COO-+H+ | 1.96��10-5 |
| HClO | HClO?ClO-+H+ | 3.0��10-8 |
| H2CO3 | H2CO3?H++HCO3- HCO3-?H++CO32- | K1=4.4��10-7 K2=5.6��10-11 |
| H3PO4 | H3PO4?H++H2PO4- H2PO4-?H++HPO42- HPO42-?H++PO43- | K1=7.1��10-3 K2=6.3��10-8 K3=4.2��10-13 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ������ϩ�⣬����Ҫ�������ֵ��壬д�������ֵ���Ľṹ��ʽCH2=CH-CN��CH2=CH-CH=CH2��
������ϩ�⣬����Ҫ�������ֵ��壬д�������ֵ���Ľṹ��ʽCH2=CH-CN��CH2=CH-CH=CH2��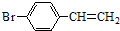 ����Ҫ��������һ��ѡ�õ��Լ�ΪHBr��Ŀ���DZ���̼̼˫����ֹ���ӳɣ�
����Ҫ��������һ��ѡ�õ��Լ�ΪHBr��Ŀ���DZ���̼̼˫����ֹ���ӳɣ� ��
��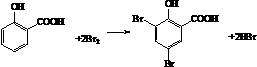 ��
��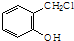 �Ʊ�A�ĺϳ�·��
�Ʊ�A�ĺϳ�·���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
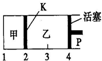 һ���¶��¿��淴ӦA��s��+2B��g��?2C��g��+D��g����H��0���ֽ�1molA��2molB����������У���4molC��2molD�����������У���ʱ���ƻ���P��ʹ�ҵ��ݻ�Ϊ��2����t1ʱ�������ھ��ﵽƽ��״̬����ͼ��ʾ������K�����ƶ���������˵����ȷ���ǣ�������
һ���¶��¿��淴ӦA��s��+2B��g��?2C��g��+D��g����H��0���ֽ�1molA��2molB����������У���4molC��2molD�����������У���ʱ���ƻ���P��ʹ�ҵ��ݻ�Ϊ��2����t1ʱ�������ھ��ﵽƽ��״̬����ͼ��ʾ������K�����ƶ���������˵����ȷ���ǣ�������| A�� | �����¶Ⱥͻ���λ�ò��䣬�ڼ����ټ���1mol A��2mol B���ﵽ�µ�ƽ�����C��Ũ��������C��Ũ�ȵ�2�� | |
| B�� | �����¶Ⱥ����е�ѹǿ���䣬�ֱ���ס����м���������ĺ�������ƽ�ⲻ�ƶ�������ƽ��������Ӧ�����ƶ� | |
| C�� | ���ֻ���λ�ò��䣬�����¶ȣ��ﵽ�µ�ƽ��ס�����B�������������С | |
| D�� | �����¶Ȳ��䣬�ƶ�����P��ʹ�ҵ��ݻ��ͼ���ȣ��ﵽ�µ�ƽ�������C����������Ǽ���C�����������2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  п�̸ɵ�� | B�� |  Ǧ���� | C�� |  ��ȼ�ϵ�� | D�� |  ���ӵ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ڶ���ӵ�ԭ��������ߵĵ���ͨ��˳��˽����������˶� | |
| B�� | ����������������������͵ĵ��Ӳ��ϣ�����ֻ��������K������L�� | |
| C�� | ������������������Ų���ȫ��ͬ�����仯ѧ����һ����ͬ | |
| D�� | ���������ֻ����8�����Ӳ��ȶ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com