
 ���ݻ�Ϊ100L���ܱ������У�����1.0molCH4��2.0molH2O��g����һ�������·�����Ӧ��CH4��g��+H2O��g��?CO��g��+3H2��g����H
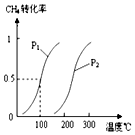
���ݻ�Ϊ100L���ܱ������У�����1.0molCH4��2.0molH2O��g����һ�������·�����Ӧ��CH4��g��+H2O��g��?CO��g��+3H2��g����H���� ��1����ͼ��֪��100��ʱCH4��ת����Ϊ0.5����
CH4��g��+H2O��g��?CO��g��+3H2��g��
��ʼ 1 2 0 0
ת�� 0.5 0.5 0.5 1.5
ƽ�� 0.5 1.5 0.5 1.5
KΪ������Ũ����֮���뷴Ӧ��Ũ����֮���ıȣ�
��2��ͼ���¶���ͬʱ��p1��Ӧ��ת���ʴ÷�ӦΪ�����������ķ�Ӧ������ѹǿƽ�������ƶ���
��3��ͼ��ѹǿ��ͬʱ���¶�Խ�ߣ�ת����Խ��
��� �⣺��1����ͼ��֪��100��ʱCH4��ת����Ϊ0.5����
CH4��g��+H2O��g��?CO��g��+3H2��g��
��ʼ 1 2 0 0
ת�� 0.5 0.5 0.5 1.5
ƽ�� 0.5 1.5 0.5 1.5
K=$\frac{��\frac{0.5}{100}mol/L������\frac{1.5}{100}mol��^{3}}{��\frac{0.5}{100}mol/L����\frac{1.5}{100}mol/L��}$=2.25��10-4 mol2•L-2��
�ʴ�Ϊ��2.25��10-4 mol2•L-2��
��2��ͼ���¶���ͬʱ��p1��Ӧ��ת���ʴ��ɷ�ӦΪ�����������ķ�Ӧ��ѹǿԽСת����Խ�ߣ���p1��p2��
�ʴ�Ϊ��������ͬ�¶�ʱp1��CH4��ת���ʴ���p2��CH4��ת���ʣ��ɷ�ӦΪ�����������ķ�Ӧ��ѹǿԽСת����Խ�ߣ�
��3��ͼ��ѹǿ��ͬʱ���¶�Խ�ߣ�ת����Խ����ÿ��淴Ӧ�ġ�H��0���¶�Խ�ߣ�KԽ����K1��K2��
�ʴ�Ϊ��������ͼ���֪���ÿ��淴Ӧ�ġ�H��0���¶����ߣ�ƽ�������ƶ���
���� ���⿼�黯ѧƽ��ļ��㣬Ϊ��Ƶ���㣬����ƽ�����η���K�ļ��㼰ƽ���ƶ�Ϊ���Ĺؼ������ط�������������Ŀ��飬ע��ͼ���¶ȡ�ѹǿ��ƽ���ƶ���Ӱ�죬��Ŀ�ѶȲ���


 ��ְٷְټ�����Ԫ��ĩ���Ծ�ϵ�д�
��ְٷְټ�����Ԫ��ĩ���Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ca2+��Na+��NO3-��Cl- | B�� | K+��Ba2+��Cl-��NO3- | ||
| C�� | Na+��HCO3-��CO32-��K+ | D�� | Na+��Cl-��K+��MnO4- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | A3BC4 | B�� | A2BC4 | C�� | A2BC3 | D�� | A4BC4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���������Ȼ�̼����ˮ | |
| B�� | �����������ϩ�����Ը��������Һ | |
| C�� | ���� ��CH��CH����ˮ ��CH��CH����ˮ | |
| D�� | ����NaCl��CH3CH2Cl����������Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
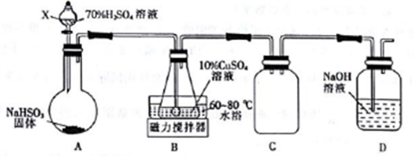
| ʵ����� | Ԥ�������� |
| ȡ������Ӧ��Ļ����Һ���Թ� A�У��μ�ϡ���� | �������ݲ��������II���I����II����III������ͬ����������û�����ݲ��������I��III���� |
| ��ȡ������Ӧ��Ļ����Һ���Թ�B�У��μӼ��ε���KI��Һ������� | ����Һ��Ϊ��ɫ����III���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2SO4��Һ��Ba��OH��2��Һ��� | B�� | NH3•H2O��Һ��HCl��Һ��� | ||
| C�� | NaHCO3��Һ��NaOH��Һ��� | D�� | HNO3��Һ��KOH��Һ��� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com