
| A. | 所得溶液中氯化钠的浓度为1 mol/L | |
| B. | 向所得的溶液中通入二氧化碳,可使溶液具备漂白性 | |
| C. | 所得溶液中有大量的单质的氯元素存在 | |
| D. | 在反应中氯元素化合价降低,钠元素化合价升高 |
分析 A.氯气与氢氧化钠反应生成氯化钠、次氯酸钠和水,溶液体积未知;
B.碳酸酸性强于次氯酸;
C.氯气与氢氧化钠反应生成氯化钠、次氯酸钠和水;
D.氯气与氢氧化钠反应为歧化反应.
解答 解:A.1mol氯气通入足量的氢氧化钠溶液生成氯化钠小于1mol,且溶液体积未知,无法计算氯化钠的物质的量浓度,故A错误;
B.碳酸酸性强于次氯酸,二氧化碳与次氯酸钠溶液反应生成次氯酸,次氯酸具有漂白性,故B正确;
C.氯气与氢氧化钠反应生成氯化钠、次氯酸钠和水,氯元素以化合态存在,故C错误;
D.氯气与氢氧化钠反应为歧化反应,反应中氧化剂、还原剂都是氯气,钠元素化合价不变,故D错误;
故选:B.
点评 本题考查了元素化合物性质,熟悉氯气的性质及氯气与氢氧化钠反应的实质是解题关键,题目难度中等,注意依据化合价变化判断元素在反应中表现的性质.


科目:高中化学 来源: 题型:选择题
| A. | 实验中要配制490mL 0.2mol/L KCl溶液,需要托盘天平称量7.3g KCl固体 | |
| B. | 室温下,浓度均为0.1mol/L Na2S2O3和H2SO4溶液,分别取6mL与10mL混合、10mL与10mL混合,可验证Na2S2O3浓度对反应速率的影响 | |
| C. | 往盛有少量淀粉溶液的试管中加入一定量稀硫酸,加热3~4分钟后,再加入NaOH溶液至碱性,最后加入银氨溶液并水浴加热,有银镜产生 | |
| D. | 在中和热的测定实验中,将KOH溶液迅速倒入装有盐酸的量热计中,立即读出并记录溶液的起始温度,充分反应后再读出并记录反应体系的最高温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2L的水中含有0.5NA个水分子 | |
| B. | 含有1molHCl的盐酸中离子总数为NA个 | |
| C. | 1molO2和H2的混合气体中含有NA个分子 | |
| D. | 1mol大米中含有NA个大米粒子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
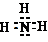 ;C气体的化学式是SO2.
;C气体的化学式是SO2.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 15种 | B. | 16种 | C. | 17种 | D. | 18种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶解度:MgCO3>Mg(OH)2 | B. | 金属性:Mg<K | ||
| C. | 还原性:H2S<SiH4 | D. | 稳定性:HF>PH3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com