
分析 (1)根据n=$\frac{m}{M}$=$\frac{N}{N{\;}_{A}}$=$\frac{V}{Vm}$计算该题相关物理量;
(2)中学常见能与酸、碱反应的物质有:Al、两性氧化物、两性氢氧化物、弱酸的酸式盐、弱酸的铵盐、氨基酸、蛋白质等,结合物质的性质解答;
(3)与足量的硫酸溶液反应,当生成气体的质量相同时,金属完全反应,H得到电子数相同,可知金属失去电子数相同,以此来解答;
(4)将氯化铝溶液和氢氧化钠溶液等体积混合,得到的沉淀物中含铝元素的质量与溶液中含铝元素的质量的2倍,沉淀为Al(OH)3,溶液中的铝可能为AlCl3或NaAlO2,可分别发生:Al3++3OH-═Al(OH)3↓、Al(OH)3+OH-=AlO2-+2H2O,结合反应的离子方程式分为两种情况讨论计算;
(5)碳酸氢钠不稳定,加热易分解,发生反应:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,2Na2O2+2CO2=2Na2CO3+O2,2Na2O2+2H2O=4NaOH+O2,由于二氧化碳与氢氧化钠反应生成碳酸钠,可以认为过氧化钠先与二氧化碳反应,再与水反应.
解答 解:(1)由n=$\frac{m}{M}$=$\frac{V}{Vm}$可知,相同质量时,气体的摩尔质量越大,物质的量越小,在相同温度和相同压强条件下,气体的体积越小,反之越大,则体积最大的是H2;
故答案为:H2;
(2)①NaAlO2 不能与氢氧化钠反应,故错误;
②Ca(OH)2 不能与氢氧化钠反应,故错误;
③Na2CO3 不能与氢氧化钠反应,故错误;
④Al(OH)3为两性物质,能够与盐酸反应生成氯化铝和水,与氢氧化钠反应生成偏铝酸钠和水,故正确;
⑤NaHCO3与盐酸反应生成氯化钠、二氧化碳和水,与氢氧化钠反应生成碳酸钠和水,故正确;
故答案为:④⑤;
(3)与足量的硫酸溶液反应,当生成气体的质量相同时,金属完全反应,H得到电子数相同,可知金属失去电子数相同,
设Na、Mg、Al的物质的量分别为x、y、z,则
x×(1-0)=y×(2-0)=z×(3-0),
解得x:y:z=6:3:2,
故答案为:6:3:2;
(4)设AlCl3和NaOH的浓度分别为c1和c2,相同体积为V,
若NaOH过量,生成NaAlO2,此时参加反应的AlCl3的物质的量是c1Vmol,NaOH是3c1Vmol,生成c1V mol 的Al(OH)3,
又因为得到的沉淀物中铝元素的质量和溶液中铝元素的质量相等,则说明第一步反应完后,生成的Al(OH)3有$\frac{1}{3}$(c1V)发生Al(OH)3+OH-=AlO2-+2H2O,
所以可求的NaOH的物质的量为:3c1V+$\frac{1}{3}$c1V=c2V,所以c1:c2=3:10;
当氯化铝过量时,氢氧化钠不足,生成氢氧化铝白色沉淀发生反应:Al3++3OH-═Al(OH)3↓,设反应掉的铝离子物质的量为x,得到的沉淀物中铝元素的质量是溶液中铝元素的质量2倍,则2(c1V-x)=x,解得x=$\frac{2}{3}$c1V,消耗氢氧化钠物质量为c2V,即3×$\frac{2}{3}$c1V=c2V,解得c1:c2=1:2;
故答案为:1:2或3:10;
(5)由方程式:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,可知2mol NaHCO3分解得到Na2CO3、CO2和H2O各1mol,
还会发生反应:2Na2O2+2CO2=2Na2CO3+O2,2Na2O2+2H2O=4NaOH+O2,由于二氧化碳与氢氧化钠反应生成碳酸钠,可以认为过氧化钠先与二氧化碳反应,再与水反应,Na2O2只有1mol,恰好和CO2反应生成1molNa2CO3和O2,气体排出后,只剩余Na2CO3,
故答案为:Na2CO3.
点评 本题考查了物质量有关计算、离子反应的计算,题目难度中等,明确发生反应的实质为解答关键,注意掌握讨论法在化学计算中的应用,试题培养了学生的分析能力及化学计算能力.


科目:高中化学 来源: 题型:解答题
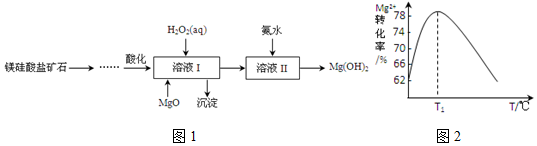
 .溶液 I中加入H2O2溶液发生反应的离子方程式是2Fe2++H2O2+2H+=2Fe3++2H2O.
.溶液 I中加入H2O2溶液发生反应的离子方程式是2Fe2++H2O2+2H+=2Fe3++2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 与等体积pH=11的NaOH溶液混合后所得溶液显酸性 | |
| B. | c(H+)=c(CH3COO-)+c(OH-) | |
| C. | 该溶液中由水电离出的c(H+)是1.0×10-11 mol/L | |
| D. | 加入少量CH3COONa固体后,c(CH3COO-)降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验现象 | 结论 |
| A. | 含0.5 mol HCl的稀溶液与含 0.55 mol NaOH的稀溶液混合 | 测得放出热量为a kJ | 强酸与强碱反应的中和热为2a kJ/mol |
| B. | 向CuCl2、MgCl2的混合溶液中滴加NaOH溶液 | 先出现蓝色沉淀 | Ksp[Mg(OH)2]>Ksp[Cu(OH)2] |
| C. | 将铁钉和铜丝用导线连接后放入滴有酚酞的氯化铵溶液中 | 铜丝附近溶液变红色 | 铁发生吸氧腐蚀 |
| D. | 向某未知溶液中滴加酸性KMnO4溶液 | KMnO4溶液褪色 | 溶液中有Fe2+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳 | B. | 钠 | C. | 硫 | D. | 铁 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
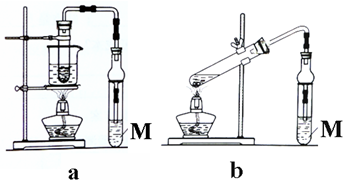
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100mL 1mol/LAlCl3溶液 | B. | 200 mL 1mol/LMgCl2溶液 | ||
| C. | 100mL 0.5mol/LCaCl2溶液 | D. | 100 mL 2 mol/L KCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 水电离的[H+]随着温度的升高而降低 | B. | 在35℃时,水电离的[H+]>[OH-] | ||
| C. | 水的电离程度:35℃>25℃ | D. | 水电离的[OH-]随温度升高而增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com