
现有一份由C、Al、Fe、Fe2O3、CuO中的几种物质组成的混合物粉末,某校化学课外小组取样品进行了如下实验(其中部分产物已略去):
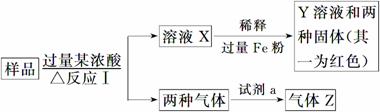
(1)取少量溶液X,加入过量的NaOH溶液,有沉淀生成。取上层清液,通入CO2,无明显变化,说明样品中不含有的物质是(填写化学式)________________。
(2)Z为一种或两种气体:
①若Z只为一种气体,试剂a为饱和NaHCO3溶液,则反应Ⅰ中能同时生成两种气体的化学方程式为______________________
②若Z为两种气体的混合物,试剂a为适量H2O,则Z中两种气体的化学式是__________。
(3)向Y中通入过量Cl2,并不断搅拌,充分反应后,溶液中的阳离子是(填写离子符号)__________。
答案 (1)Al
(2)①C+2H2SO4(浓)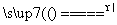 CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O
②NO、CO2
(3)Cu2+、Fe3+、H+
解析 (1)样品与浓酸反应产生两种气体,经分析知浓酸为浓硫酸或浓硝酸,但不管是哪种浓酸,溶液X中都可能含有Fe3+、 Cu2+及Al3+;当加入过量的NaOH溶液后,Fe3+和Cu2+转化为Fe(OH)3和Cu(OH)2沉淀而析出,Al3+转化为[Al(OH)4]-。取上层清液通入CO2后,[Al(OH)4]-与CO2反应能产生白色沉淀Al(OH)3,这与“取上层清液,通入CO2,无明显变化”不相符,所以样品中肯定没有Al。(2)浓酸若为浓硫酸,其与样品中的C反应生成CO2和SO2,通入NaHCO3溶液后SO2被吸收,剩余CO2;浓酸若为浓硝酸,其与样品中的C反应生成CO2和NO2,通入水中后NO2转变为NO。(3)X溶液中加过量Fe粉,得Y溶液和两种固体(其中一种固体为红色的Cu,另一种为过量的Fe粉),这个过程发生了置换反应:Cu2++Fe===Cu+Fe2+;再向Y溶液中通入过量Cl2,则会发生反应:Cl2+2Fe2+===2Cl-+2Fe3+、2Fe3++Cu===2Fe2++Cu2+、Cl2+H2OHCl+HClO。所以充分反应后,溶液中的阳离子为Cu2+、Fe3+、H+。
Cu2+及Al3+;当加入过量的NaOH溶液后,Fe3+和Cu2+转化为Fe(OH)3和Cu(OH)2沉淀而析出,Al3+转化为[Al(OH)4]-。取上层清液通入CO2后,[Al(OH)4]-与CO2反应能产生白色沉淀Al(OH)3,这与“取上层清液,通入CO2,无明显变化”不相符,所以样品中肯定没有Al。(2)浓酸若为浓硫酸,其与样品中的C反应生成CO2和SO2,通入NaHCO3溶液后SO2被吸收,剩余CO2;浓酸若为浓硝酸,其与样品中的C反应生成CO2和NO2,通入水中后NO2转变为NO。(3)X溶液中加过量Fe粉,得Y溶液和两种固体(其中一种固体为红色的Cu,另一种为过量的Fe粉),这个过程发生了置换反应:Cu2++Fe===Cu+Fe2+;再向Y溶液中通入过量Cl2,则会发生反应:Cl2+2Fe2+===2Cl-+2Fe3+、2Fe3++Cu===2Fe2++Cu2+、Cl2+H2OHCl+HClO。所以充分反应后,溶液中的阳离子为Cu2+、Fe3+、H+。


科目:高中化学 来源: 题型:
按要求写出下列反应的离子方程式:
(1)在NH4Cl溶液中加入NaOH溶液,并加热
________________________________________________________________________。
(2)在NH4Cl溶液中滴加NaOH溶液
________________________________________________________________________。
(3)NH4Cl溶液呈酸性的原因
_____________________ ___________________________________________________。
___________________________________________________。
(4)在饱和NH4Cl溶液中滴加Na[Al(OH)4],产生刺激性气味的气体和白色沉淀
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
1.52 g铜镁合金完全溶解于50 mL密度为1.40 g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120 mL(标准状况)。向反应后的溶液中加入1.0 mol/L NaOH溶液,当金属离子全部沉淀时,得到2.54 g沉淀。下列说法不正确的是( )
A.该合金中铜与镁的物质的量之比是21
B.该浓硝酸中HNO3的物质的量浓度是14.0 mol/L
C.得到2.54 g沉淀时,加入NaOH溶液的体积是600 mL
D.NO2和N2O4的混合气体中,NO2的体积分数是80%
查看答案和解析>>
科目:高中化学 来源: 题型:
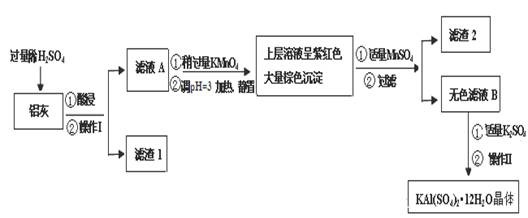 明矾[KAl(SO4)2·12H2O] 在生产、生活中有广泛用途:饮用水的净化;造纸工业上作施胶剂;食品工业的发酵剂等。利用炼铝厂的废料——铝灰(含Al 、 Al2O3及少量SiO2和FeO ·xFe2O3)可制备明矾。工艺流程如下:
明矾[KAl(SO4)2·12H2O] 在生产、生活中有广泛用途:饮用水的净化;造纸工业上作施胶剂;食品工业的发酵剂等。利用炼铝厂的废料——铝灰(含Al 、 Al2O3及少量SiO2和FeO ·xFe2O3)可制备明矾。工艺流程如下:
回答下列问题:
(1)明矾净水的原理是(用离子方程表示)
(2)操作Ⅰ是 ,操作Ⅱ是蒸发浓缩、 、过滤、 干燥。
(3)检验滤液A中是否存在Fe2+的方法是 (只用一种试剂)
(4)在滤液A中加入高锰酸钾的目的是 ,发生反应的离子方程式为(该条件下Fe2+ 转化为Fe3+,MnO4- 转化为Mn2+) 。
已知:生成氢氧化物沉淀的pH如下表所示
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
注:金属离子的起始浓度为0.1 mol·L-1
根据表中数据解释调pH=3的目的 。
(5)己知:在pH=3、加热条件下,MnO4- 可与Mn2+反应生成MnO2。加入MnS04发生反应的离子方程式为: 。滤渣2含有的物质是 。
(6)以Al和NiO(OH)为电极,KOH溶液为电解液可组成新型、高效电池,充放电过程中,发生Ni(OH)2与NiO(OH)之间的转化,写出放电时电池反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室中有6瓶失去标签的白色固体:纯碱、氢氧化镁、氯化钡、硫酸铝、硫酸氢钠、氯化钾。除蒸馏水、试管和胶头滴管外,无其他任何试剂和仪器。某学生通过以下实验步骤即可鉴别它们。请填写下列空白:
(1)各取适量固体于6支试管中,分别加入适量蒸馏水,有一支试管中的现象和其他5支明显不同,此试管中的现象是
________________________________________________________________________,
据此现象鉴别出的一种物质是__________。
(2)分别将所剩5种溶液依次编号为A、B、C、D、E,然后进行两两混合。观察到C没有出现任何现象;D分别和A、B、E混合时均产生了白色沉淀;B和E混合时既有白色沉淀产生,又有无色气体放出。据此可推断出:
①A、C、D三种物质的化学式依次是________________________________________。
②B、E两者中有一种可与A反应,它与足量A反应的离子方程式为________________________________________________________________________。
③在两两混合时,能最终确定B、E成分的实验现象及结论是_____________________
___________________________________________________。
(3)上述物质溶于水抑制水的电离,且溶液显酸性的物质的化学式为________,其溶液显酸性的原因是___________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
判断正误,正确的划“√”,错误的划“×”
(1)在标准状况下,1 mol O2与1 mol SO3的体积相同 ( )
(2)在标准状况下,1 mol气体的体积约是22.4 L,在非标准状况下,1 mol气体的体积则一定不是22.4 L ( )
(3)在相同条件下,相同物质的量的CO、N2的混合气体与O2的分子个数相同,原子个数也相同 ( )
(4)若把(3)中的O2改成氩气,判断结果是 ( )
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值,下列说法正确的是 ( )
A.46 g NO2和N2O4混合气体中含有的分子总数为NA
B.用含4 mol HCl的浓盐酸跟足量二氧化锰反应生成的氯气在标准状况下的体积为
22.4 L
C.0.1 mol金属钠与氧气在一定条件下完全反应,生成钠的氧化物的混合物时,失去的电子数为0.1NA
D.1 mol苯中含有3NA个碳碳双键
查看答案和解析>>
科目:高中化学 来源: 题型:
纯碱、烧碱等是重要的化工原料。
(1)利用右下图所示装置可间接证明二氧化碳与烧碱溶液发生了反应:将A与B连接,打开止水夹,将胶头滴管中的液体挤入烧瓶,此时的实验现象是 ,反应的离子方程式是______ _。
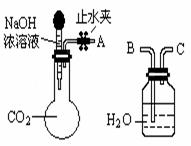 (2)向100 mL2 mol/L的NaOH 溶液中通入一定量CO2,充分反应后将溶液在一定条件下蒸发结晶,得到少量的白色固体。试设计实验确认该白色固体的成分。
(2)向100 mL2 mol/L的NaOH 溶液中通入一定量CO2,充分反应后将溶液在一定条件下蒸发结晶,得到少量的白色固体。试设计实验确认该白色固体的成分。
①提出合理假设。
假设1:该白色固体为NaOH和Na2CO3;
假设2:该白色固体为只有Na2CO3;
假设3:该白色固体为只有NaHCO3;
假设4:该白色固体为Na2CO3 和NaHCO3
②基于假设4,设计实验方案进行实验证明固体的成分是NaOH和Na2CO3。请在答题卡上写出实验步骤及预期现象和结论。(步骤可不填满也可增加)
限选实验试剂及仪器: 1moL·L–1HCl溶液、1mol·L–1 MgCl2溶液、0.5moL·L–1BaCl2溶液、1mol·L–1 Ba(OH)2溶液、甲基橙试液、酚酞试液、试管、胶头滴管、过滤装置。
| 实验步骤 | 预期现象和结论 |
| 步骤1: | |
| 步骤2: |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com