
| A. | 元素b、c在同一周期 | |
| B. | 元素a、b、d各自最高和最低化合价的代数和均为0 | |
| C. | b的最高价氧化物对应的水化物酸性比d的弱 | |
| D. | 元素a、b、c不能存在于同一离子化合物中 |
分析 原子序数依次增大的短周期主族元素a、b、c、d,它们的最外层电子数分别为1、4、1、4,则a、c处于IA族,b、d处于IVA族,可推知b为C、d为Si,结合原子序数可知c为Na,a-的L层电子的电子数为0,则a为H,据此解答.
解答 解:原子序数依次增大的短周期主族元素a、b、c、d,它们的最外层电子数分别为1、4、1、4,则a、c处于IA族,b、d处于IVA族,可推知b为C、d为Si,结合原子序数可知c为Na,a-的L层电子的电子数为0,则a为H.
A.b为C,处于第二周期,c为Na,处于第三周期,故A错误;
B.H元素最高正化合价为+1、最低化合价为-1,C元素最高正化合价为+4、最低价化合价为-4,Si元素最高正化合价为+4、最低价化合价为-4,最高和最低化合价的代数和均为0,故B正确;
C.非金属性C>Si,故最高价氧化物对应水化物酸性:碳酸>硅酸,故C错误;
D.H、C、Na可以存在于NaHCO3等离子化合物中,故D错误,
故选:B.
点评 本题考查结构性质位置关系应用,推断元素是解题关键,侧重对元素周期律的考查,注意氢负离子为中学盲点,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | NaBH4中B元素化合价为+3 | B. | 每生成11.2 L氏转移Na个电子 | ||
| C. | NaBH4在反应中作氧化剂 | D. | NH3BH3在反应中属于还原产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤⑥ | B. | ③④⑤⑥⑧② | C. | ⑧①⑤⑥⑦③ | D. | ⑧⑨⑤⑥②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石灰石与盐酸反应:CO32-+2H+═H2O+CO2↑ | |
| B. | 石灰乳与Na2CO3溶液混合:Ca(OH)2+CO32-═CaCO3↓+2OH- | |
| C. | 铁与稀硫酸:2Fe+6H+═2Fe3++3 H2↑ | |
| D. | 氢氧化钡溶液与稀硫酸反应:Ba2++SO42-+H++OH-═BaSO4↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
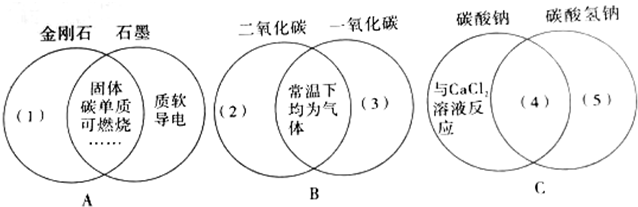
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ; (2)铝离子的结构示意图:
; (2)铝离子的结构示意图: ;
;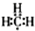
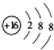 ; (6)NH4Cl的电子式:
; (6)NH4Cl的电子式: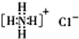 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 车辆排放的氮氧化物、煤燃烧产生的二氧化硫是导致雾霾天气的“罪魁祸首”.活性炭可处理大气污染物NO.在5L密闭容器中加入NO和活性炭(假设无杂质),一定条件下生成气体E和F.当温度分别在T1和T2时,测得各物质平衡时物质的量(n/mol)如表:
车辆排放的氮氧化物、煤燃烧产生的二氧化硫是导致雾霾天气的“罪魁祸首”.活性炭可处理大气污染物NO.在5L密闭容器中加入NO和活性炭(假设无杂质),一定条件下生成气体E和F.当温度分别在T1和T2时,测得各物质平衡时物质的量(n/mol)如表:| 物质 T/℃ | 活性炭 | NO | E | F |
| 初始 | 3.000 | 0.10 | 0 | 0 |
| T1 | 2.960 | 0.020 | 0.040 | 0.040 |
| T2 | 2.975 | 0.050 | 0.025 | 0.025 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (1)区分晶体和非晶体常用方法为X-射线衍射实验.
(1)区分晶体和非晶体常用方法为X-射线衍射实验.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用食醋除去水壶中的水垢 | B. | 氯气泄漏后应顺风向低处跑 | ||
| C. | 用铝锅炒菜比用铁锅好 | D. | 食用“加碘”食盐不利于健康 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com