
| A、向某物质中滴加盐酸后,有能使澄清石灰水变浑浊的无色无味气体产生,证明含CO32- |
| B、向某溶液中滴加氯化钡溶液,产生白色沉淀,再滴加足量稀硝酸,依然有白色固体,说明原溶液含有SO42- |
| C、向某溶液中逐渐滴加NaOH溶液,先有白色胶状沉淀产生,后来沉淀逐渐溶解,则原溶液中可能含有Al3+ |
| D、向某溶液中先加入氯水,再滴入KSCN溶液,最后溶液显血红色,则原溶液中一定含有Fe3+ |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| 3 |
| 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠与水反应:Na+2H2O=Na++2OH-+H2↑ |
| B、小苏打与醋酸反应:HCO3-+H+═CO2↑+H2O |
| C、氯气与水反应:Cl2+H2O?2H++Cl-+ClO- |
| D、氯化铝溶液与过量氨水反应:3NH3?H2O+Al3+=Al(OH)3↓+3NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,22.4L水含有的分子数为NA |
| B、2NA个N2分子和2mol N2的质量都是28g |
| C、通常状况下,44g CO2气体所含氧原子数NA |
| D、1mol NO2中原子总数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用HNO3溶液完全中和后,溶液不显中性 |
| B、加水稀释后,溶液中c(NH4+)?c(OH-)变大 |
| C、与AlCl3溶液发生反应的离子方程式为 Al3++3OH-=Al(OH)3↓ |
| D、其溶液的pH=13 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol?L-1甲酸溶液的pH值约为2 |
| B、甲酸电离出的阳离子全部是H+ |
| C、10mL 1mol?L-1甲酸与10mL 1mol?L-1 NaOH溶液完全反应后,溶液呈碱性 |
| D、1L H+浓度为0.1mol?L-1的甲酸和足量Zn反应放出的H2在标况下远大于1.12L |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、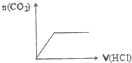 在碳酸氢钠溶液中逐滴加入稀盐酸 |
B、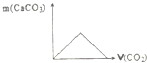 向澄清石灰水中逐渐通入二氧化碳气体 |
C、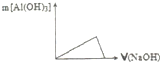 向氧化铝溶液中逐滴加入氢氧化钠溶液 |
D、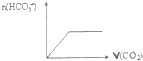 向偏铝酸钠溶液中逐渐通入二氧化碳气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 五种短周期元素的部分性质数据如下:
五种短周期元素的部分性质数据如下:| 元素 | T | X | Y | Z | W |
| 原子半径(nm) | 0.037 | 0.075 | 0.099 | 0.102 | 0.143 |
| 最高或最低化合价 | +1 | +5 -3 |
+7 -1 |
+6 -2 |
+3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com