
【题目】Fe3+与SCN-形成的配离子颜色极似血液,常被用于电影特技和魔术表演。回答下列问题:
(1)画出Fe3+的外围电子排布图:___________;SCN-的结构式为________,SCN-中σ键与π键数目之比为________。
(2)基态硫原子中,核外占据最高能级电子的电子云轮廓图形状为_________。硫的一种同素异形体分子式为S8,其结构如右图所示,其中S原子的杂化轨道类型为______。S8易溶于二硫化碳的原因是___________。
![]()
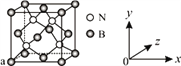
(3)N与B可形成化合物立方氮化硼,其结构与金刚石相似,是超硬材料,立方氮化硼属于________晶体。已知立方氮化硼晶体内存在配位键,则其晶体中配位键与普通共价键数目之比为______。原子坐标参数可表示晶胞内部各原子的相对位置,图中a处B的原子坐标参数为(0, 0, 0),则距离该B原子最近的N原子坐标参数为_________。
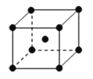
(4)单质铁的晶体结构如右图所示,该堆积方式名称为________。已知该晶胞的密度为ρg/cm3,则铁原子半径的计算式为_________ pm。
(5)磺酰氯(SO2Cl2)和亚硫酰氯(SOCl2)是两种重要试剂。磺酰氯可看成是硫酸分子中2个羟基被氯原子取代后的衍生物,主要用于有机合成;亚硫酰氯可与水剧烈反应,常用于与一些易水解的无机氯化物(MgCl2·6H2O)作用制取无水金属氯化物(MgCl2)。
已知:SO2(g)+Cl2(g)+SCl2(g)![]() 2SOCl2(g) ……(Ⅰ)
2SOCl2(g) ……(Ⅰ)
SO2(g)+Cl2(g)![]() SO2Cl2(g) ………………(Ⅱ)
SO2Cl2(g) ………………(Ⅱ)
回答下列问题:
(a)SO2Cl2的空间构型为_______________。
(b)反应Ⅰ、Ⅱ的化学平衡常数分别为K1、K2,则:SO2Cl2(g)+SCl2(g)![]() 2SOCl2(g)的平衡常数K=_______。
2SOCl2(g)的平衡常数K=_______。
(c)在50L恒容密闭容器中充入1.0molSO2和1.0molCl2发生反应Ⅱ,测得SO2的转化率随时间变化关系如右图所示。

①反应Ⅱ属于________反应(填“放热”“ 吸热”)。在T1温度下,从反应开始至刚好达到平衡时的平均反应速率v(SO2)=___________。为了提高SO2的平衡转化率,除改变温度外,还可以采取的一条措施是__________。
②在T2温度下反应,起始压强为101kPa,则平衡时气体的压强p平=__________kPa。气体分压(p分)=气体总压(p总)×体积分数,用某物质的平衡分压代替物质的量浓度也可以表示化学平衡常数(记作Kp),T2温度下,该反应的化学平衡常数Kp=______________。
(d)无水AlCl3在有机合成中应用广泛。蒸干AlCl3溶液不能得到无水AlCl3,用化学方程式表示其原因:______________。工业上常用SOCl2与AlCl3·6H2O混合并加热制备无水AlCl3,原因是__________________。
【答案】 ![]() [S-C≡N]-或[S=C=N]- 1:1 哑铃形 sp3 S8和二硫化碳都是非极性分子,根据相似相溶原理S8易溶于二硫化碳 原子 1:3 (4) (,,) 体心立方堆积
[S-C≡N]-或[S=C=N]- 1:1 哑铃形 sp3 S8和二硫化碳都是非极性分子,根据相似相溶原理S8易溶于二硫化碳 原子 1:3 (4) (,,) 体心立方堆积 ![]() ×
×![]() ×1010 四面体
×1010 四面体 ![]() 放热 3.2×10-3mol/(L·min) 充入氯气、分离产物等 70.7 0.0743(kPa)-1或
放热 3.2×10-3mol/(L·min) 充入氯气、分离产物等 70.7 0.0743(kPa)-1或![]() (kPa)-1
(kPa)-1 ![]() (kPa)-1 AlCl3+3H2O
(kPa)-1 AlCl3+3H2O![]() Al(OH)3+3HCl↑ SOCl2与结晶水反应产生的HCl抑制了AlCl3水解
Al(OH)3+3HCl↑ SOCl2与结晶水反应产生的HCl抑制了AlCl3水解
【解析】(1)铁原子的核电荷数为26,外围电子排布图为3d64s2,Fe3+的外围电子排布图:![]() ;SCN-的结构式为[S-C≡N]-或[S=C=N]-;根据其结构可知:σ键数目为2,π键数为2,数目之比为1:1;正确答案:
;SCN-的结构式为[S-C≡N]-或[S=C=N]-;根据其结构可知:σ键数目为2,π键数为2,数目之比为1:1;正确答案: ![]() ; [S-C≡N]-或[S=C=N]- ; 1:1。
; [S-C≡N]-或[S=C=N]- ; 1:1。
(2)基态硫原子中,核外电子排布1s22s22p63s23p4,核外占据最高能级为p,电子云轮廓图形状为哑铃形;硫的一种同素异形体(结构如图所示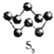 )易溶于
)易溶于![]() ,此硫的同素异形体形成分子晶体,硫原子电子对数为
,此硫的同素异形体形成分子晶体,硫原子电子对数为![]() ,杂化类型为
,杂化类型为![]() ,S8和二硫化碳都是非极性分子,根据相似相溶原理S8易溶于二硫化碳;正确答案:哑铃形; sp3; S8和二硫化碳都是非极性分子,根据相似相溶原理S8易溶于二硫化碳。
,S8和二硫化碳都是非极性分子,根据相似相溶原理S8易溶于二硫化碳;正确答案:哑铃形; sp3; S8和二硫化碳都是非极性分子,根据相似相溶原理S8易溶于二硫化碳。
(3)金刚石为原子晶体,所以氮化硼为原子晶体;则其晶体中配位键与普通共价键数目之比为4:12=1:3;根据坐标B(0,0,0);B(l/2,0,l/2);B(l/2,l/2,0),可知晶胞的边长为1,距离上述三个B原子最近且等距的N原子的坐标参数为(![]() ,
,![]() ,
,![]() );正确答案: 原子;1:3;(,,)。
);正确答案: 原子;1:3;(,,)。
(4)根据晶胞结构可知,铁的晶胞为体心立方堆积;设晶胞的棱长为acm,则晶胞的体积为a3cm3;该晶胞中含有铁原子个数为8×1/8+1=2,所以该晶胞的体积a3=![]() ;晶胞的体对角线为√3a
;晶胞的体对角线为√3a![]() ,铁原子半径为体对角线的
,铁原子半径为体对角线的![]() =
= ![]() ×
×![]() ×1010 pm;正确答案:体心立方堆积;
×1010 pm;正确答案:体心立方堆积;![]() ×
×![]() ×1010 。
×1010 。
(5)(a)SO2Cl2的空间构型为 ,价层电子对个数=孤电子对个数+σ键个数=0+4=4,故S原子采取sp3杂化,结构四面体构型;正确答案:四面体。
,价层电子对个数=孤电子对个数+σ键个数=0+4=4,故S原子采取sp3杂化,结构四面体构型;正确答案:四面体。
(b)SO2(g)+Cl2(g)+SCl2(g)![]() 2SOCl2(g),K1=c2(SOCl2)/c(SCl2)c(Cl2) c(SO2);SO2(g)+Cl2(g)
2SOCl2(g),K1=c2(SOCl2)/c(SCl2)c(Cl2) c(SO2);SO2(g)+Cl2(g)![]() SO2Cl2(g),K2= c(SOCl2)/ c(Cl2) c(SO2);SO2Cl2(g)+SCl(g)2SOCl2(g),K= c2(SOCl2)/ c(SCl2) c(SOCl2) 所以是由(Ⅰ)、(Ⅱ)相除得到,K=K1/K2;正确答案:K1/K2。
SO2Cl2(g),K2= c(SOCl2)/ c(Cl2) c(SO2);SO2Cl2(g)+SCl(g)2SOCl2(g),K= c2(SOCl2)/ c(SCl2) c(SOCl2) 所以是由(Ⅰ)、(Ⅱ)相除得到,K=K1/K2;正确答案:K1/K2。
(c)①根据图像可知,温度T2>T1,温度由T2升高到T1,二氧化硫的转化率增大,反应正向移动,该反应正反应为放热反应;根据反应方程式可知:
SO2(g)+Cl2(g) ![]() SO2Cl2(g)
SO2Cl2(g)
起始量 1 1 0
变化量 0.8 0.8 0.8
平衡量 0.2 0.2 0.8
到平衡时的平均反应速率v(SO2)=0.8/50×5=.3.2×10-3mol/(L·min) 为了提高SO2的平衡转化率,除改变温度外,还可以采取的一条措施增加氯气浓度、减少产物浓度等;正确答案: 放热;3.2×10-3mol/(L·min);充入氯气、分离产物等 。
②根据图像可知,温度为T2时,压强为101kPa,二氧化硫的转化率为60%,据此进行下列计算:
SO2(g)+Cl2(g) ![]() SO2Cl2(g)
SO2Cl2(g)
起始量 1 1 0
变化量 0.6 0.6 0.8
平衡量 0.4 0.4 0.6
平衡分压 2/7 2/7 3/7
根据压强之比等于气体的物质的量之比,所以:2:101=(0.4+0.4+0.6):p平,p平=70.7 kPa;该反应的化学平衡常数Kp=KP(SO2Cl2) p平/ KP(Cl2) p平KP(CSO2) p平= 3/7/ (2/7 p平)2= 0.0743;正确答案:70.7;0.0743(kPa)-1或![]() (kPa)-1 或
(kPa)-1 或![]() (kPa)-1 。
(kPa)-1 。
(d)AlCl3属于强酸弱碱盐,水解显酸性:AlCl3+3H2O![]() Al(OH)3+3HCl↑;SOCl2与结晶水反应生成盐酸,抑制了AlCl3水解;正确答案:SOCl2与结晶水反应产生的HCl抑制了AlCl3水解。
Al(OH)3+3HCl↑;SOCl2与结晶水反应生成盐酸,抑制了AlCl3水解;正确答案:SOCl2与结晶水反应产生的HCl抑制了AlCl3水解。


科目:高中化学 来源: 题型:
【题目】2008年5月,我国四川地区发生特大地震灾害,地震过后,饮用水的消毒杀菌成为抑制大规模传染性疾病暴发的有效方法之一。氯气(Cl2)是制备消毒剂的主要原料之一。工业上主要采用电解饱和食盐水的方法来制取Cl2。请回答下列问题:
(1)电解之前,食盐水需要精制,目的是除去粗盐的中的Ca2+、Mg2+、SO42-等杂质离子,使用的试剂有:①Na2CO3溶液 ②Ba(OH)2溶液 ③稀盐酸。其中合理的加入顺序为___(填序号);
(2)实验室欲配制6.00 mol/L的食盐水90 mL,回答下列问题:
①需要纯净的NaCl___________________g。
②可供选择的仪器有:a玻璃棒 b烧瓶 c烧杯 d胶头滴管 e试管 f托盘天平、砝码 h药匙。在配制食盐水时不需要使用的有_______(填字母),还缺少的仪器是__________。
③配制溶液时,一般可以分为以下几个步骤:计算称量溶解(________________________)转移(_____________________)定容(__________________________)装瓶。
④下列操作会使所配溶液的浓度偏小的是___________________。
A. 转移完溶液后未洗涤玻璃棒和烧杯 B. 容量瓶中原来有少量蒸馏水
C. 定容时,俯视刻度线 D. 称量氯化钠固体时左码右物
(3)在电解饱和食盐水过程中,还生成了H2和NaOH,则所发生反应的化学反应方程式为_____________________________;
(4)将电解生成的Cl2通入NaOH溶液,生成两种盐,其中一种是消毒液的主要成分NaClO,应用氧化还原反应原理,写出此反应的化学方程式是_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过传感器可以监测空气中甲醛的含量。一种燃料电池型甲醛气体传感器的原理如图所示,下列说法错误的是
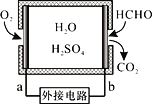
A. a为电池的正极,发生还原反应
B. b极的电极反应为HCHO+H2O-4e-==CO2+4H+
C. 传感器工作过程中,电解质溶液中硫酸的浓度减小
D. 当电路中转移2×10-4 mol电子时,传感器内参加反应的HCHO为3.0 mg
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铷元素(Rb)位于元素周期表中第五周期第ⅠA族,有关Rb及其化合物的性质推测正确的是( )
A.Rb与冷水反应比K更剧烈
B.Rb投入CuSO4溶液中可置换出Cu
C.Rb与O2反应只有Rb2O产生
D.Rb2CO3难溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应属于氧化还原反应的是
A. CaCO3+2HCl=CaCl2+CO2↑+ H2O
B. CaO+H2O=Ca(OH)2
C. 2H2O2![]() 2H2O+O2↑
2H2O+O2↑
D. CaCO3![]() CaO+CO2↑
CaO+CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸(乙二酸)存在于自然界的植物中,草酸的钠盐和钾盐易溶于水,而其钙盐难溶于水;草酸晶体(H2C2O4·2H2O)无色,熔点为101℃,易溶于水,受热脱水、升华,170℃以上分解。回答下列问题:
(1)甲组同学按照如图所示的装置,通过实验检验草酸晶体的分解产物。装置C中可观察到的现象是________________________,由此可知草酸晶体分解的产物中有_______。
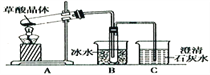
装置B的主要作用是_________________________________________________________。
(2)乙组同学认为草酸晶体分解的产物中含有CO,为进行验证,选用甲组实验中的装置A、B和下图所示的部分装置进行实验。

①乙组的实验装置中,依次连接的合理顺序为A→B→(_____)→( )→( )→( )→I。装置H反应管中盛有的物质是__________;I中集气瓶收集到的气体主要是_________。
②能证明草酸晶体分解产物中有CO的现象是_______________________________。
(3)丙组同学欲进一步证明产物CO能否与Na2O2反应。从A~J中选用装置进行实验,最简单的装置接口连接顺序是:A→B→(_____)→J(盛Na2O2的干燥管);实验后用J中的固体进行验证的方法是:__________________________________(可另选试剂)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列各题:
Ⅰ.下列实验不能成功的是______________
A.为了检验R-X是碘代烷,将R-X与NaOH水溶液共热,经充分反应后冷却,向冷却液中加稀HNO3酸化后,再加AgNO3溶液,观察沉淀颜色
B.为检验淀粉是否水解,将淀粉与少量稀H2SO4共热一段时间,加入新制的Cu(OH)2 ,观察变化
C. 向银氨溶液中加入几滴乙醛后用酒精灯加热至沸制取银镜
D.无水乙醇与浓硫酸按1:3的体积比混合快速加热到170℃左右制取乙烯
Ⅱ.有机物M的结构简式为: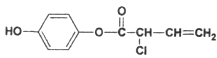 ,则:
,则:
(1)1 mol M最多消耗的H2、Br2、NaOH溶液的比值为_________________;
写出M在酸性(稀硫酸)条件下的水解反应方程式_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下微粒含配位键的是( )
①[Al(OH)4]- ②CH4 ③OH- ④NH![]() ⑤[Cu(NH3)4]2+ ⑥Fe(SCN)3 ⑦H3O+ ⑧[Ag(NH3)2]OH
⑤[Cu(NH3)4]2+ ⑥Fe(SCN)3 ⑦H3O+ ⑧[Ag(NH3)2]OH
A. ①②④⑦⑧ B. ③④⑤⑥⑦ C. ①④⑤⑥⑦⑧ D. 全部
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com