
| A. | (NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH-═Fe(OH)2↓ | |
| B. | 向明矾溶液中滴加Ba(OH)2溶液,恰好使SO${\;}_{4}^{2-}$沉淀完全:2Al3++3SO${\;}_{4}^{2-}$+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ | |
| C. | AlCl3溶液中加入过量稀氨水:Al3++4NH3•H2O═AlO${\;}_{2}^{-}$+4NH${\;}_{4}^{+}$+2H2O | |
| D. | 向FeBr2溶液中通入足量氯气:2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- |
分析 A.氢氧化钠过量,铵根离子也参与反应;
B.硫酸根离子完全沉淀时,铝离子与企业广告离子的物质的量之比为1:4,反应生成偏铝酸根离子;
C.氨水为弱碱,二者反应生成氢氧化铝沉淀;
D.氯气足量,亚铁离子和溴离子都完全被氧化.
解答 解:A.(NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2,铵根离子和亚铁离子都参与反应,正确的离子方程式为:Fe2++2NH4++4OH-═Fe(OH)2↓+2NH3•H2O,故A错误;
B.明矾溶液中滴加Ba(OH)2至SO42-完全沉淀,铝离子恰好反应生成偏铝酸根离子,反应的化学方程式为:KAl(SO4)2+2Ba(OH)2=2BaSO4↓+KAlO2+2H2O,对应的离子方程为:Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+AlO2-+2H2O,故B错误;
C.AlCl3溶液中加入过量稀氨水,反应生成氢氧化铝沉淀,正确的离子方程式为:Al3++3NH3•H2O=Al(OH)3↓+3NH4+,故C错误;
D.FeBr2溶液中通入足量氯气,亚铁离子和溴离子都完全反应,反应的离子方程式为:2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl-,故D正确;
故选D.
点评 本题考查了离子方程式的书写判断,为高考的高频题,属于中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.


 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案科目:高中化学 来源: 题型:实验题
| 沸点/℃ | 水溶性 | |
| 甲醇 | 65 | 与水混溶 |
| 甲醛 | -21 | 与水混溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苏打不仅可用于治疗胃病,还可作灭火剂 | |
| B. | 用酸洗灼烧后的铂丝蘸取样品灼烧,火焰呈紫色,说明该样品中含钾元素 | |
| C. | 纯铁的熔点比生铁的低 | |
| D. | 日用铝制品表面覆盖着氧化膜,对内部金属起保护作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NF3是氧化剂,H2O是还原剂 | |
| B. | NF3是一种无色、无臭的气体,因此NF3在空气中泄漏时不易被察觉 | |
| C. | 一旦NF3泄漏,可以用NaOH溶液喷淋的方法减少空气污染 | |
| D. | 若生成0.2 mol HNO3,则转移0.2 mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
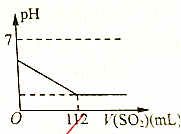 在标准状况下,向100mL新配制的氯水中通入SO2气体,SO2被氧化成硫酸,溶液的pH值变化如图所示,则原氯水的物质的量浓度为( )
在标准状况下,向100mL新配制的氯水中通入SO2气体,SO2被氧化成硫酸,溶液的pH值变化如图所示,则原氯水的物质的量浓度为( )| A. | 0.5mol/L | B. | 0.05mol/L | C. | 1mol/L | D. | 0.1mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室通常用重结晶的方法分离提纯液体有机物 | |
| B. | 通过李比希燃烧法,可以确定有机物的结构 | |
| C. | 对有机物分子红外光谱图的研究有助于确定有机物分子中的官能团种类 | |
| D. | 核磁共振氢谱图中吸收峰的面积即为有机物中H原子的数目 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
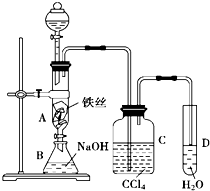 某化学课外小组用如图装置制取溴苯.先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中.
某化学课外小组用如图装置制取溴苯.先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com