
| A. | 元素原子半径大小呈周期性变化 | |
| B. | 元素原子量依次递增 | |
| C. | 元素原子核外电子排布呈周期性变化 | |
| D. | 元素的最高正化合价呈周期性变化 |
分析 A.原子半径属于元素的性质,元素的原子半径随原子序数的递增呈周期性变化;
B.元素的原子的相对原子质量增大,但不呈现周期性的变化;
C.随着原子序数的递增,元素原子的核外电子排布(电子层数和最外层电子数)呈现周期性的变化而引起元素性质的周期性变化;
D.元素化合价属于元素的性质,不能解释元素性质周期性变化的原因.
解答 解:A.原子半径属于元素的性质,元素的原子半径的周期性变化是原子的电子排布周期性变化的结果,故A错误;
B.元素的原子的相对原子质量增大,但不呈现周期性的变化,则不能决定元素性质出现周期性变化,故B错误;
C.由原子的电子排布可知,随原子序数的递增,电子层数和最外层电子数都呈现周期性的变化而引起元素性质的周期性变化,即原子的电子层排布的周期性变化是引起元素性质周期性变化的决定因素,故C正确;
D.化合价属于元素的性质,元素的最高正化合价的周期性变化是原子的电子排布周期性变化的结果,故D错误;
故选C.
点评 本题考查原子结构及周期律,为高频考点,把握元素的性质、元素周期律的实质为解答的关键,侧重分析与应用能力的考查,注意周期律实质的理解,题目难度不大.


 优生乐园系列答案
优生乐园系列答案科目:高中化学 来源: 题型:选择题
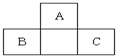 A、B、C均为短周期元素,它们在周期表中的位置如图.已知B、C两元素在周期表中族序数之和是A元素族序数的2倍;B、C元素的原子序数之和是A元素原子序数的4倍,则A、B、C所在的一组元素是( )
A、B、C均为短周期元素,它们在周期表中的位置如图.已知B、C两元素在周期表中族序数之和是A元素族序数的2倍;B、C元素的原子序数之和是A元素原子序数的4倍,则A、B、C所在的一组元素是( )| A. | Be、Na、Al | B. | B、Mg、Si | C. | C、Al、P | D. | O、P、Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氟酸可用于雕刻玻璃,说明氢氟酸具有强酸性 | |
| B. | 浓硝酸在光照下颜色变黄,说明浓硝酸具有强氧化性 | |
| C. | 常温下浓硫酸可用铝罐贮存,说明铝与浓硫酸不反应 | |
| D. | 氨水可使酚酞试剂变为红色,说明氨水显碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | CaCO3(s)═CaO(s)+CO2(g)室温下不能自发进行,说明该反应的△H<0 | |
| B. | 镀铜铁制品镀层受损后,铁制品比受损前更容易生锈 | |
| C. | N2(g)+3H2(g)═2NH3(g)△H<0,其他条件不变时升高温度,反应速率v(H2)和H2的平衡转化率均增大 | |
| D. | 水的离子积常数Kw 随着温度的升高而增大,说明水的电离是吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铸铁输油管道应埋在干燥致密不透气的土壤中 | |
| B. | 白铁(镀Zn铁)表面有划损时,也能阻止铁被氧化 | |
| C. | 钢铁发生电化学腐蚀时,负极发生的反应是2H2O+O2+4e-=4OH- | |
| D. | 在空气中,金属铝表面能迅速被氧化形成保护膜,因此铝不容易被腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质分子中不一定存在化学键 | |
| B. | 离子化合物中只含离子键,不含共价键 | |
| C. | 共价化合物一定含共价键,可能含离子键 | |
| D. | 非金属元素组成的化合物不存在离子键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com