
| A. | 标准状况下,2.24LH2O含有H-O键的数目为0.2NA | |
| B. | 5.6g Fe与0.1molCl2充分反应转移电子的数目为0.3NA | |
| C. | 常温下,lLpH=2的硫酸中由水电离出的H+的数目为0.01NA | |
| D. | 3g乙酸和葡萄糖混合物完全燃烧所消耗的氧分子数为0.1NA |
分析 A.标准状况下水的状态不是气体;
B.0.1mol氯气与铁完全反应最多转移0.2mol电子;
C.硫酸抑制了水的电离,其溶液中氢氧根离子是水电离的;
D.乙酸和葡萄糖的最简式都是CH2,根据最简式计算.
解答 解:A.标况下水不是气体,不能使用标况下的气体摩尔体积计算,故A错误;
B.0.1molCl2与Fe完全反应最多转移0.2mol电子,充分反应转移电子的数目为0.2NA,故B错误;
C.pH=2的硫酸中氢离子浓度为0.1mol/L,硫酸溶液中的氢氧根离子是水电离的,水电离的氢离子浓度为1×10-12mol/L,1L该溶液中水电离的氢离子的物质的量为1×10-12mol,由水电离出的H+的数目为1×10-12NA,故C错误;
D.甲醛、乙酸与葡萄糖的实验式相同,都是CH2O,3gCH2O的物质的量为:$\frac{3g}{30g/mol}$=0.1mol,0.1molCH2O完全燃烧消耗0.1mol氧气,消耗的氧分子数为0.1NA,故D正确;
故选D.
点评 本题考查阿伏加德罗常数的综合应用,题目难度中等,明确标况下气体摩尔体积的使用条件为解答关键,注意掌握以物质的量为中心的各化学量与阿伏加德罗常数的关系,试题有利于培养学生的化学计算能力.


 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:选择题
| A. | 铜与浓硝酸反应 | |
| B. | 铜片和稀硝酸共热反应 | |
| C. | 先灼烧废铜屑生成氧化铜,然后再用稀硝酸溶解 | |
| D. | 适当温度下,使铜片在持续通入空气的硝酸中溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A、B同时作原电池的电极时,A的质量增加 | |
| B. | A原子电子层数比B原子电子层数多 | |
| C. | 1molA从酸中置换出H2比1molB从酸中置换出H2多 | |
| D. | 常温时,A能从稀酸溶液中置换出氢,而B不能与稀酸溶液发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 吸热反应一定需要加热才能发生 | |
| B. | 碳不完全燃烧属于吸热反应 | |
| C. | Cu、Zn、稀硫酸组成的原电池中,Zn是负极 | |
| D. | 组成原电池的两极一定是不同的金属 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 过氧化钠的电子式: | B. | F-的结构示意图: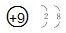 | ||
| C. | 中子数为20的氯原子${\;}_{17}^{20}$Cl | D. | NH3的电子式: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH2CH2CH2Cl | B. |  | C. |  | D. |  |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题


查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 物质W、X、Y、Z的转化关系如图所示,其中X、W是单质,Y、Z是化合物.
物质W、X、Y、Z的转化关系如图所示,其中X、W是单质,Y、Z是化合物.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com