
【题目】2015年发生的天津港有关仓库物品爆炸涉及电石与氰化钠等,而CN-作为配位剂可形成[Au(CN)2]-、[Ag(CN)2]-、[Zn(CN)4]2-、[Fe(CN)3]4-、[Fe(CN)4]3-等。常把原子个数相同,最外层电子数也相同的微粒称作等电子体,同时它们的结构相似。
试分析并回答:
(1)电石的主要成分是__________(写化学式),其中阴离子与CN-是等电子体,写出CN-的电子式:__________。
(2)有着“闪电式死亡”之称的剧毒物品氰化钠,在地面水中很不稳定,pH大于7时,可被氧气氧化成碳酸盐和氨气,试写出该反应的离子方程式:______。
(3)以剧毒物氰化钠比例,从反应原理角度去思考如何防止其污染。试提出两个有关应用的好方案________、_______。
(4)电石中还含有CaS等,与水反应还有H2S的生成,H2S完全氧化生成S2,S2又可催化氧化生成SO3。已知2SO2(g)+O2(g)![]() 2SO3(g) △H<0。某温度下,将2mol SO2和1 mol O2置于10L密闭容器中,反应达到平衡后,SO2的平衡转化率(a)与体系总压强(p)的关系如图所示。
2SO3(g) △H<0。某温度下,将2mol SO2和1 mol O2置于10L密闭容器中,反应达到平衡后,SO2的平衡转化率(a)与体系总压强(p)的关系如图所示。
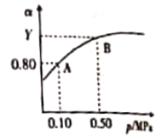
则①Y大于0.8的原因是__________;
②K(A)____________(填“大于”“等于”或“小于”)K(B);
③若压强为0.10MPa,试做出T1、T2不同温度下(设T2< T1)SO2转化率与温度的关系图__________。

【答案】CaC2 ![]()
![]() 方案一:湿法冶金; 方案二:含氰废水制备亚铁氰化钾(也可以用有关盐处理,使其转化为含氰配合物) 该反应是气体体积缩小的反应,温度一定时,增大压强,平衡向正反应方向移动,二氧化硫的转化率增大 等于
方案一:湿法冶金; 方案二:含氰废水制备亚铁氰化钾(也可以用有关盐处理,使其转化为含氰配合物) 该反应是气体体积缩小的反应,温度一定时,增大压强,平衡向正反应方向移动,二氧化硫的转化率增大 等于 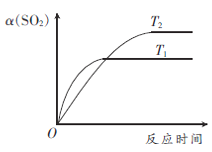
【解析】
(1)电石主要为碳化钙;根据碳化钙的结构推出CN-的电子式;
(2)根据题意结合氧化还原反应的规律书写离子方程式;
(3)结合氰化物的工业用法设计方案;
(4)2SO2(g)+O2(g)![]() 2SO3(g)为气体体积缩小的放热反应,结合外因对化学反应速率与化学平衡的影响效果回答;
2SO3(g)为气体体积缩小的放热反应,结合外因对化学反应速率与化学平衡的影响效果回答;
(1)电石主要成分的化学式为:CaC2,其阴离子中C与C原子共用3个电子对,因等电子体的结构相似,故CN-的电子式为:![]() ,故答案为:CaC2;
,故答案为:CaC2;![]() ;
;
(2)氰化钠中C为+2价,N为-3价,在碱性条件下可被氧气氧化成磷酸钠和氨气,根据氧化还原反应的规律可知,反应的离子方程式为:![]() ;
;
(3)根据题意可设计如下:
方案一:用湿法冶金氰化法提炼,即采用稀的NaCN溶液处理已粉碎的矿石,同时通入空气,把少量的金浸取到溶液中生成Na[Au(CN)2];
方案二:含氰废水制备亚铁氰化钾(也可以用有关盐处理,使其转化为含氰配合物),故答案为:方案一:湿法冶金;方案二:含氰废水制备亚铁氰化钾(也可以用有关盐处理,使其转化为含氰配合物);
(4)①该反应是气体体积缩小的反应,温度一定时,增大压强,平衡向正反应方向移动,二氧化硫的转化率增大,因此Y大于0.8,故答案为:该反应是气体体积缩小的反应,温度一定时,增大压强,平衡向正反应方向移动,二氧化硫的转化率增大;
②温度一定时,K值不变,因此K(A)等于K(B),故答案为:等于;
③2SO2(g)+O2(g)![]() 2SO3(g) △H<0,则压强一定时,升高温度,反应速率均增大,因T2< T1,根据“先拐先平数值大”的原则可知在T1条件先达到平衡状态;反应放热,升高温度不利于SO2的转化率,T2< T1,故达到平衡时,T2条件下SO2的转化率较高,综上SO2转化率与温度的关系图如下:
2SO3(g) △H<0,则压强一定时,升高温度,反应速率均增大,因T2< T1,根据“先拐先平数值大”的原则可知在T1条件先达到平衡状态;反应放热,升高温度不利于SO2的转化率,T2< T1,故达到平衡时,T2条件下SO2的转化率较高,综上SO2转化率与温度的关系图如下:
 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】N2O5是一种新型硝化剂,其性质和制备受到人们的关注。已知N2O5能与水发生反应,并放出大量的热。
Ⅰ.一定温度下,在恒容密闭容器中N2O5发生下列反应:2N2O5(g)![]() 4NO2(g)+O2(g)ΔH。
4NO2(g)+O2(g)ΔH。
(1)下表为反应在T1温度下的部分实验数据:
t/s | 0 | 500 | 1000 |
c(N2O5)/mol·L—1 | 5.00 | 3.52 | 2.48 |
则500s内NO2的生成速率为______________。
(2)反应达到平衡后,若再通入一定量N2O5,达到新平衡时,N2O5的转化率将______(填“增大”、“减小”、“不变”)。
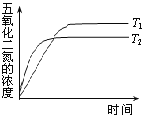
(3)在温度T1和T2时,N2O5的浓度与反应时间的关系如图所示。据此判断:T1______T2(填“>”、“<”或“=”,下同),ΔH______0。
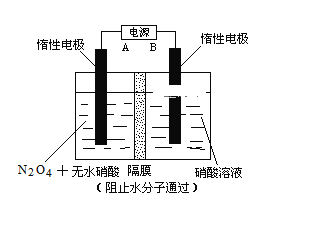
Ⅱ.下图所示装置,可用于制备N2O5气体。A是电源的____________(填“负极”或“正极”),电解池的阳极反应式为______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH4(其中C为-4价)既是一种重要的能源,也是一种重要的化工原料。
(1)已知8.0gCH4完全燃烧生成二氧化碳和液态水时放出444.8kJ热量。若一定量的甲烷完全燃烧生成二氧化碳和液态水时放出1334.4kJ的热量,则需要标准状况下的氧气约___L。
(2)以CH4为燃料可设计成结构简单、能量转化率高、对环境无污染的燃料电池,其工作原理如图甲所示,通入2.24L(已换算为标准状况)a气体时,通过质子交换膜转移的H+数目为___(设NA为阿伏加德罗常数的值)。

(3)在一定温度和催化剂作用下,CH4与CO2可直接转化成乙酸,这是实现“减排”的一种研究方向。
①在不同温度下,催化剂的催化效率与乙酸的生成速率如图乙所示,则该反应的最佳温度应控制在___℃左右。
②该反应催化剂的有效成分为偏铝酸亚铜(CuAlO2,难溶物)。将CuAlO2溶解在稀硝酸中生成两种盐并放出NO气体,其反应的离子方程式为___。
③CH4还原法是处理NOx气体的一种方法。已知一定条件下CH4与NOx反应转化为N2、CO2和H2O,若标准状况下8.96LCH4可处理22.4LNOx,则x值为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空。
(1)有下列各组物质:
(A)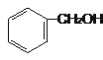 和
和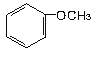 ;(B)CH2=CH-CH=CH2和CH3-CH2-C=CH;(C)
;(B)CH2=CH-CH=CH2和CH3-CH2-C=CH;(C) ;(D)
;(D)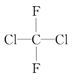 和
和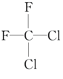 ;(E)甲烷和新戊烷
;(E)甲烷和新戊烷
其中____组两物质互为同系物;_______组两物质互为同分异构体;______组两物质互为同一物质;A组第一个物质的名称是:_________。
(2)写出1,3﹣丁二烯与Br2的CCl4溶液发生1,4﹣加成后的产物的结构简式:___________。
(3)写出由甲苯生成TNT(2,4,6﹣三硝基甲苯)的方程式:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某白色粉状固体X,它是碘的一种较稳定氧化物,M=334 g·mol-1;有关化学性质与转化如下:
①X在343K时,与CO作用生成B和CO2;
②X在573K时,分解生成A和B;
③X与水作用生成D;
④D+HCl→B+Z+H2O;
⑤Z与氯仿在一定条件下生成灭火剂Y等。
又知A、B、Z是常见单质。试分析并回答:
(1)组成B的元素处于第_____________族。
(2)写出②的化学方程式:_______________。
(3)写出Y的分子式:_________
(4)B与KI作用生成的阴离子的符号是_________
(5)写出④的离子方程式:____________。
(6)根据较为完全的反应①,再利用某一经典反应原理(方法),在工业上可以测定废气中CO的含量。试简述其测定方法:________。
(7)Z与氯仿反应的方程式一般为Z+氯仿→Y+氢化物,但也有另一种可能,其化学方程式是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组依据甲烷燃烧的反应原理,设计如图a所示的电池装置:
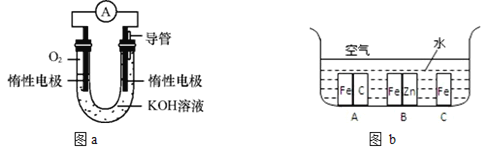
(1)该电池的能量转化形式为____________。
(2)该电池正极的电极反应为____________。
(3)工作一段时间后,测得溶液的pH______,该电池总反应的化学方程式为_________。
(4)在生产生活中,金属腐蚀所带来的损失非常严重,所以防止金属腐蚀已经成为科学研究和技术领域的重大问题。兴趣小组的同学在实验室对金属腐蚀进行了探究。如图b所示,铁处于A、B、C三种不同的环境中,铁被腐蚀的速率由大到小的顺序是(填序号)_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E 均为有机物,其中 B 是化学实验中常见的有机物, 它易溶于水并有特殊香味;A 的产量可衡量一个国家石油化工发展的水平,G 是生活中常见的高分子材料。有关物质的转化关系如图甲所示:
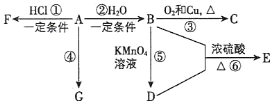
(1)写出 A 的结构式_____;B 中官能团的名称为_____。
(2)写出下列反应的化学方程式:
反应③____;
反应④____。
(3)实验室利用反应⑥制取 E,常用如图装置:
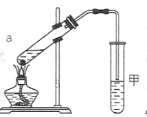
①a 试管中主要反应的化学方程式为_____。
②实验开始时,试管甲中的导管不伸入液面下的原因是_____;当观察到试管甲中_____时,认为反应基本完成。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NF3(三氟化氮)在常温常压下是无色、无味的气体,是微电子工业中一种优良的等离子蚀刻气体。回答下列问题:
(1)NF3的电子式为______,N元素的化合价为______。
(2)F2与NH3直接反应生成NF3的化学方程式为______。
(3)实验室模拟工业上利用电解熔融NH4HF2(NH4FHF)法制取NF3,阳极为以Ni为基本材料的合金(内含其他金属,忽略镍及其他金属的反应),阴极为碳素钢,电解废液可回收再利用。
①电解时NF3在______极生成;阴极产生的气体是______(填化学式)。
②电解后废液(含Ni少量Fe和Cu的单质及NH4HF2等)可经如下流程进行回收再利用:
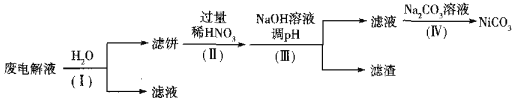
已知该实验条件下,部分金属离子开始沉淀与沉淀完全的pH如下表
金属离子 | Ni2+ | Fe2+ | Cu2+ | Fe3+ |
开始沉淀时的pH | 7.2 | 7.0 | 4.7 | 1.9 |
沉淀完全时的pH | 9.2 | 9.0 | 6.7 | 3.2 |
步骤I的目的是______;步骤Ⅱ滤饼中Ni溶于硝酸的离子方程式为______(HNO3的还原产物为NO);步骤Ⅲ调节pH时,理论上pH应控制的范围是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组为确定一种从煤中提取的液态烃X的结构,对其进行探究。
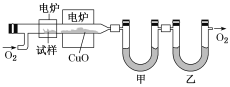
步骤一:这种碳氢化合物蒸气通过热的氧化铜(催化剂),氧化成二氧化碳和水,再用装有无水氯化钙和固体氢氧化钠的吸收管完全吸收。2.12 g有机物X的蒸气氧化产生7.04 g二氧化碳和1.80 g水。
步骤二:通过仪器分析得知X的相对分子质量为106。
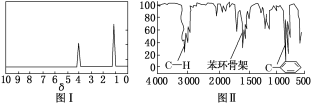
步骤三:用核磁共振仪测出X的核磁共振氢谱有2个峰,其面积之比为2∶3,如图Ⅰ。
步骤四:利用红外光谱仪测得X分子的红外光谱如图Ⅱ。
试填空:
(1)X的分子式为_____;X的名称为_____。
(2)步骤二中的仪器分析方法称为________。
(3)写出X与足量浓硝酸和浓硫酸混合物反应的化学方程式:________。
(4)写出X符合下列条件的同分异构体的结构简式_______________。
①芳香烃 ②苯环上一氯代物有三种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com