
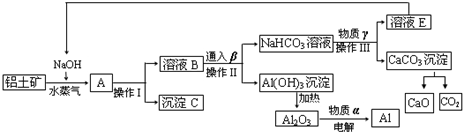
分析 铝土矿中含有氧化铝和氧化铁,向铝土矿中加入NaOH溶液,发生反应Al2O3+2OH-═2AlO2-+H2O,氧化铁不溶于NaOH溶液,然后过滤,得到溶液B为NaOH、NaAlO2混合溶液,沉淀C为Fe2O3,向溶液B中通入CO2,发生反应2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-、2OH-+CO2=CO32-+H2O,然后过滤得到沉淀Al(OH)3和NaHCO3溶液,向溶液中加入CaO,发生反应NaHCO3+CaO═NaOH+CaCO3↓,然后过滤,将NaOH循环利用;将Al(OH)3加热得到Al2O3,电解熔融Al2O3得到Al.以此解答该题.
解答 解:铝土矿中含有氧化铝和氧化铁,向铝土矿中加入NaOH溶液,发生反应Al2O3+2OH-═2AlO2-+H2O,氧化铁不溶于NaOH溶液,然后过滤,得到溶液B为NaOH、NaAlO2混合溶液,沉淀C为Fe2O3,向溶液B中通入CO2,发生反应2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-、2OH-+CO2=CO32-+H2O,然后过滤得到沉淀Al(OH)3和NaHCO3溶液,向溶液中加入CaO,发生反应NaHCO3+CaO═NaOH+CaCO3↓,然后过滤,将NaOH循环利用;将Al(OH)3加热得到Al2O3,电解熔融Al2O3得到Al.
(1)只有氧化铝与氢氧化钠反应,方程式为Al2O3+2 OH-→2AlO2-+H2O,故答案为:Al2O3+2 OH-→2AlO2-+H2O;
(2)由以上分析可知沉淀C为Fe2O3,可用于做颜料,故答案为:Fe2O3;颜料;
(3)从溶液中得到氢氧化钠晶体,可加热浓缩或蒸发浓缩,然后趁热过滤,冷却结晶并过滤洗涤,故答案为:加热浓缩或蒸发浓缩;冷却结晶;过滤洗涤;
(4)煅烧碳酸钙得到CaO和CO2,B生成沉淀需要二氧化碳、碳酸钠转化为碳酸钙需要CaO,所以CaO和CO2能循环利用,
故答案为:CaO;CO2.
点评 本题考查物质分离和提纯以及制备,侧重考查学生分析及知识运用能力,明确物质性质及基本操作方法、反应原理即可解答,知道常见元素化合物知识及常见离子检验方法,题目难度不大.


科目:高中化学 来源: 题型:解答题

| a | b | c | d | |
| n(A)/mol | 2.0 | 1.2 | 2 | 3.6 |
| n(B)/mol | 1.2 | 0.4 | 1 | 1.5 |
| n(c)/mol | 0.1 | 0 | 0.5 | 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在沥青公路上翻晒粮食 | |
| B. | 用生活用煤直接烧烤鸡、鸭 | |
| C. | 用小苏打作发酵粉做面包 | |
| D. | 香肠中加过量亚硝酸钠以保存肉类新鲜 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| 元素编号 | 元素性质或原子结构 |
| T | 失去一个电子后,形成Ne原子电子层结构 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 其单质之一是空气中主要成分,最常见的助燃剂 |
| Z | 阳离子就是一个质子 |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫和氧气反应中作氧化剂 | B. | 氧气的氧化性比硫强 | ||
| C. | 硫的氧化性比氧气强 | D. | 铜是一种具有可变化合价的元素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com