
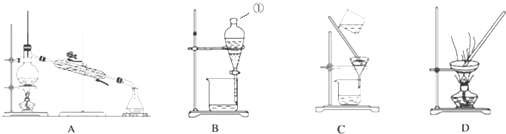
科目:高中化学 来源: 题型:选择题
| A. | 0.1(y-2x)mol/L | B. | 10(2x-y)mol/L | C. | 10(y-x)mol/L | D. | 10(y-2x)mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通入足量氨气:NH4+、SO42-、OH-、AlO2- | |
| B. | 加入足量Na2O2:Na+、Fe2+、SO42-、OH- | |
| C. | 加入过量稀硝酸:Al3+、Fe3+、H+、NO3-、SO42- | |
| D. | 加入过量漂白粉溶液:Ca2+、Fe2+、Cl-、ClO- |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
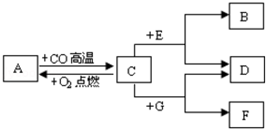 现有A、B、C、D、E、F、G七种物质,C、F是最常见的金属,B是气体单质,D为FeSO4溶液,G为CuSO4溶液,它们之间存在如图所示关系:
现有A、B、C、D、E、F、G七种物质,C、F是最常见的金属,B是气体单质,D为FeSO4溶液,G为CuSO4溶液,它们之间存在如图所示关系:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在标准状况下,22.4L的C6H14所含分子数为NA | |
| B. | 相同质量的H2和Cl2相比,H2的分子数多 | |
| C. | 2.3g金属Na变成Na+时失去的电子数目为0.1NA | |
| D. | 在1L0.1mol/L的HAc溶液中,所含Ac-与HAc之和为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入少量W,逆反应速率增大 | |
| B. | 当容器中气体压强不变时,一定是n(X):n(Y):n(Z)=1:1:1 | |
| C. | 当容器中气体的平均相对分子质量不变时,一定是V(X):V(Y):V(Z)=1:1:1 | |
| D. | 加入X,上述反应的△H增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(H+)=1×10-14mol/L的溶液:K+、Cu2+、I-、SO42- | |
| B. | 水电离出的c(H+)=1×10-14mol/L的溶液:K+、Na+、AlO2-、S2O32- | |
| C. | 能与Al反应生成H2的溶液:NH4+、Ca2+、NO3-、I- | |
| D. | 使石蕊试液变蓝色的溶液:Mg2+、K+、SO 42-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②④ | C. | ③④ | D. | ①② |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com