
| A. | 电解熔融氯化镁制备镁,副产物氯气可以用于制盐酸,循环利用 | |
| B. | 联合制碱法最终副产物为氯化铵,原子利用率小于100% | |
| C. | 步骤②的操作是:在空气中加热氯化镁晶体得到无水氯化镁 | |
| D. | 海水中离子的浓度较小,上述流程图只涉及溴元素的富集过程 |
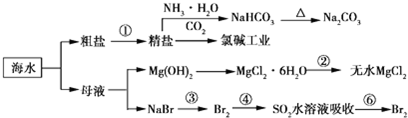
分析 由流程可知,海水晒盐得到粗盐、母液,①为粗盐精制,BaCl2溶液→NaOH溶液→Na2CO3溶液→过滤后加盐酸得到NaCl,NaCl、水、氨气与二氧化碳反应生成碳酸氢钠,第②步中由MgCl2•6H2O获得无水氯化镁,在HCl气流中加热防止水解;第③步将溴离子被氧化为溴单质,第④步中溴单质被还原为溴离子,第⑥步中溴离子被氧化为溴单质,此过程的目的是浓缩、富集溴单质,以此来解答.
解答 解:A.Mg为活泼金属,则电解熔融氯化镁制备镁,副产物氯气与氢气反应生成HCl,溶于水可以用于制盐酸,循环利用,故A正确;
B.NaCl、水、氨气与二氧化碳反应生成碳酸氢钠和氯化铵,加热二者均分解,且产物都可循环利用,故B错误;
C.在空气中加热氯化镁晶体,镁离子水解生成的HCl易挥发,不能得到氯化镁,故C错误;
D.海水中溴离子浓度小,溶剂水很多,则海水提溴,先浓缩、再氧化、富集,图中均涉及提溴过程,故D错误;
故选A.
点评 本题考查了海水资源的综合应用,为高频考点,涉及物质的分离提纯等知识,侧重于化学与生活的综合运用,培养了学生运用知识分析问题的能力,题目难度中等.


 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源: 题型:选择题
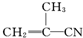 ②
②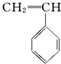 ③
③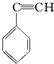 ④CH3-CH═CH-CN,其中可用于合成结构简式为
④CH3-CH═CH-CN,其中可用于合成结构简式为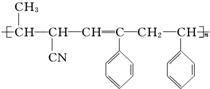 的高分子材料的正确的组合为( )
的高分子材料的正确的组合为( )| A. | ①③④ | B. | ①②③ | C. | ①②④ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通过足量NaOH溶液 | B. | 通过足量的溴水 | ||
| C. | 在Ni粉催化、加热条件下通入H2 | D. | 通入足量的KMnO4 酸性溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②不对 | B. | ③不对 | C. | ①不对 | D. | 全部正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢键 范德华力 非极性键 | B. | 氢键 氢键 极性键 | ||
| C. | 氢键 极性键 范德华力 | D. | 范德华力 氢键 非极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
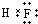 ;A的最高价氧化物对应水化物的化学式为HNO3.
;A的最高价氧化物对应水化物的化学式为HNO3.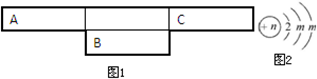
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
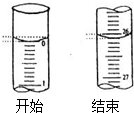 某校化学兴趣小组的同学对一含有少量Na2SO4的NaOH样品中NaOH的含量进行测定,请回答下列问题:
某校化学兴趣小组的同学对一含有少量Na2SO4的NaOH样品中NaOH的含量进行测定,请回答下列问题:| 滴定次数 | 待测氢氧化钠溶液的体积/mL | 0.1000mol/L盐酸的体积(mL) | |
| 滴定前刻度 | 滴定后刻度 | ||
| 第一次 | 20.00 | 0.00 | 26.01 |
| 第二次 | 20.00 | 1.56 | 30.30 |
| 第三次 | 20.00 | 0.22 | 26.21 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com