
【题目】已知硫酸亚铁溶液中加入过氧化钠时发生反应:4Fe2++4Na2O2+6H2O=4Fe(OH)3↓+O2↑+8Na+,则下列说法正确的是
A.该反应中Fe2+是还原剂,O2是还原产物
B.4 mol Na2O2在反应中共得到8NA个电子
C.每生成0.2 mol O2,则被Fe2+还原的氧化剂为0.4 mol
D.反应过程中可以看到白色沉淀转化为灰绿色再转化为红褐色沉淀
【答案】C
【解析】
A.该反应中Fe元素化合价由+2价变为+3价、O元素化合价由-1价变为0价和-2价,得电子化合价降低的反应物是氧化剂、失电子化合价升高的反应物是还原剂,氧化剂对应的产物是还原产物,所以Fe2+和![]() 的过氧化钠作还原剂,Fe(OH)3和O2是氧化产物,故A错误;
的过氧化钠作还原剂,Fe(OH)3和O2是氧化产物,故A错误;
B.该反应中有4mol过氧化钠反应时有3mol过氧化钠得电子发生还原反应,有![]() 的过氧化钠作氧化剂,因此4molNa2O2在反应中共得到6NA个电子,故B错误;
的过氧化钠作氧化剂,因此4molNa2O2在反应中共得到6NA个电子,故B错误;
C.根据方程式,生成0.2 mol O2,反应的Fe2+为0.8mol,被0.8mol Fe2+还原的氧化剂(Na2O2)的物质的量=![]() =0.4mol,故C正确;
=0.4mol,故C正确;
D.该反应中有氧气生成,所以不能生成氢氧化亚铁沉淀,而是直接生成红褐色沉淀,故D错误;
故选C。


科目:高中化学 来源: 题型:
【题目】AlPO4的沉淀溶解平衡曲线如图所示(T2>T1).下列说法正确的是( )
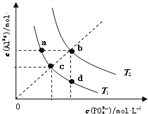
A. 图象中四个点的Ksp:a=b>c>d
B. AlPO4在b点对应的溶解度大于c点
C. AlPO4(s)Al3+(aq)+PO43-(aq)△H<0
D. 升高温度可使d点移动到b点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新型锂空气电池具有使用寿命长、可在自然空气环境下工作的优点。其原理如图所示(电解质为离子液体和二甲基亚砜),电池总反应为:![]() 下列说法不正确的是( )
下列说法不正确的是( )
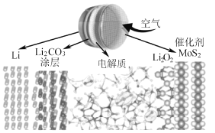
A.充电时电子由Li电极经外电路流入Li2O2
B.放电时正极反应式为2Li++O2 +2e-=Li2O2
C.充电时Li电极与电源的负极相连
D.碳酸锂涂层既可阻止锂电极的氧化又能让锂离子进入电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近科学家获得了一种稳定性好、抗氧化能力强的活性化合物A;其结构如下:

为了研究X的结构,将化合物A在一定条件下水解只得到 和C。经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生。
和C。经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生。
请回答下列问题:
(1)化合物B能发生下列哪些类型的反应________。
A.取代反应 B.加成反应
C.缩聚反应 D.氧化反应
(2)写出化合物C所有可能的结构简式______________________________。
(3)C可通过下图所示途径合成,并制取冬青油和阿司匹林。

(ⅰ)写出有机物的结构简式:D:______________,C:________________,E:______________。
(ⅱ)写出变化过程中①、⑥的化学方程式(注明反应条件)
反应①__________________________________;反应⑥_____________________________。
(ⅲ)变化过程中的②属于____________反应,⑦属于________反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液X含有K+、Mg2+、Fe3+、Al3+、Fe2+、Cl-、CO32-、OH-、SiO32-、NO3-、SO42-中的几种,已知该溶液中各离子物质的量浓度均为0.2mol·L-1(不考虑水的电离及离子的水解)。为确定该溶液中含有的离子,现进行了如下的操作:

下列说法正确的是
A.无色气体可能是NO和CO2的混合物
B.原溶液可能存在Fe3+
C.溶液X中所含离子种类共有4种
D.另取l00mL原溶液X,加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,理论上得到的固体质量为2.4g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用MnO2与浓盐酸反应制备Cl2(反应装置如图所示)

(1)制备实验开始时,先检查装置气密性,接下来的操作依次是______(填序号)
A.往烧瓶中加入MnO2粉末 B.加热 C.往烧瓶中加入浓盐酸
(2)制备反应会因盐酸浓度下降而停止.为测定已分离出过量MnO2后的反应残余液中盐酸的浓度,探究小组提出下列实验方案:
甲方案:与足量AgNO3溶液反应,称量生成的AgCl质量。
乙方案:采用酸碱中和滴定法测定。
丙方案:与已知量CaCO3(过量)反应,称量剩余的CaCO3质量。
丁方案:与足量Zn反应,测量生成的H2体积。
继而进行下列判断和实验:判定甲方案不可行,理由是______________。
(3)进行乙方案实验: 准确量取残余清液稀释一定倍数后作为试样。
a.量取试样20.00 mL,用0.1000 mol·L-1NaOH标准溶液滴定,消耗22.00mL,该次滴定测得试样中盐酸浓度为_____mol·L-1
b.平行滴定后获得实验结果。
采用此方案还需查阅资料知道的数据是:________。
(4)丙方案的实验发现,剩余固体中含有MnCO3,说明碳酸钙在水中存在______,测定的结果会:______(填“偏大”、“偏小”或“准确”)
(5)进行丁方案实验:装置如图所示(夹持器具已略去)

①使Y形管中的残余清液与锌粒反应的正确操作是将_________转移到_____________中。
②反应完毕,每间隔1分钟读取气体体积,气体体积逐次减小,直至不变。气体体积逐次减小的原因是______(排除仪器和实验操作的影响因素)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚合硫酸铁、明矾可用作净水剂。某课题组拟以废弃的铝铁合金为原料制备聚合硫酸铁和明矾,设计化工流程如下:
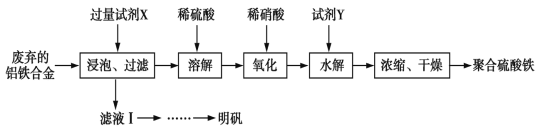
已知:聚合硫酸铁能溶于水,微溶于乙醇,其化学式可表示为[Fe2(OH)x(SO4)y]n。
(1)在聚合硫酸铁中,x、y之间的关系是_______________。试剂X中溶质的化学式为______。
(2)写出上述流程图中的“氧化”的离子方程式:______________该设计存在缺陷,请提出改进意见;________
(3)加入试剂Y的目的是为了调节溶液的pH,若Y为氧化物,写出调节pH的离子方程式:_____
(4)已知常温下Fe(OH)3和Mg(OH)2的Ksp分别为8.0×10-38、1.0×10-11,向浓度均为0.1mol/L的FeCl3、MgCl2 的混合溶液中加入碱液,要使Fe3+ 刚好完全沉淀的pH为____,而Mg2+刚好开始要沉淀的pH为__________。(已知lg 2=0.3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的分类或归类正确的是
A.化合物:CaCl2、烧碱、聚苯乙烯、HD
B.电解质:明矾、胆矾、冰醋酸、硫酸钡
C.同系物:CH2O2、C2H4O2、C3H6O2、C4H8O2
D.同位素:![]() 、
、![]() 、
、![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸氢铵是我国主要的氮肥品种之一,在贮存和运输过程中容易挥发损失。为了鉴定其质量和确定田间施用量,必须测定其含氮量。
I.某学生设计了一套以测定二氧化碳含量间接测定含氮量的方法。将样品放入圆底烧瓶中:
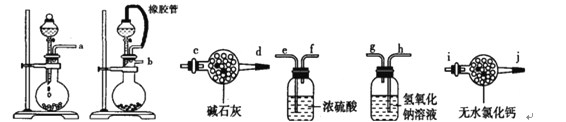
(1)请选择必要地装置,按气流方向连接顺序为________________。
(2)分液漏斗中的液体最适合的是___________。
A.稀盐酸 B.稀硫酸 C.浓硝酸 D.氢氧化钠
(3)连在最后的装置起到的作用____________________________________。
Ⅱ.如果氮肥中成分是(NH4)2SO4,则可以用甲醛法测定含氮量。甲醛法是基于甲醛与一定量的铵盐作用,生成相当量的酸,反应为2(NH4)2SO4+6HCHO→(CH2)6N4 +2H2SO4 + 6H2O,生成的酸再用氢氧化钠标准溶液滴定,从而测定氮的含量。步骤如下:
(4)用差量法称取固体(NH4)2SO4样品0.6g于烧杯中,加入约30mL蒸馏水溶解,最终配成100mL溶液。用________准确取出20.00mL的溶液于锥形瓶中,加入18%中性甲醛溶液5mL,放置5min后,加入1~2滴________指示剂(已知滴定终点的pH约为8.8),用浓度为0.08mol/L氢氧化钠标准溶液滴定,读数如下表:
滴定次数 | 滴定前读数(mL) | 滴定后读数(mL) |
1 | 1.20 | 16.21 |
2 | 3.00 | 18.90 |
3 | 4.50 | 19.49 |
达滴定终点时的现象为______________________________,由此可计算出该样品中的氮的质量分数为_________________。
(5)在滴定实验结束后发现滴定用的滴定管玻璃尖嘴内出现了气泡,滴定开始时无气泡,则此实验测定的含氮量比实际值________(填“偏大”“偏小”或“无影响”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com