
| A£® | SeO2”¢H2SO4£ØÅØ£©”¢I2µÄŃõ»ÆŠŌÓÉĒæµ½ČõµÄĖ³ŠņŹĒH2SO4£ØÅØ£©£¾SeO2£¾I2 | |
| B£® | ¢ŁÖŠSeŹĒŃõ»Æ²śĪļ£¬I2ŹĒ»¹Ō²śĪļ | |
| C£® | ·“Ó¦¢ŁÖŠKIŹĒŃõ»Æ¼Į£¬SeO2ŹĒ»¹Ō¼Į | |
| D£® | ·“Ó¦¢ŁÖŠĆæÓŠ1.0mol I2Éś³É£¬×ŖŅʵē×ÓŹżÄæĪŖ4NA |
·ÖĪö ·“Ó¦¢ŁSeO2+4KI+4HNO3=Se+2I2+4KNO3+2H2OÖŠ£¬SeŌŖĖŲµÄ»ÆŗĻ¼Ū½µµĶ£¬±»»¹Ō£¬IŌŖĖŲµÄ»ÆŗĻ¼ŪÉżøߣ¬±»Ńõ»Æ£»·“Ó¦¢ŚSe+2H2SO4£ØÅØ£©=2SO2”ü+SeO2+2H2OÖŠ£¬SeŌŖĖŲ»ÆŗĻ¼ŪÉżøߣ¬±»Ńõ»Æ£¬SŌŖĖŲ»ÆŗĻ¼Ū½µµĶ£¬±»»¹Ō£¬øł¾ŻŌŚĶ¬Ņ»·“Ó¦ÖŠŃõ»Æ¼ĮŃõ»ÆŠŌ“óÓŚŃõ»Æ²śĪļŃõ»ÆŠŌÅŠ¶ĻŃõ»ÆŠŌĒæČõ£¬½įŗĻŌŖĖŲ»ÆŗĻ¼ŪµÄ±ä»Æ¼ĘĖć×ŖŅʵē×ÓŹżÄ森
½ā“š ½ā£ŗA£®ŌŚĶ¬Ņ»·“Ó¦ÖŠŃõ»Æ¼ĮŃõ»ÆŠŌ“óÓŚŃõ»Æ²śĪļŃõ»ÆŠŌ£¬Ōņøł¾Ż¢ŁæÉÖŖŃõ»ÆŠŌ£ŗSeO2£¾I2£¬¢ŚÖŠ·½æņÖŠĪļÖŹÓ¦ĪŖSeO2£¬Ńõ»ÆŠŌ£ŗH2SO4£ØÅØ£©£¾SeO2£¬ŌņŃõ»ÆŠŌÓÉĒæµ½ČõµÄĖ³ŠņŹĒH2SO4£ØÅØ£©£¾SeO2£¾I2£¬¹ŹAÕżČ·£»
B£®·“Ó¦¢ŁSeO2+4KI+4HNO3=Se+2I2+4KNO3+2H2OÖŠ£¬SeŌŖĖŲµÄ»ÆŗĻ¼Ū½µµĶ£¬±»»¹Ō£¬IŌŖĖŲµÄ»ÆŗĻ¼ŪÉżøߣ¬±»Ńõ»Æ£¬ŌņSeŹĒ»¹Ō²śĪļ£¬I2ŹĒŃõ»Æ²śĪļ£¬¹ŹB“ķĪó£»
C£®·“Ó¦¢ŁÖŠKIŹĒ»¹Ō¼Į£¬SeO2ŹĒŃõ»Æ¼Į£¬¹ŹC“ķĪó£»
D£®øł¾Ż»ÆŗĻ¼ŪµÄ±ä»ÆæÉÖŖ£¬·“Ó¦¢ŁÖŠĆæÓŠ1molI2Éś³É£¬×ŖŅʵĵē×ÓŹżÄæÓ¦ĪŖ1mol”Į2”Į£Ø1-0£©=2mol£¬¹ŹD“ķĪó£®
¹ŹŃ”A£®
µćĘĄ ±¾Ģāæ¼²éŃõ»Æ»¹Ō£¬ĪŖøßĘµæ¼µć£¬²ąÖŲӌѧɜµÄ·ÖĪöÄÜĮ¦ŗĶ¼ĘĖćÄÜĮ¦£¬ĢāÄæÄѶČÖŠµČ£¬×¢Ņāøł¾ŻŌŚĶ¬Ņ»·“Ó¦ÖŠŃõ»Æ¼ĮŃõ»ÆŠŌ“óÓŚŃõ»Æ²śĪļŃõ»ÆŠŌĄ“ÅŠ¶ĻŃõ»ÆŠŌµÄĒæČõ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ijĶéĢžµÄĻµĶ³ĆüĆū£ŗ3-¼×»ł-2-ŅŅ»łĪģĶé | |
| B£® | °±»łŅŅĖįŗĶĻõ»łŅŅĶ黄ĪŖĶ¬·ÖŅģ¹¹Ģå | |
| C£® | ŅŅĻ©ŗĶ1£¬3-¶”¶žĻ©ŹōÓŚĶ¬ĻµĪļCH3 | |
| D£® | 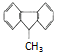 Ņ»ĀČ“śĪļÓŠ5ÖÖ Ņ»ĀČ“śĪļÓŠ5ÖÖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĀČŅŅĻ©ŗĶäåŅŅĶé¾łÄÜ·¢Éś¼Ó³É·“Ó¦ | |
| B£® | »ØÉśÓĶŗĶÓńĆ×ÓĶ¶¼ŹĒæÉŌķ»ÆµÄ±„ŗĶõ„Ąą | |
| C£® | ĢģČ»ĘųŗĶĖ®ĆŗĘųµÄÖ÷ŅŖ³É·Ö¶¼ŹĒĢžĄą | |
| D£® | ·Ö×ÓŹ½ĪŖC10H14µÄµ„Č”“ś·¼Ģž£¬ĘäæÉÄܵĽį¹¹ÓŠ4ÖÖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1£ŗ1 | B£® | 1£ŗ2 | C£® | 1£ŗ3 | D£® | 1£ŗ4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ģ¼ĖįøĘÓėŃĪĖį·“Ó¦ CO32-+2H+ØTCO2”ü+H2O | |
| B£® | ĮņĖįŗĶĀČ»Æ±µČÜŅŗ·“Ó¦ Ba2++SO42-ØTBaSO4”ż | |
| C£® | ĒāŃõ»ÆÄĘŗĶÉŁĮæĮņĖį·“Ó¦ 2OH-+H2SO4ØTSO42-+2H2O | |
| D£® | Ģś¶¤·ÅČėĮņĖįĶČÜŅŗÖŠ Fe+3Cu2+ØT2Fe3++3Cu |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
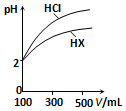 Ė®ŹĒ¼«ČõµÄµē½āÖŹ£¬øıäĪĀ¶Č»ņ¼ÓČėijŠ©µē½āÖŹ»įÓ°ĻģĖ®µÄµēĄė£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
Ė®ŹĒ¼«ČõµÄµē½āÖŹ£¬øıäĪĀ¶Č»ņ¼ÓČėijŠ©µē½āÖŹ»įÓ°ĻģĖ®µÄµēĄė£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com