
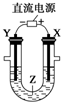
| A. | 氯碱工业中,X电极上反应式是4OH--4e-═2H2O+O2↑ | |
| B. | 电解精炼铜时,Z溶液中的Cu2+浓度不变 | |
| C. | 在铁片上镀铜时,Y是纯铜 | |
| D. | 制取金属镁时,Z是熔融的氯化镁 |
分析 A、依据电源正负极确定电解池中x为阳极,氯碱工业电解的是饱和食盐水,溶液中氯离子失电子;
B、电解精炼铜溶液中铜离子浓度减少;
C、铁片上镀铜时阴极为铁片;
D、金属镁是电解熔融的氯化镁制得的.
解答 解:A、氯碱工业中,X电极连接电源正极,为电解池的阳极,溶液中的氯离子失电子生成氯气,2Cl--2e-=Cl2↑,故A错误;
B、电解精炼铜时,粗铜做阳极含有铁、锌、镍等活泼金属,精铜做阴极,电解过程中电子守恒,溶液中的铜离子浓度减少,故B错误;
C、在铁片上镀铜时,铁片做阴极为Y电极,铜做阳极为X电极,故C错误;
D、金属镁是电解熔融的氯化镁,镁阴极得到电子析出,水溶液中镁离子不放电,故D正确;
故选D.
点评 本题考查了氯碱工业,电解精炼铜,电镀铜,冶炼镁等几种工业制备的原理应用,熟练掌握电解原理是解题关键.


 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:高中化学 来源: 题型:选择题
| A. | 溴离子具有氧化性 | B. | 溴离子的还原性比氯离子弱 | ||
| C. | 该反应属于复分解反应 | D. | 氯气的氧化性比溴单质强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 熔化的铝滴落 | |
| B. | 熔化的铝开始剧烈燃烧 | |
| C. | 熔化的铝不滴落,好像有一层膜兜着 | |
| D. | 熔化的铝火星四溅 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 定容摇匀后,有少量溶液外流,则NaClO的物质的量浓度偏小 | |
| B. | 容量瓶用蒸馏水洗净后可以不烘干即能用于溶液的配制 | |
| C. | 所配得的NaClO消毒液在空气中光照,久置后溶液中NaClO的物质的量浓度减小 | |
| D. | 所配制NaClO溶液的物质的量浓度为2.4 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠和钾合金在常温下是液体,可用于快中子反应堆的热交换剂 | |
| B. | 镁合金密度小但强度大,大量用于火箭、飞机的部件等 | |
| C. | 高炉炼铁得到含碳0.03%~2%的生铁 | |
| D. | 生物炼铜是利用能耐受铜盐毒性的细菌将不溶性硫化铜转化为可溶性铜盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | +1 | B. | +2 | C. | +4 | D. | +5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 镭比钙的金属性更强 | B. | 单质能与水反应,放出氢气 | ||
| C. | 其氢氧化物呈两性 | D. | 其碳酸盐难溶于水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com