
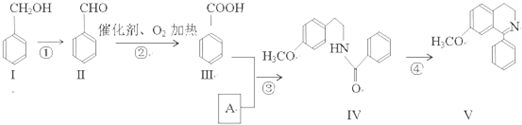
 ,
, ;
; ,
, ;
; ,
, ;
; ,故答案为:
,故答案为: .
.


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案科目:高中化学 来源: 题型:
| A、元素A所形成的氧化物只有一种 |
| B、元素B的最高价氧化物对应的水化物为强酸 |
| C、元素C、D、E的最高价氧化物对应的水化物两两之间可发生反应 |
| D、氢化物的稳定性:A>B |
查看答案和解析>>
科目:高中化学 来源: 题型:

| ||
| H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、离子半径:W>X>Z |
| B、原子半径:Z>X>Y |
| C、单质的熔点:W>Z>Y |
| D、最高正价:Z>W>X |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 浓度 时间/min 物质 | 0 | 1 | 2 | 3 | 4 |
| CH4 | 0.2mol?L-1 | 0.13mol?L-1 | 0.1mol?L-1 | 0.1mol?L-1 | 0.09moˉL-1 |
| H2 | 0mol?L-1 | 0.2mol?L-1 | 0.3mol?L-1 | 0.3mol?L-1 | 0.33mol?L-1 |
| n(CH4) |
| n(H2O) |

查看答案和解析>>
科目:高中化学 来源: 题型:


 ,该物质在NaOH水溶液中加热反应,可生成有机物的结构简式为
,该物质在NaOH水溶液中加热反应,可生成有机物的结构简式为 的合成路线流程图(无机试剂可任选).合成路线流程图示例如下:CH2=CH2
的合成路线流程图(无机试剂可任选).合成路线流程图示例如下:CH2=CH2| HBr |
| NaOH溶液 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、萃取、分液前需对分液漏斗检漏 |
| B、制取硝基苯时,采取水浴加热,将温度计插入水浴液中 |
| C、点燃甲烷、氢气、乙烯、CO等可燃性气体前必须验纯 |
| D、液溴保存时液面覆盖一层水,装在带橡胶塞的细口试剂瓶中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com