
【题目】实验室需要0.1mol·L-1NaOH溶液500mL。根据溶液的配制情况回答下列问题。
(1)在如图所示仪器中,配制上述溶液肯定不需要的是________(填字母),除图中已有仪器外,配制上述溶液还需要的玻璃仪器是________________________________________。
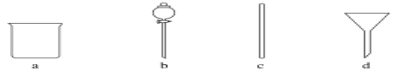
(2)配制时,正确的操作顺序是(用字母表示,每个操作只用一次)______________。
A.用少量水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
B.在盛有NaOH固体的烧杯中加入适量水溶解
C.将烧杯中已冷却的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,反复上下颠倒,摇匀
E.改用胶头滴管加水,使溶液凹液面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线1~2cm处
(3)实验两次用到玻璃棒,其作用分别是:先用于___________、后用于____________。
(4) 根据计算用托盘天平称取NaOH固体的质量为________g。
(5)分析下列操作对所配制溶液浓度的影响(填“偏高”、“偏低”或“无影响”)。
①转移液体过程中有少量液体溅出:_______________。
②定容时仰视刻度线:_______。 ③容量瓶洗净后,未经干燥处理:________。
【答案】bd 500ml容量瓶、胶头滴管 BCAFED 搅拌,加速溶解 引流 2.0 偏低 偏低 不变
【解析】
(1)根据配制一定物质的量浓度溶液用到仪器进行分析;
(2)依据配制一定物质的量浓度溶液的步骤(计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶等)进行排序;
(3)溶解过程中用玻璃棒不断搅拌加速固体溶解,移液时用玻璃棒引流;
(4)依据m=cVM计算需要溶质的质量;
(5)利用公式![]() 进行分析。
进行分析。
(1)配制一定物质的量浓度溶液用到的仪器有:托盘天平、药匙、烧杯、玻璃棒、500mL容量瓶、胶头滴管,不需要的仪器有漏斗和分液漏斗,还需用到的玻璃仪器是500ml容量瓶、胶头滴管,故答案为:bd;500ml容量瓶、胶头滴管;
(2)配制一定物质的量浓度溶液一般步骤:计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶等,所以正确的顺序为:BCAFED,故答案为:BCAFED;
(3)溶解过程中用玻璃棒不断搅拌加速固体溶解,移液时用玻璃棒引流,
故答案为:搅拌,加速溶解;引流;
(4) 用托盘天平称取NaOH固体的质量为0.1mol·L-1×0.500L×40g/mol=2.0g,故答案为:2.0;
(5)①转移液体过程中有少量液体溅出:n减小,V不变,则c偏低,故答案为:偏低;
②定容时仰视刻度线:n不变,V偏大,则c偏低,故答案为:偏低;
③容量瓶洗净后,未经干燥处理:n不变,V不变,则c不变,故答案:不变。


科目:高中化学 来源: 题型:
【题目】加碘食盐是含KIO3的食盐,其中KIO3可由反应KI+3Cl2+3H2O=KIO3+6HCl制取。市面上销售的加碘食盐中的碘元素含量为20~50mg/kg。请计算:制取1000kg含碘元素25.4mg/kg的加碘食盐,需要消耗Cl2的体积是多少___?(标准状况)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含有11.2 g KOH的稀溶液与1 L 0.1 molL﹣1的H2SO4溶液反应,放出11.46 kJ的热量,下列热化学方程式正确的是
A. KOH(aq)+![]() H2SO4(aq) ===
H2SO4(aq) === ![]() K2SO4(aq)+H2O(l) ΔH =-11.46 kJmol﹣1
K2SO4(aq)+H2O(l) ΔH =-11.46 kJmol﹣1
B. 2KOH(aq)+H2SO4(aq) === K2SO4(aq)+2H2O(l) ΔH =-11.46 kJmol﹣1
C. 2KOH(aq)+H2SO4(aq) === K2SO4(aq)+2H2O(l) ΔH =+114.6 kJmol﹣1
D. KOH(aq)+![]() H2SO4(aq) ===
H2SO4(aq) === ![]() K2SO4(aq)+H2O(l) ΔH =-57.3 kJmol﹣1
K2SO4(aq)+H2O(l) ΔH =-57.3 kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用Na2O2与H2O反应快速制取少量O2.用下面装置制取O2并演示Na在O2中的燃烧实验.

请回答下列问题:
(1)写出A装置中反应的化学方程式_____.
(2)B装置中盛放的试剂是_____.
(3)D装置中盛放的试剂是_____,其作用是_____.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】混合物分离和提纯常用下图装置进行,按要求回答下列问题:
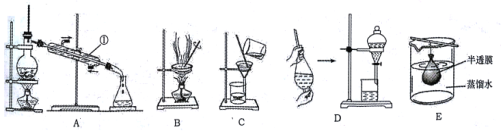
(1)仪器①的名称__________。
(2)除去澄清石灰水中悬浮的CaCO3颗粒应选用_______(填字母,下同)。
(3)分离乙酸(沸点118℃)和乙酸乙酯(沸点77.1℃)的混合物应选用_______。
(4)用CCl4提取碘水中的碘单质应选用_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把0.6molX气体和0.4molY气体混合于容积为2L的容器中,使其发生如下反应:3X(g)+Y(g)![]() nZ(g)+2W(g)。5min末生成0.2molW,若测知以Z浓度变化表示的平均反应速率为0.01mol/( L· min),则n的值为
nZ(g)+2W(g)。5min末生成0.2molW,若测知以Z浓度变化表示的平均反应速率为0.01mol/( L· min),则n的值为
A. 1B. 2C. 3D. 4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究和开发CO、CO2的应用及水体污染的治理是化学工作者研究的重要课题。
(1)水体常见污染物之一的氨氮主要指游离氨或铵盐,可以通入一定量的氯气,利用产生的HClO除去。已知: NH4++HClO=NH2Cl+H++H2O;ΔH=a kJ·mol-1
NH4++4HClO=NO3- +6H++4Cl-+H2O;ΔH=b kJ·mol-1。
2NH2Cl+HClO=N2+H2O+3H++3Cl-;ΔH=c kJ·mol-1
则2NH4++3HClO=N2+3H2O+5H++3Cl-;ΔH=_____ kJ·mol-1
(2)将CO2与金属钠组合设计成Na-CO2电池,很容易实现可逆的充、放电反应,该电池反应为4Na+3CO2![]() 2Na2CO3+C。放电时当电路中转移1mol电子时被还原的CO2的质量为_____;充电时,阳极的反应式为________
2Na2CO3+C。放电时当电路中转移1mol电子时被还原的CO2的质量为_____;充电时,阳极的反应式为________
(3)废水中重金属离子常用沉淀法除去,已知Ksp(NiS)=1.1×10-21,Ksp(CuS)=1.3×10-36,国家规定的排放标准:镍低于1.1×10-5 mol·L-1,铜低于7.8×10-5 mol·L-1。则需要控制溶液中S2-的浓度不低于_____________mol·L-1。
(4)NO易被O2氧化为NO2。其他条件不变时,NO的氧化率α(NO)与温度、压强的关系如图1所示(p1线在p2的上方)则p1__p2(填“>”、“<”或“=”);温度高于800℃时,α(NO)几乎为0的原因是____

(5)环境中的有害物质常通过转化为CO2来降低污染,TiO2是一种性能优良的半导体光催化剂,能有效地将有机污染物转化为CO2等小分子物质。下图2为在TiO2的催化下,O3降解CH3CHO的示意图,则该反应的化学方程式为_____。

(6)用新型钛基纳米PbO2作电极可将苯、酚类等降解为CO2 和H2O。该电极可通过下面过程制备:将钛基板用丙酮浸泡后再用水冲洗,在钛板上镀上一层铝膜。用它做阳极在草酸溶液中电解,一段时间后,铝被氧化为氧化铝并同时形成孔洞。再用Pb(NO3)2溶液处理得纳米PbO2,除去多余的氧化铝,获得钛基纳米PbO2电极。电解时,电流强度和基板孔洞深度随时间变化如上图3所示,氧化的终点电流强度突然增加,其可能的原因是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电浮选凝聚法是工业上采用的一种污水处理方法,即保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3胶体,Fe(OH)3胶体具有吸附作用,可吸附水中的污物而使其沉淀下来,起到净水的作用,其原理如图所示。下列说法正确的是
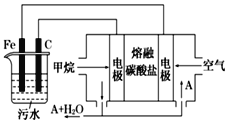
A. 石墨电极上发生氧化反应
B. 根据图示,物质A为CO2
C. 为增强污水的导电能力,可向污水中加入适量乙醇
D. 甲烷燃料电池中CO32-向空气一极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】茅台酒中存在少量具有凤梨香味的物质X,其结构如下图所示,下列说法正确的是
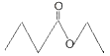
A. X难溶于乙醇
B. 酒中少量的丁酸能抑制X的水解
C. X完全燃烧后生成CO2和H2O的物质的量比为1:2
D. 分子式为![]() 且官能团与X相同的物质共有5种
且官能团与X相同的物质共有5种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com