
研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2-CaO作电解质,利用如图所示装置获得金属钙,并以钙为还原剂,还原二氧化钛制备金属钛。下列正确的是:
A、由TiO2制得1mol 金属Ti ,理论上外电路转移2NA电子
B、阳极的电极反应式为:C + 2O2- - 4e- == CO2↑
C、若用铅蓄电池作该装置的供电电源,“ +”接线柱应连接Pb电极
D、在制备金属钛前后,整套装置中CaO的总量减少
 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案科目:高中化学 来源: 题型:
在2升的密闭容器中,发生以下反应:2A(g)+ B(g) 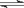 2C(g)+D(g) 。若最初加入的A和B都是4 mol,在前10秒钟A的平均反应速度为0.12 mol/(L·s),则10秒钟时,容器中B的物质的量是
2C(g)+D(g) 。若最初加入的A和B都是4 mol,在前10秒钟A的平均反应速度为0.12 mol/(L·s),则10秒钟时,容器中B的物质的量是
A. 1.6 mol B. 2.8 mol C. 2.4 mol D. 1.2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
实验探究是学习化学的一种重要方法,某实验小组的同学利用下列装置完成了一些常见气体的制备以及相关物质性质探究(夹持装置及连接用的橡胶管已省略,其中装置E有多个供使用)。

可供选择的液体试剂及固体药品:
| 液体试剂 | 固体药品 |
| 稀硫酸、稀盐酸、稀硝酸、NaOH溶液、浓氨水、5%H2O2溶液、浓盐酸、饱和食盐水 | CaCO3、CaO、MnO2、KMnO4、CaC2、碱石灰、Cu、Zn、Na2S |
请回答下列问题:
(1)装置B中a仪器的名称________。
(2)可由A装置制取相对分子质量小于32的气体有________(任意写2种)。
(3)已知氨气和氯气在常温下可以发生氧化还原反应,A、B分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气的反应装置,则仪器的连接顺序是A→________→C←________←________←B。写出装置B(无需加热)中反应的离子方程式_________________________________________________。
(4)完成上述实验需选用仪器D和E,D中选用( )、E中选用( )(填写序号)
a.无水氯化钙 b.饱和碳酸氢钠溶液
c.饱和食盐水 d.五氧化二磷
e.碱石灰 f.浓硫酸
(5)C内出现大量白烟,另一种生成物常用作食品包装袋内的保护气,请写出反应的化学方程式__________________________________________。
(6)请你利用所学化学知识设计一个实验方案检验白烟物质中的离子:_________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
取相同体积的KI、Na2S、FeBr2溶液,分别通入足量的Cl2,当反应恰好完成时,消耗Cl2的体积相同(同温、同压条件下),则KI、Na2S、FeBr2溶液的物质的量浓度之比是( )
A.1:1:2 B.2:1:3 C.6:3:2 D.3:2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
在由Fe、FeO和Fe2O3组成的混合物中加入100 mL 2 mol / L的盐酸,恰好使混合物完全
溶解,并放出448 mL气体(标准状况),此时溶液中无Fe3+离子,则下列判断正确的是( )
A.混合物里3种物质反应时消耗盐酸的物质的量之比为1:1:3
B.反应后所得溶液中的Fe2+离子与Cl-离子的物质的量浓度之比为1:3(不考虑Fe2+水解)
C.混合物里,FeO的物质的量无法确定,但Fe比Fe2O3的物质的量多
D.混合物里,Fe2O3的物质的量无法确定,但Fe比FeO的物质的量多
查看答案和解析>>
科目:高中化学 来源: 题型:
能正确表示下列反应的离子方程式的是
A、NH4HSO3溶于过量的NaOH溶液中:HSO3-+OH-=SO32-+H2O
B、向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-
C、Fe3O4与稀硝酸反应:Fe3O4+8H+=2Fe3++Fe2++4H2O
D、酸性KMnO4溶液与双氧水溶液反应:2MnO4- +5H2O2+6H+=2Mn2++5O2 ↑+8H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
下列与化学概念有关的说法正确的是
A.化合反应均是氧化还原反应 B.金属氧化物均为碱性氧化物
C.催化剂能改变可逆反应达到平衡的时间 D.石油是混合物,其分馏产品汽油为纯净物
查看答案和解析>>
科目:高中化学 来源: 题型:
(一)将一小块钠用小刀切开,可以看到表面光亮,但很快变暗,该反应的化学方程为___________________________________________________________,
若将钠块放到石棉网上加热会生成淡黄色固体,该反应的化学方程式为:___________________________________________________________________,
该固体遇水会有无色无味的气体生成,该反应的化学方程式为:
___________________________________________________________________;
通常情况下,为了防止污染环境,在做完实验后,多余的氯气应用NaOH溶液吸收,其化学方程式为 ;
工业上用氯气和石灰乳反应制漂白粉,漂白粉的有效成分是 ,
漂白粉长时期露至在空气中会失效,用化学方程式表示其失效的原因:
, 。
(二)某兴趣小组为探究Na2O2滴入酚酞试液中时溶液颜色变化的原因,设计如下方案。将2药匙Na2O2加入滴有3~4滴酚酞试剂的蒸馏水(10ml)中,发现有如下现象:
①立即有大量气泡生成。
②无色透明的酚酞溶液迅速变红,振荡后,溶液中的红色褪去,又变为无色。
③反应放出大量的热量,试管壁手触感觉很烫。
请回答:
(1)该兴趣小组同学认为酚酞试液颜色变化的为:
假设①: 。
假设②:可能是反应放出的热量,使红色消失。
假设③:可能是Na2O2与水反应生成的NaOH溶液浓度太大,使得酚酞变性,不显颜色。
(2)验证假设②,设计补充实验:取滴加酚酞的稀NaOH溶液加热,若红色消失,则证明假设②成立;若红色不消失,则假设②不成立。
(3)验证假设③,设计补充实验: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
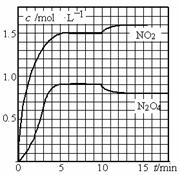 向2L的密闭容器中充入7.6mol NO和3.8mol O2,发生如下反应:
向2L的密闭容器中充入7.6mol NO和3.8mol O2,发生如下反应:
①2NO(g)+O2(g) 2NO2(g)
2NO2(g)
②2NO2(g) N2O4(g)
N2O4(g)
测得NO2和N2O4的浓度变化如图所示,0~10min维持容器温度为T1℃, 10min后升高并维持容器的温度为T2℃。下列说法正确的是( )
A.前5min反应的平均速率v(N2O4)=0.18mol·L-1·s-1
B.T1℃时反应②的化学平衡常数K=0.6
C.反应①、②均为吸热反应
D.若起始时向该容器中充入3.6mol NO2和2. 0mol N2O4,T1℃达到平衡时,N2O4的转化率为10%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com