
【题目】下列判断中,正确的是( )
A.泡沫灭火器的灭火原理:2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2↑
B.将CH3COONa溶液从20℃升温至30℃,溶液中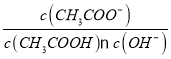 增大
增大
C.某物质的溶液中由水电离出的c(H+)= 1×10-a mol/L,若a>7时,则该溶液的pH一定为14-a
D.已知25℃时NH4CN显碱性,则25℃时的电离常数K(NH3·H2O)>K(HCN)
【答案】D
【解析】
A.泡沫灭火器中盛装的反应物是NaHCO3溶液和Al2(SO4)3溶液,利用两者的双水解反应生成CO2,其灭火原理为Al3++3HCO3-=Al(OH)3↓+3CO2↑,故A错误;
B.CH3COONa溶液中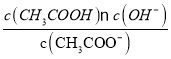 =Kh,升高温度促进水解,Kh增大,所以
=Kh,升高温度促进水解,Kh增大,所以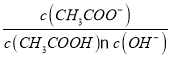 减小,故B错误;
减小,故B错误;
C.某物质的溶液中由水电离出的c(H+)=1×10-amol/L,若a>7时,说明水的电离被抑制,酸或碱都能抑制水的电离,所以溶液的pH可以是a,也可以是14-a,故C错误;
D.已知25℃时NH4CN水溶液显碱性,说明CN-水解程度大于NH4+,HCN电离程度小于NH3H2O电离程度,则25℃时的电离常数K(NH3H2O)>K(HCN),故D正确;
故答案为D。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】导电性实验可以作为研究电解质电离本质及反应机理的有效方法。
(1)在如图所示的装置里,若灯泡亮,广口瓶内的物质A可以是__(填序号)。
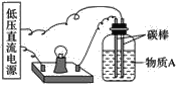
①干燥的氯化钠晶体 ②干燥的氢氧化钠晶体 ③蔗糖晶体 ④酒精 ⑤氯化钠溶液 ⑥氢氧化钠溶液 ⑦稀盐酸 ⑧硫酸铜溶液
(2)在电解质溶液的导电性装置(如图所示)中,若向某一电解质溶液中逐滴加入另一溶液时,则灯泡由亮变暗,至熄灭后又逐渐变亮的是__(填字母)。
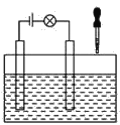
A.盐酸中逐滴加入食盐溶液 B.硫酸中逐滴加入氢氧化钠溶液
C.石灰乳中滴加稀盐酸 D.硫酸中逐滴加入氢氧化钡溶液
(3)已知:CO2+Ca(OH)2=CaCO3↓+H2O,CaCO3+CO2+H2O=Ca(HCO3)2,且Ca(HCO3)2易溶于水。若在(2)题图中,电解质溶液为Ca(OH)2溶液,向溶液中逐渐通入CO2。则:下列四个图中,__(填字母)能比较准确地反映出溶液的导电能力和通入CO2气体量的关系(x轴表示CO2通入的量,y轴表示导电能力)。
A.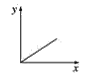 B.
B.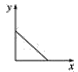 C.
C.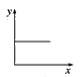 D.
D.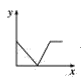
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组热化学方程式中,化学反应的ΔH前者大于后者的是( )
①C(s)+O2(g)= CO2(g)ΔH1;C(s)+ ![]() O2(g)= CO(g)ΔH2
O2(g)= CO(g)ΔH2
②S(s)+O2(g)= SO2(g)ΔH3;S(g)+O2(g)=SO2(g)ΔH4
③H2(g)+ ![]() O2(g)=H2O(l)ΔH5;2H2(g)+O2(g)= 2H2O(l)ΔH6
O2(g)=H2O(l)ΔH5;2H2(g)+O2(g)= 2H2O(l)ΔH6
④CaCO3(s)= CaO(s)+CO2(g)ΔH7;CaO(s)+H2O(l)= Ca(OH)2(s)ΔH8
A.①B.④C.②③④D.①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知拆开![]() 键、
键、![]() 键、
键、![]() 键分别需要吸收的能量为
键分别需要吸收的能量为![]() 、
、![]() 、
、![]() 。则由
。则由![]() 和
和![]() 反应生成1molHCl需要_______
反应生成1molHCl需要_______![]() 填“放出”或“吸收”
填“放出”或“吸收”![]() _________
_________![]() 的热量。
的热量。
(2)H2可以在![]() 中安静地燃烧。甲、乙两图中,能表示该反应能量变化的是图_____
中安静地燃烧。甲、乙两图中,能表示该反应能量变化的是图_____![]() 填“甲”或“乙”
填“甲”或“乙”![]() 。
。
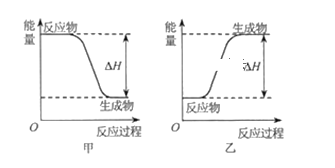
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O。
(1)参加反应的HNO3和作为氧化剂的HNO3的个数比为________。
(2)若有64 g Cu被氧化,则被还原的HNO3的质量是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示的是纯净物、单质、化合物、含氧化合物、氧化物、碱之间的包含、不包含关系,若整个大圆圈代表纯净物,则下列选项中,能正确指出①、②、③、④、⑤所属物质类别的是( )
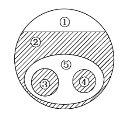
A. ①单质、③化合物
B. ②碱、⑤氧化物
C. ④碱、⑤含氧化合物
D. ④含氧化合物、③氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作、现象和所得结论均正确的是( )
选项 | 实验内容 | 实验结论 |
A | 向盛有5mL0.005mol/L FeCl3溶液中加入5mL0.01mol/LKSCN溶液,再继续加入少量KCl固体,观察现象 | 证明溶液存在平衡: FeCl3+3KSCNFe(SCN)3+3KCl |
B | 取两只试管,分别加入等体积等浓度的双氧水,然后试管①中加入0.01mol/LFeCl3溶液2mL,试管②中加入0.01mol/LCuCl2溶液2mL,试管①产生气泡快 | 加入FeCl3时,双氧水分解反应的活化能较大 |
C | 检验FeCl3溶液中是否含有Fe2+时,将溶液滴入酸性KMnO4溶液,溶液紫红色褪去 | 不能证明溶液中含有Fe2+ |
D | 取两只试管分别加入4mL0.01mol/LKMnO4酸性溶液,然后向一只试管中加入0.01mol/L H2C2O4溶液2mL,向另一只试管中加入0.01mol/L H2C2O4溶液4mL,第一只试管中褪色时间长 | H2C2O4浓度越大,反应速率越快 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某废催化剂含SiO2、ZnO、ZnS和CuS。实验室从该废催化剂中回收锌和铜的一种流程如下图所示。
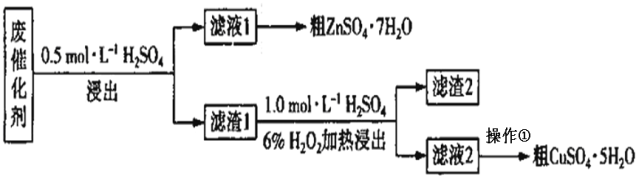
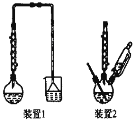
浸出使用的装置如图所示。回答下列问题:
 蒸发浓缩、冷却结晶蒸发浓缩、冷却结晶
蒸发浓缩、冷却结晶蒸发浓缩、冷却结晶
(1)第一次浸出必须选用装置 _______(填“1”或“2”),原因是 ________。滤渣1的主要成分有_______。
(2)第二次浸出时生成单质硫,写出反应的离子方程式:_______________。该步骤即使加热温度不高也可能会有副反应发生,产物之一是空气的主要成分,分析可能原因是_____________________ 。
(3)从滤液2中得到CuSO4·5H2O的操作是 __________ 、过滤、洗涤。
(4)下列叙述中涉及到与该流程中的“操作①”相同操作的是_____________ 。
A.《肘后备急方》中治疟疾:“青蒿一握,以水升渍,绞取汁,尽服之”
B.《本草衍义》中精制砒霜:“将生砒就置火上,以器覆之,令砒烟上飞着覆器”
C.《开宝本草》中获取硝酸钾:“冬月地上有霜,扫取以水淋汁后,乃煎炼而成”
D. 《本草纲目》中烧酒的制造工艺:“凡酸坏之酒,皆可蒸烧”
(5)若该废催化剂中含12.8%的CuS,实验中称取15.0g废催化剂最终得到3.0gCuSO4·5H2O,则铜的回收率为 __________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Weiss利用光敏剂QD制备2—环已基苯乙烯(c)的过程如图。下列说法不正确的是( )
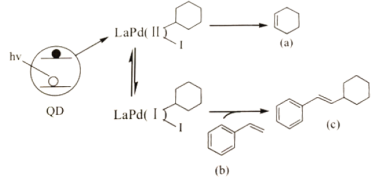
A.a的二氯代物有3种
B.1molb完全燃烧消耗10molO2
C.c具有顺式和反式2种结构
D.a、b、c均能使溴水和稀高锰酸钾溶液褪色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com