
| A. | 向苯酚浊液中滴加少量饱和Na2CO3溶液,浊液变澄清,证明结合质子的能力:CO32->C6H5O- | |
| B. | 配制Fe(NO3)2溶液时加入适量的硝酸,可抑制Fe2+水解 | |
| C. | 测定相同温度下相同浓度的碳酸钠和亚硫酸钠溶液的pH,前者大于后者,证明元素的非金属性:C<S | |
| D. | 用激光笔照射蛋白质溶液、硅酸溶胶,可将二者区分开 |
分析 A.向苯酚浊液中滴加少量饱和Na2CO3溶液,浊液变澄清,反应生成苯酚钠、碳酸氢钠;
B.加入适量的硝酸,可氧化亚铁离子;
C.测定相同温度下相同浓度的碳酸钠和亚硫酸钠溶液的pH,可比较碳酸、亚硫酸的酸性,亚硫酸不是最高价含氧酸;
D.蛋白质溶液、硅酸溶胶均为胶体分散系.
解答 解:A.向苯酚浊液中滴加少量饱和Na2CO3溶液,浊液变澄清,反应生成苯酚钠、碳酸氢钠,可知结合质子的能力:CO32->C6H5O-,故A正确;
B.加入适量的硝酸,可氧化亚铁离子,则不能加硝酸抑制水解,故B错误;
C.测定相同温度下相同浓度的碳酸钠和亚硫酸钠溶液的pH,可比较碳酸、亚硫酸的酸性,亚硫酸不是最高价含氧酸,则不能比较C、S的非金属性,故C错误;
D.蛋白质溶液、硅酸溶胶均为胶体分散系,则用激光笔照射不能鉴别,故D错误;
故选A.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、盐类水解、物质的鉴别、非金属性比较、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 高温下0.3molFe与足量水蒸气完全反应,失去的电子数为0.8NA | |
| B. | 常温下,0.2molNaHSO4固体中含有的离子数为0.6NA | |
| C. | 标准状况下,2.24LCCl4中含有极性共价键的数目为0.4NA | |
| D. | 25℃时,pH=12的Ba(OH)2溶液中含有的氢氧根离子数为0.01NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+,Fe2+,Cl-,ClO- | B. | Na+,Cu2+,SO42-,NO3- | ||
| C. | Mg2+,NH4+,SO42-,Cl- | D. | Ba2+,CO32-,NO3-,K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 按系统命名法,化合物  的名称为2,4-二乙基-丙基辛烷 的名称为2,4-二乙基-丙基辛烷 | |
| B. | 若两种二肽互为同分异构体,则二者的水解产物一定不相同 | |
| C. | 分子式为C5H5O2Cl并能与饱和NaHCO3溶液反应产生气体的有机物有(不含立体结构)有15种 | |
| D. | 某有机物的结构简式是  ,该有机物能够发生加成反应、取代反应、缩聚反应和消去反应 ,该有机物能够发生加成反应、取代反应、缩聚反应和消去反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 物质 | 乙炔 | 氧气 | 水 | 二氧化碳 | M |
| 反应前质量/g | 5.2 | 14.4 | 0.4 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 4.0 | m | 2.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
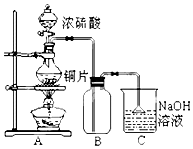 某研究性学习小组的同学为验证浓硫酸与铜能反应而稀硫酸不能,设计了如图所示装置进行探究:将6.4g 铜片和含0.2moL溶质的18.4mol/L浓硫酸放在圆底烧瓶中共热,直到无气体生成为止.(假定在此过程溶液体积不变)
某研究性学习小组的同学为验证浓硫酸与铜能反应而稀硫酸不能,设计了如图所示装置进行探究:将6.4g 铜片和含0.2moL溶质的18.4mol/L浓硫酸放在圆底烧瓶中共热,直到无气体生成为止.(假定在此过程溶液体积不变)| 序号 | 不合理的原因 | 误差 (偏低或偏高) | 改变措施 |
| 方案① | |||
| 方案② |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 A、B、C、D四种元素的核电荷数均小于18,A元素原子核外只有1个电子;B是地壳中含量最多的元素;B、C可形成两种化合物CB和CB2,C的最高正价与最低负价绝对值相等,CB有毒,CB2可用于灭火;D+具有与Ne原子相同的电子层结构.
A、B、C、D四种元素的核电荷数均小于18,A元素原子核外只有1个电子;B是地壳中含量最多的元素;B、C可形成两种化合物CB和CB2,C的最高正价与最低负价绝对值相等,CB有毒,CB2可用于灭火;D+具有与Ne原子相同的电子层结构.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com