
Ϊ��̽��Cl2��SO2ͬʱͨ��H2O�з����ķ�Ӧ��ijУ��ѧ��ȤС��ͬѧ���������ͼ��ʾ��ʵ��װ�á�
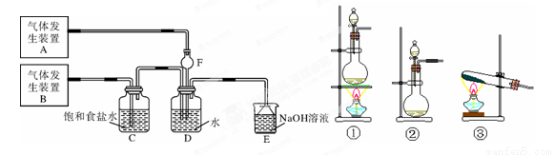
��1������ͬѧΪ����ȡCl2��SO2���壬�ֲ���Na2SO3��70%��Ũ����Ϊԭ����ȡSO2������MnO2��Ũ���ᣨ12mol/L��Ϊԭ����ȡCl2���ڴ�ʵ���У�����װ��BӦѡ������װ���е�___________��ѡ����ţ���F��������_____________��
��2��Dװ������Ҫ��Ӧ�����ӷ���ʽΪ__________________________��
��3��Ϊ����ͨ��Dװ���е�Cl2�Ƿ����������ͬѧȡ����D��Һ�μ���ʢ��������ɫʯ����Թ��У�������___________������Cl2��������ʱE�з��������ӷ�Ӧ����ʽΪ______________________����D�г���__________________ʵ��������������������
��1���٣���ֹ����
��2��Cl2+SO2+2H2O��4H++SO42��+2Cl��
��3��ʯ��ȱ�����ɫ��2OH��+Cl2��Cl��+ClO��+H2O��ʯ����
��������
�����������1��ʵ�����Ʊ������ù�Һ����װ�ã�ѡ��װ�â٣���F�������Ƿ�ֹ��������2��D��ͨ���������Ͷ����������壬�����ķ�ӦΪCl2+SO2+2H2O��2HCl+H2SO4�����ӷ�ӦΪCl2+SO2+2H2O��4H++SO42��+2Cl������3�����������Ƿ������ʯ����Һ������Ϊ�������壬ʯ����Һ�ȱ�죬����������ˮ��Ӧ�����ɴ����ᣬ�����������Ư���ԣ���ʯ�������ɫ�����ӷ���ʽΪ2OH��+Cl2��Cl��+ClO��+H2O�������粻��������ֻ��ʯ����Һ��졣
���㣺���������������������֪ʶ
��������� ����1���ۺ���ʵ�� ����2��±�� ����3������Ԫ�� ��������


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ�����и���3��������黯ѧ�Ծ��������棩 ���ͣ�ѡ����
һ������ȼ�ϵ�صĽṹʾ��ͼ������ʾ�����ڸõ�ص�������ȷ����
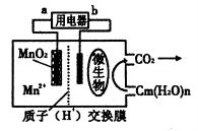
A����ع���ʱ��������a����b
B���������ڵ缫���ŵ�ʱ������ԭ��Ӧ
C���ŵ�����У�H+��������������
D��������ӦʽΪ��MnO2+4H+ +2e�� ===Mn2+ +2 H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�Ĵ�ʡ�����и߶���ѧ��ѧ����ĩ��ѧ�Ծ��������棩 ���ͣ������
��6�֣�ij�¶��£���4.0 mol��HI�������1 L�Ѿ���յĹ̶��ݻ����ܱ������У��������·�Ӧ��2HI(g)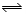 H2(g)��I2(g) ��H��0����һ��ʱ��Ը������ڵ����ʽ��з������õ��������ݣ�
H2(g)��I2(g) ��H��0����һ��ʱ��Ը������ڵ����ʽ��з������õ��������ݣ�
ʱ��/s n /mol | 0 | 40 | 80 | 120 |
n(HI) | 4.0 | 2.8 | b | c |
n(H2) | 0 | a | 1.0 | 1.0 |
��1��a = ��c = ��
��2�������ڸ��¶�ʱ�˷�Ӧ��ƽ�ⳣ��K = ��
��3�������¶Ȳ��䣬120 sʱ��ͨ��2.0 mol��H2�����ٴδﵽƽ��ʱ��HI��ƽ��ת�����Ƕ��٣�����С��Ҫ���ʵ��Ľ�����̣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�Ĵ�ʡ�����и߶���ѧ��ѧ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
�������������˵����ȷ����
A�����ڱ��е�ˮ���Ӽ����������������ܶȴ���Һ̬ˮ
B��������������ͽӽ��е��ˮ��������Է��������ⶨֵ���û�ѧʽ��H2O�������������Է���������
C�����Ӽ�����ͷ������������ʹ�۷е�����
D��ˮ���ȵ��ܸߵ��¶ȶ����Էֽ⣬���������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�Ĵ�ʡ�����и߶���ѧ��ѧ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
NH3��������ˮ����������ص���
A��NH3��ˮ�γɷ��Ӽ���� B��NH3�Ǽ��Է���
C��NH3��Է�������С�����»���С D��NH3����ˮ������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�Ϻ��и�һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ������
ʳ������Ҫ�Ļ���ԭ�ϣ���ⱥ��ʳ��ˮ�Ļ�ѧ����ʽ��________________________�����ʳ��ˮ�м����˼��η�̪��Һ����ͨ��Դ����������____________����____________��ֽ���飬�����Կ���____________����������Һ��죬������������ķ�����______________�����������ֲ��ﻯ���ֿ��Եõ��Ȼ��⣬����________��ǿ�������ǣ�����ʣ���������ˮ��ĵ��뷽��ʽΪ__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�Ϻ��и�һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����к���Ԫ�أ�����������²�������ȡ�⣺
��ͨ����Cl2���ڽ������ճɻң�����м�ˮ���裻�ۼ�CCl4���ܹ��ˣ����÷�Һ©����Һ����ȷ�IJ���˳����
A���٢ۢݢڢ� B���ڢܢۢ٢� C���ڢܢ٢ۢ� D���ۢ٢ڢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�걱����ʯ��ɽ������һģ���ۻ�ѧ�Ծ��������棩 ���ͣ������
��13�֣����Ĺ̶��Ǽ���������ѧ��һֱ�о��Ŀ��⡣
��1���±��о��˲�ͬ�¶��´����̵���ҵ�̵��IJ���Kֵ��
��Ӧ | �����̵� N2 (g)+O2 (g) | ��ҵ�̵� N2 (g)+3H2 (g) | |||
�¶�/�� | 27 | 2000 | 25 | 400 | 450 |
K | 3.84��10-31 | 0.1 | 5��108 | 0.507 | 0.152 |
�ٷ������ݿ�֪�������̵���Ӧ����__________������ȡ����ȡ�����Ӧ��
�ڷ������ݿ�֪������ʺϴ��ģģ������̵���ԭ��__________��
�۴�ƽ���ӽǿ��ǣ���ҵ�̵�Ӧ��ѡ������������ʵ�ʹ�ҵ����ȴѡ��500�����ҵĸ��£�������ԭ��_______________________��
 ��2����ҵ�̵���Ӧ�У�������������ͬʱ���ֱ�ⶨN2��ƽ��ת�����ڲ�ͬѹǿ����1����2�������¶ȱ仯�����ߣ���ͼ��ʾ��ͼʾ�У���ȷ����________���A����B�������Ƚϧ�1����2�Ĵ�С��ϵ_________��
��2����ҵ�̵���Ӧ�У�������������ͬʱ���ֱ�ⶨN2��ƽ��ת�����ڲ�ͬѹǿ����1����2�������¶ȱ仯�����ߣ���ͼ��ʾ��ͼʾ�У���ȷ����________���A����B�������Ƚϧ�1����2�Ĵ�С��ϵ_________��
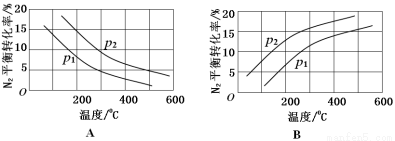

��3��20����ĩ����ѧ�Ҳ��ø����ӵ����Ե�SCY�մɣ��ܴ���H+��Ϊ���ʣ�������������������ϵĽ����ٶྦྷ��Ĥ���缫��ʵ�ָ��³�ѹ�µĵ绯ѧ�ϳɰ�������˷�Ӧ���ת���ʣ���ʵ���ͼ��C��ʾ�������ĵ缫��Ӧʽ��_____________��
��4�����꣬���п�ѧ������ڳ��¡���ѹ�������������ºϳɰ�������˼·����Ӧԭ��Ϊ��2N2(g)+6H2O(1) 4NH3(g)+3O2(g)�����䷴Ӧ�Ȧ�H��___________________��
4NH3(g)+3O2(g)�����䷴Ӧ�Ȧ�H��___________________��
����֪��N2(g)+3H2(g) 2NH3(g) ��H����92.4kJ��mol��1
2NH3(g) ��H����92.4kJ��mol��1
2H2(g) +O2(g) 2H2O(l) ��H����571.6kJ��mol��1 ��
2H2O(l) ��H����571.6kJ��mol��1 ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������ʡ�����и�����ѧ�ڵ�һ���¿����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��NAΪ�����ӵ�������������˵����ȷ����
A��һ�������£�2.3g Na��ȫ��O2��Ӧ����3.6g����ʱ�õ��ĵ�����Ϊ0.1NA
B��1L 0.1mol������Һ����������������0.1NA
C��ˮ������1mol�ǻ����еĵ�������Ϊ9NA
D��1 mol H2O2���м��Թ��ۼ�����ΪNA�����зǼ��Թ��ۼ�Ϊ����2NA
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com