
ÄÜÓĆH++OH﹣=H2OĄ“±ķŹ¾µÄ»Æѧ·“Ó¦ŹĒ£Ø£©
A£® Ba£ØOH£©2ČÜŅŗµĪČėĻ”ĻõĖįÖŠ
B£® NaHSO4ČÜŅŗŗĶ³ĪĒåŹÆ»ŅĖ®·“Ó¦
C£® ĒāŃõ»ÆĆ¾ŗĶĻ”ŃĪĖį·“Ó¦
D£® ¶žŃõ»ÆĢ¼ĶØČėNaOHČÜŅŗÖŠ
æ¼µć£ŗ Ąė×Ó·½³ĢŹ½µÄŹéŠ“£®
·ÖĪö£ŗ Ąė×Ó·½³ĢŹ½”°H++OH﹣=H2O”±±ķŹ¾ĒæĖįÓėæÉČÜŠŌµÄĒæ¼īČÜŅŗ·“Ӧɜ³ÉæÉČÜŠŌµÄŃĪŗĶĖ®µÄ·“Ó¦£¬×¢ŅāĖį±ŲŠėŹĒĒæĖį£¬²»ÄÜĪŖ“×Ėį”¢Ģ¼Ėį£¬¼ī±ŲŠėŹĒæÉČÜŠŌĒæ¼ī£¬Éś³ÉµÄŃĪ±ŲŠėĪŖæÉČÜŠŌµÄ£¬¾Ż“Ė½ųŠŠÅŠ¶Ļ£®
½ā“š£ŗ ½ā£ŗA£®Ba£ØOH£©2ČÜŅŗµĪČėĻ”ĻõĖįÖŠ£¬¶žÕß·“Ӧɜ³ÉæÉČÜŠŌµÄĻõĖį±µŗĶĖ®£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗH++OH﹣=H2O£¬¹ŹAÕżČ·£»
B£®NaHSO4ČÜŅŗŗĶ³ĪĒåŹÆ»ŅĖ®·“Ӧɜ³ÉĮņĖįÄĘ”¢ĮņĖįøĘŗĶĖ®£¬ĮņĖįøĘĪŖĪ¢ČÜĪļ£¬Ąė×Ó·½³ĢŹ½ÖŠĮņĖįøĘ²»ÄܲšæŖ£¬øĆ·“Ó¦²»ÄÜÓĆH++OH﹣=H2O±ķŹ¾£¬¹ŹB“ķĪó£»
C£®ĒāŃõ»ÆĆ¾ĪŖÄŃČÜĪļ£¬Ąė×Ó·½³ĢŹ½ÖŠ²»ÄܲšæŖ£¬ĒāŃõ»ÆĆ¾ÓėŃĪĖįµÄ·“Ó¦²»ÄÜÓĆH++OH﹣=H2O±ķŹ¾£¬¹ŹC“ķĪó£»
D£®¶žŃõ»ÆĢ¼ĪŖŃõ»ÆĪļ£¬Ąė×Ó·½³ĢŹ½ÖŠ¶žŃõ»ÆĢ¼²»ÄܲšæŖ£¬ŠčŅŖ±£Įō·Ö×ÓŹ½£¬¶žŃõ»ÆĢ¼ÓėĒāŃõ»ÆÄĘČÜŅŗµÄ·“Ó¦²»ÄÜÓĆH++OH﹣=H2O±ķŹ¾£¬¹ŹD“ķĪó£»
¹ŹŃ”A£®
µćĘĄ£ŗ ±¾Ģāæ¼²éĮĖĄė×Ó·½³ĢŹ½µÄŹéŠ“ÅŠ¶Ļ£¬ĢāÄæÄѶČÖŠµČ£¬Ć÷Č·Ąė×Ó·½³ĢŹ½µÄŹéŠ“ŌŌņ¼°±ķŹ¾µÄŅāŅåĪŖ½ā“š¹Ų¼ü£¬×¢ŅāÕĘĪÕ³£¼ūµÄÄŃČÜĪļ”¢Čõµē½āÖŹ”¢Ņ×ČÜĪļ£¬ŹŌĢā²ąÖŲ»ł“”ÖŖŹ¶µÄ漲飬ӊĄūÓŚÅąŃųѧɜĮé»īÓ¦ÓĆĖłŃ§ÖŖŹ¶µÄÄÜĮ¦£®


 Ķ¬²½Į·Ļ°Ēæ»ÆĶŲÕ¹ĻµĮŠ“š°ø
Ķ¬²½Į·Ļ°Ēæ»ÆĶŲÕ¹ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÓŠX”¢Y”¢Z”¢W”¢MĪåÖÖ¶ĢÖÜĘŚŌŖĖŲ£¬ĘäÖŠX”¢Y”¢Z”¢WĶ¬ÖÜĘŚ£¬Z”¢MĶ¬Ö÷×壻 X+ÓėM2﹣¾ßÓŠĻąĶ¬µÄµē×Ó²ć½į¹¹£»Ąė×Ó°ė¾¶£ŗZ2﹣£¾W﹣£»YµÄµ„ÖŹ¾§ĢåČŪµćøß”¢Ó²¶Č“ó£¬ŹĒŅ»ÖÖÖŲŅŖµÄ°ėµ¼Ģå²ÄĮĻ£®ĻĀĮŠĖµ·ØÖŠ£¬ÕżČ·µÄŹĒ£Ø””””£©
| ”” | A£® | X”¢MĮ½ÖÖŌŖĖŲÖ»ÄÜŠĪ³ÉX2MŠĶ»ÆŗĻĪļ |
| ”” | B£® | ÓÉÓŚW”¢Z”¢MŌŖĖŲµÄĒā»ÆĪļĻą¶Ō·Ö×ÓÖŹĮæŅĄ“Ī¼õŠ”£¬ĖłŅŌĘä·ŠµćŅĄ“Ī½µµĶ |
| ”” | C£® | ŌŖĖŲY”¢Z”¢WµÄµ„ÖŹ¾§ĢåŹōÓŚĶ¬ÖÖĄąŠĶµÄ¾§Ģå |
| ”” | D£® | ŌŖĖŲWŗĶMµÄijŠ©µ„ÖŹæÉ×÷ĪŖĖ®“¦ĄķÖŠµÄĻū¶¾¼Į |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÓĆŅ»¶ØĢå»żµÄÅضČĪŖ18mol•L﹣1ÅØĮņĖįÅäÖĘ100mL3.0mol•L﹣1Ļ”ĮņĖįµÄŹµŃé²½ÖčČēĻĀ£ŗ
¢Ł¼ĘĖćĖłÓĆÅØĮņĖįµÄĢå»ż ¢ŚĮæČ”Ņ»¶ØĢå»żµÄÅØĮņĖį ¢ŪČܽā¢Ü×ŖŅĘ”¢Ļ“µÓ ¢Ż¶ØČŻ ¢ŽŅ”ŌČ
°“ŅŖĒó»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ĖłŠčÅØĮņĖįµÄĢå»żŹĒ Č”ÅØĮņĖįĖłÓƵÄĮæĶ²µÄ¹ęøńŹĒB£®
“ÓĻĀĮŠŃ”ĻīÖŠŃ”Ōń£ŗA.10mL B.25mL C.50mL D.100mL£®
£Ø2£©¶ŌĖłÅäÖʵÄĻ”ĮņĖį½ųŠŠ²ā¶Ø£¬·¢ĻÖĘäÅØ¶Č“óÓŚ3mol/L£¬ÅäÖĘ¹ż³ĢÖŠĻĀĮŠø÷Ļī²Ł×÷æÉÄÜŅżĘšøĆĪó²īµÄŌŅņÓŠ
A£®ÓĆĮæĶ²ĮæČ”ÅØĮņĖįŹ±£¬ŃöŹÓæĢ¶ČĻßČ”ÅØĮņĖį
B£®¶ØČŻŹ±£¬ø©ŹÓČŻĮæĘææĢ¶ČĻß½ųŠŠ¶ØČŻ
C£®½«Ļ”ŹĶŗóµÄĻ”ĮņĖįĮ¢¼“×ŖČėČŻĮæĘæŗ󣬽ō½ÓמĶ½ųŠŠŅŌŗóµÄŹµŃé²Ł×÷
D£®×ŖŅĘČÜŅŗŹ±£¬²»É÷ÓŠÉŁĮæČÜŅŗČ÷µ½ČŻĮæĘæĶāĆę
E£® ČŻĮæĘæÓĆÕōĮóĖ®Ļ“µÓŗóĪ“øÉŌļ£¬ŗ¬ÓŠÉŁĮæÕōĮóĖ®
F£®¶ØČŻŗ󣬰ŃČŻĮæĘæµ¹ÖĆŅ”ŌČŗó·¢ĻÖŅŗĆęµĶÓŚæĢ¶ČĻߣ¬±ć²¹³ä¼øµĪĖ®ÖĮæĢ¶Č“¦
£Ø3£©½«ÕżČ·ÅäÖʵÄÉĻŹöČÜŅŗČ”³ö10mL£¬½«“Ė10mLČÜŅŗĻ”ŹĶÖĮ1L£¬ŌņĮņĖįµēĄė³öµÄH+ĪļÖŹµÄĮæÅضČĪŖ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
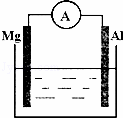
ČēĶ¼ĖłŹ¾×°ÖĆ£ŗ
£Ø1£©ČōÉÕ±ÖŠČÜŅŗĪŖĻ”ĮņĖį£¬Ōņ¹Ū²ģµ½µÄĻÖĻóĪŖ Ź½ĪŖ£ŗÕż¼« £®øĆ×°ÖĆ½«»ÆѧÄÜ×Ŗ»ÆĪŖ
£Ø2£©ČōÉÕ±ÖŠČÜŅŗĪŖĒāŃõ»ÆÄĘČÜŅŗ£¬Ōņøŗ¼«ĪŖ ·½³ĢŹ½ĪŖ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠŹµŃé²Ł×÷»ņŹż¾ŻŗĻĄķµÄŹĒ£Ø£©
A£® ÓĆ¹żĀĖµÄ·½·Ø·ÖĄėFe£ØOH£©3½ŗĢåŗĶHClČÜŅŗ
B£® ÓĆĶŠÅĢĢģĘ½³ĘČ”25.12gNaCl¹ĢĢå
C£® ·Ö±šŗ¬ÓŠMg2+”¢Cu2+ŗĶNa+µÄČżÖÖŃĪČÜŅŗ£¬ÓĆNaOHČÜŅŗ¾ĶÄÜŅ»“Ī¼ų±šæŖ
D£® “ÓĀČĖį¼ŲŗĶ¶žŃõ»ÆĆĢÖĘŃõĘųŗóµÄ»ģŗĻĪļÖŠ·ÖĄė³öæÉČÜĪļµÄ²Ł×÷²½Öč£ŗČܽā”ś¹żĀĖ”śÕōĮó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŅŃÖŖI﹣”¢Fe2+”¢SO2”¢Cl﹣ŗĶH2O2¾łÓŠ»¹ŌŠŌ£¬ĖüĆĒŌŚĖįŠŌČÜŅŗÖŠµÄ»¹ŌŠŌĖ³ŠņĪŖ£ŗSO2£¾I﹣£¾Fe2+£¾H2O2£¾Cl﹣£¬ŌņĻĀĮŠ·“Ó¦²»æÉÄÜ·¢ÉśµÄŹĒ£Ø£©
A£® 2Fe3++SO2+2H2O═2Fe2++SO42﹣+4H+
B£® 2Fe2++I2═2Fe3++2I﹣
C£® I2+SO2+2H2O═H2SO4+2HI
D£® H2O2+SO2═H2SO4
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
£Ø1£©1molNa2SO4ČÜÓŚĖ®ÄܵēĄė³ö øöNa+”¢ øöSO42﹣£®
£Ø2£© molH2OÖŠŗ¬ÓŠµÄŃõŌ×ÓŹżÓė1.5molCO2ÖŠŗ¬ÓŠµÄŃõŌ×ÓŹżĻąµČ£®
£Ø3£©±ź×¼×“æöĻĀ£¬ĆܶČĪŖ0.75g/LµÄNH3ÓėCH4×é³ÉµÄ»ģŗĻĘųĢåÖŠ£¬NH3µÄĢå»ż·ÖŹżĪŖ £®øĆ»ģŗĻĘųĢå¶ŌĒāĘųµÄĻą¶ŌĆܶČĪŖ £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
øł¾ŻŌµē³ŲµÄ¹¤×÷ŌĄķ£¬Ēė·ÖĪöĻĀŹöŌµē³ŲµÄ×é³É£¬¶ŌÓ¦ÕżČ·µÄŅ»×éŹĒ£Ø£©
×Ü·“Ó¦Ź½ Zn+Cu2+=Zn2++Cu
Õż¼« Cu Cu Zn Ag
øŗ¼« Zn Zn Cu Cu
µē½āÖŹČÜŅŗ CuSO4 AgNO3 CuCl2 CuS04
A B C D
A£® A B£® B C£® C D£® D
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻÖÓŠA”¢B”¢C”¢DĖÄÖÖŌŖĖŲ£¬ĖüĆĒµÄÖŹ×ÓŹżŅĄ“ĪŌö¶ą£®
¢ŁAµÄŗĖµēŗÉŹż“óÓŚ2£¬æÉŠĪ³ÉĒā»ÆĪļH2A£¬øĆĒā»ÆĪļŌŚ³£ĪĀĻĀŹĒŅŗĢ壻
¢ŚAŗĶBĮ½ŌŖĖŲæÉŠĪ³ÉB2A3»ÆŗĻĪļ£¬øĆ»ÆŗĻĪļ¼ČÄÜČÜÓŚĒæĖį£¬ÓÖÄÜČÜÓŚĒæ¼ī£»
¢ŪC+Ąė×Ó±ČB3+Ąė×Ó¶ą8øöµē×Ó£»
¢ÜCÓėDŌŖĖŲæÉŅŌŠĪ³É»ÆŗĻĪļCD£»
¢ŻCDµÄČÜŅŗÖŠĶØČėĀČĘųŗó¼Óµķ·ŪČÜŅŗĻŌĄ¶É«£»
£Ø1£©Š“³öC”¢DµÄĆū³Ę£ŗC¼Ų£»µā
£Ø2£©AŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆ
£Ø3£©Š“³öB2A3ÓėĒāŃõ»ÆÄĘČÜŅŗ·“Ó¦µÄĄė×Ó·½³ĢŹ½ £®
£Ø4£©±Č½ĻB”¢C¶žÖÖŌŖĖŲŠĪ³ÉµÄ¼ņµ„Ąė×Ó°ė¾¶µÄ“󊔣ØÓĆĄė×Ó·ūŗűķŹ¾£©£ŗĄė×Ó°ė¾¶£ŗ £®
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com