
25℃和101 kPa时,乙烷、乙炔和丙烯组成的混合烃32 mL,与过量氧气混合并完全燃烧,除去水蒸气,恢复到原来的温度和压强,气体总体积缩小了72 mL,原混合烃中乙炔的体积分数为( )
A.12.5% B.25% C.50% D.75%
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:
向少量FeCl3溶液中滴入KSCN溶液,发生反应:FeCl3+3KSCN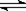 Fe(SCN)3+3KCl。欲使试管内溶液红色变浅,下列措施合理的是
Fe(SCN)3+3KCl。欲使试管内溶液红色变浅,下列措施合理的是
①加Fe(SCN)3 ②加NaOH固体 ③加Zn粉 ④加KCl固体
A.②③ B.②④ C.①② D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
“封管实验”具有简易、方便、节约、绿色等优点,观察下面四个“封管实验”(夹持装置未画出),判断下列说法正确的是( )
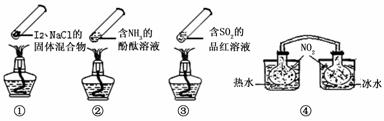
A.加热时,①上部汇聚了固体碘,说明碘的热稳定性较差
B.加热时,②、③中的溶液均变红,冷却后又都变为无色
C.④中,浸泡在热水中的容器内气体颜色变深,浸泡在冰水中的容器内气体颜色变浅
D.四个“封管实验”中都有可逆反应发生
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素A、B、C、D在周期表中的位置如图所示,B、D最外层电子数之和为12,二者可形成DB2、DB3两种分子,DB2具有漂白性。回答下列问题:
| A | B | |
| C | D |
(1)A的氢化物的电子式是 。
(2)下列叙述中,正确的是 (填字母)。
a.稳定性:A的氢化物>C的氢化物 b.还原性:B2->D2-
c.酸性:H4CO4>H2DO4 d.最高化合价:D=B>A>C
(3)DB2通过下列工艺流程可制化工业原料H2DB4和清洁能源H2。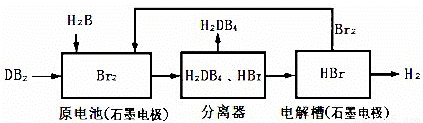
①根据资料:
| 化学式 | Ag2SO4 | AgBr | AgCl |
| Ksp | 1.4×10-5 | 5.0×10-13 | 1.8×10-10 |
为检验分离器的分离效果,取分离后的H2DB4溶液于试管,向其中逐滴加入AgNO3溶液至充分反应,若观察到 ,证明分离效果较好。
②在原电池中,负极发生的反应式为 。
③在电解过程中,电解槽阴极附近溶液pH (填“变大”、“变小”或“不变”)。
④将该工艺流程用总反应的化学方程式表示为: ;该生产工艺的优点有 (答一点即可)。
⑤某含有大量氯化银沉淀的悬浊液中c(Cl-)=0.36mol·L-1,加入等体积的溴化钠溶液,若要产生溴化银沉淀,加入的溴化钠溶液的最小浓度是 mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
以下化学用语正确的是( )
A.甲醛的结构式: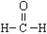 B.乙醇的分子式: CH3CH2OH
B.乙醇的分子式: CH3CH2OH
C.乙烯的结构简式: CH2CH2 D.苯的实验式: C6H6
查看答案和解析>>
科目:高中化学 来源: 题型:
主链为5个碳原子的C7H16的同分异构体中,其中一种同分异构体A的核磁共振氢谱有3个峰且面积比为1︰1︰6,则A的一氯代物的同分异构体的数目为( )
A.2 B.3  C.4
C.4  D.5
D.5
查看答案和解析>>
科目:高中化学 来源: 题型:
在室温下,一种气态烷烃和一种气态烯烃的混合物9克,其密度是相同条件下H2密度的11.25倍。当混合物通过足量的溴水时,溴水增重4.2克,则这两种气态烃是( )
A.CH4和C3H6 B.C2H6和C2H4 C.CH4和C2H4 D.CH4和C4H8
查看答案和解析>>
科目:高中化学 来源: 题型:
查阅有关资料知:金属铝与氢氧化钠溶液反应实际是分以下两步进行:
第一步:2Al+6H2O===2Al(OH)3+3H2↑
第二步:Al(OH)3+NaOH===Na[Al(OH)4]
试回答下列问题:
(1)书写金属铝与氢氧化钠溶液反应的离子方程式:____________________________。
(2)判断两步反应的反应类型:第一步属________,第二步属________(用四种基本反应类型答题)。
(3)请分析,金属铝与氢氧化钠溶液的反应中氧化剂是________,还原剂是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知甲、乙、丙、X是4种中学化学中常见的物质,其转化关系符合如图.则甲和X(要求甲和X能互换)不可能是[提示:Al3++3AlO2﹣+6H2O=4Al(OH)3↓]( )
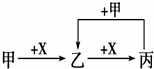
A. C和O2 B. SO2和NaOH溶液
C. Cl2和Fe D. AlCl3溶液和NaOH溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com