
|
有Fe2+、 | |
| [ ] | |
A. |
氧化剂与还原剂的物质的量之比为8∶1 |
B. |
还原产物为 |
C. |
若有1 mol |
D. |
若把该反应设计原电池,则负极反应为:Fe2+-e-=Fe3+ |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:阅读理解
| ||
| ||
| 第一次B中溶液含有离子 | 第二次B中溶液含有离子 | |
| 甲 | 有Fe2+,无Fe3+ | 有SO 42- |
| 乙 | 既有Fe3+,又有Fe2+ | 有SO 42- |
| 丙 | 有Fe3+,无Fe2+ | 有Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
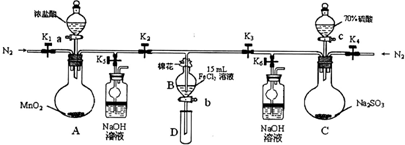
为了验证“铁丝可以在纯净的氧气中燃烧”及“燃烧产物有中Fe2+、Fe3+的存在”。同学们将一根火柴棒塞入一段螺旋状普通细铁丝末端固定;用镊子将铁丝夹住,然后将火柴在酒精灯上点燃,将铁丝由集气瓶口向下慢慢深入,观察现象:
(1)甲同学只发现铁丝红热一下,然后没有现象了。请你分析铁丝没有燃烧的可能原因 (填序号):
A.氧气不纯(或没收集满)
B.火柴太长消耗了氧气
C.铁丝表面有氧化物(或铁锈)
D.没有预热末端铁丝,温度没有达到铁丝的着火点
(2)乙同学做了一些准备工作,当铁丝在纯净氧气中燃烧时,火星四射,并有黑色固体生成。现有实验用品:细纯铁铁丝、细含碳铁丝、镁条、细铜丝、集气瓶装的几瓶纯氧、火柴、酒精灯、镊子、砂纸等。请回答:
①你对“没有火焰”的现象,能提出的问题是: ;验证方法是: 。
②为了找出铁丝在纯氧中燃烧“火星四射”的原因,其假设和对应验证方法是:
。
③如果探究发现只有含碳细铁丝在纯氧中燃烧才出现“火星四射”现象,你分析其原因是: 。
(3)丙某同学为了验证“铁在氧气的燃烧产物中有Fe2+、Fe3+的存在”,设计并进行了如下实验:

试回答下列问题:
①试剂1是 ,试剂2是 。
②加入新制氯水后溶液中颜色加深是因为(用离子方程式表示)
。
③该同学猜想血红色溶液一段时间后变为无色溶液的原因是溶液中的+3价铁被还原为+2价铁,你认为该同学的猜想合理吗? 。若你认为不合理,请提出你的猜想 ,并设计一个简单的实验加以验证(若你认为合理,该空不要作答) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中可能存在Mg2+、Fe2+、Fe3+,加入NaOH溶液,开始时有白色絮状沉淀,迅速变成灰绿色,最后变成红褐色,下列结论中正确的是( )
A.一定有Fe2+,一定没有Fe3+、Mg2+ B.一定有Fe3+,一定没有Fe2+、Mg2+
C.一定有Fe3+,可能有Fe2+,一定没有Mg2+ D.一定有Fe2+,可能有Mg2+,一定没有Fe3+
查看答案和解析>>
科目:高中化学 来源:2012-2013学年贵州省高三上学期期末考试化学试卷(解析版) 题型:选择题
有Fe2+﹑NO3-﹑Fe3+、NH4+﹑H2O和H+六种微粒,分别属于一个氧化还原反应中的反应物和生成物,下列叙述错误的是( )
A.氧化剂与还原剂的物质的量之比为8∶1
B.还原产物为NH4+
C.若有1 mol NO3-参加还原反应,则转移8mol e-
D.若把该反应设计为原电池,则负极反应为Fe2+—e-= Fe3+
查看答案和解析>>
科目:高中化学 来源:2010-2011学年贵州省高三上学期第四次月考(理综)化学部分 题型:选择题
有Fe2++H++NO3-→Fe3++NH4++H2O这样一个变化过程,下列叙述不正确的是
A.氧化剂和还原剂的物质的量之比为1:8
B.该过程说明Fe(NO3)2溶液不宜加酸酸化
C.每1 mol NO3-发生氧化反应,转移8 mol 电子
D.若把该反应设计为原电池,则负极反应为Fe2+- e- = Fe3+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com