
在基态多电子原子中,关于核外电子能量的叙述错误的是( )
A. 最易失去的电子能量最高 B. 电离能最小的电子能量最高
C. p轨道电子能量一定高于s轨道电子能量 D. 在离核最近区域内运动的电子能量最低
科目:高中化学 来源: 题型:
活性炭可处理大气污染物NO。T℃时,在1L密闭容器中加入NO气体和炭粉,发生反应生成两种气体A和B,测得各物质的物质的量如下:
| 活性炭/mol | NO/mol | A/mol | B/mol | |
| 起始状态 | 2.030 | 0.100 | 0 | 0 |
| 2 min时 | 2.000 | 0.040 | 0.030 | 0.030 |
(1)2 min内,用NO表示该反应的平均速率v(NO)=______mol·L-1·min-1。
(2)该反应的化学方程式是______;T℃时,它的平衡常数K=9/16,则2 min时反应_____
(填“是”或“不是”)平衡状态;已知升高温度时,K增大,则该反应为______(填“吸热”或“放热”)反应。
(3)为了提高反应速率和NO的转化率,可采取的措施是____ __。
查看答案和解析>>
科目:高中化学 来源: 题型:
根据化学变化的实质是旧的化学键断裂、新的化学键形成这一理论,判断下列变化是化学变化的是
A.固体氯化钠溶于水 B.氯化铵受热分解生成氯化氢和氨气
C.冰经加热变成水蒸气 D.氯化氢溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
元素周期律和周期表,揭示了元素之间的内在联系,反映了元素性质与它的原子结构的关系,在哲学、自然科学、生产实践各方面都有重要意义。下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:
 |
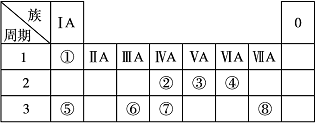
(1)这8种元素中金属性最强的元素是______(填元素符号或化学式,下同),元素最高价氧化物对应的水化物中酸性最强的酸是______;
(2)元素⑧的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式是_________;
(3)③、⑤、⑦三种元素按原子半径由大到小的顺序排列为___________;
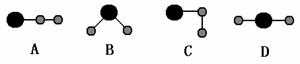 (4)①、④、⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式______________,______________。若用球棍模型表示①和④形成的化合物的分子结构,应该是___________。
(4)①、④、⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式______________,______________。若用球棍模型表示①和④形成的化合物的分子结构,应该是___________。
(5)w是第四周期与③同主族的元素。据此推测w不可能具有的性质是
A.最高正化合价为+5价 B.气态氢化物比NH3稳定
C.最高价氧化物的水化物的酸性比硝酸弱 D.单质在常温下可与氢气化合
(6)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:
|
|
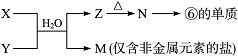
X溶液与Y溶液反应的离子方程式_______,M中阳离子的鉴定方法____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中不正确的是( )
A.在NH4+和[Cu(NH3)4]2+中都存在配位键
B.C2H5OH与C2H5Br相比,前者的沸点远高于后者,其原因是前者的分子间存在氢键
C.同周期ⅠA族元素和 ⅦA族元素之间只能形成离子化合物
D.由两种非金属元素组成的化合物分子中只可能有极性键,不会有非极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W是原子序数依次增大的短周期主族元素,X、Z在周期表中的相对位置如下表。已知X元素最低负化合价的绝对值与其原子最外层电子数相等,Y是地壳中含量最多的金属元素。下列说法错误的是( )
| X | ||
| Z |
A.X位于第二周期第IVA族
B.原子半径由小到大的顺序为:W<Z<Y
C.Z、W两元素的气态氢化物中,Z的气态氢化物更稳定
D.无论氧气是否过量,Z在氧气中燃烧的产物唯一
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实及其解释不正确的是 ( )。
A.滴有酚酞的NaHCO3溶液呈浅红色,微热后红色加深,是因为NaHCO3分解生成了Na2CO3
B.钠保存在煤油中,是因为煤油不与钠发生反应,钠比煤油密度大,煤油可以使钠隔绝空气和水蒸气
C.用洁净的玻璃管向包有Na2O2的脱脂棉吹气,脱脂棉燃烧,说明CO 2、H2O与Na2O2的反应是放热反应
2、H2O与Na2O2的反应是放热反应
D.钠长期暴露在空气中的产物是Na2CO3,原因是钠与氧气生成的Na2O与水和二氧化碳反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列排列顺序正确的是 ( )
①热稳定性:H2O>HF>H2S ②原子半径:Na>Mg>F
③酸性:H3PO4>H2SO4>HClO4 ④失电子能力:Na>Mg>Al
⑤晶体的熔点:SiO2>NaCl>CCl4>SO2
A.②④⑤ B.①②④ C.②③⑤ D.全部正确
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com