
 .
.分析 (1)CO2是共价化合物,其结构式为O=C=O,碳原子和氧原子之间有2对电子;
(2)碳酸钠与CO2和水反应生成NaHCO3,NaHCO3溶解度小于Na2CO3,溶液中出现白色浑浊;
(3)根据氧化还原反应中得失电子数相等和质量守恒配平.
解答 解:(1)CO2是共价化合物,其结构式为O=C=O,碳原子和氧原子之间有2对电子,其电子式为 ,
,
故答案为: ;
;
(2)碳酸钠与CO2和水反应生成酸式盐NaHCO3,NaHCO3溶解度小于Na2CO3,并且反应生成的NaHCO3固体质量比原来Na2CO3多,溶剂质量减少,溶液中有浑浊出现,反应的离子方程式为:2Na++CO32-+H2O+CO2=2NaHCO3↓,
故答案为:2Na++CO32-+CO2+H2O═2NaHCO3↓;
(3)双氧水中氧元素的化合价从-1价升高到0价,失去1个电子.而高锰酸钾中锰元素的化合价从+7价降低到+2价,得到2个电子,所以根据电子的得失守恒可知,配平后的反应为2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2↑,
故答案为:2;5;6H+;2;8;5O2↑.
点评 本题考查了电子式、离子方程式、氧化还原反应方程式的书写,注意掌握电子式的概念及表示方法,氧化还原反应应把握反应中元素的化合价变化为解答的关键,侧重分析、应用能力的考查,题目难度不大.


 华东师大版一课一练系列答案
华东师大版一课一练系列答案科目:高中化学 来源: 题型:解答题
 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
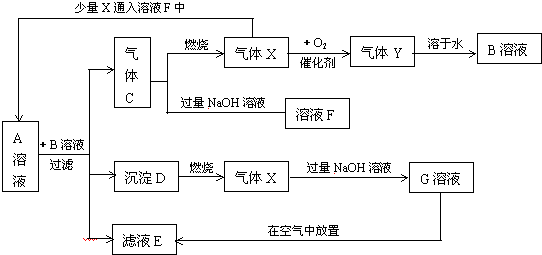
| A. | 气体C是SO2 | |
| B. | 溶液A和溶液B可能的化学反应为3Na2S+Na2SO3+4H2SO4=3S↓+H2S↑+4Na2SO4+3H2O | |
| C. | 若氧气足量气体C可以一步反应得到气体Y | |
| D. | 图中少量X通入溶液F中不涉及氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正戊烷、异戊烷和新戊烷互为同分异构体,沸点依次升高 | |
| B. | 乙醇依次通过消去、取代、加成反应可生成乙二醇 | |
| C. | 在鸡蛋清溶液中分别加入饱和Na2SO4、CuSO4溶液,都会因盐析产生沉淀 | |
| D. | 等质量的甲烷、乙烯、1,3-丁二烯分别充分燃烧,所耗用氧气的量依次减少 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化铝溶液中加入过量氨水:Al3++4 NH3•H2O═AlO2-+4NH4++2H2O | |
| B. | 18gD2O中含有的中子数为10 NA(设NA为阿伏加德罗常数的数值) | |
| C. | 明矾既可以用于净水,又可杀菌消毒 | |
| D. | 恒温恒容下,某可逆反应X(g)+Y(g)?Z(g)+W(s)△H>0达平衡后再加入X,该反应的△H不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
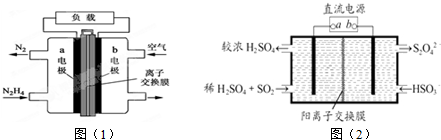
| A. | 图(1)中的a电极应与 图(2)的a相连 | |
| B. | 图(1)中a电极应的反应方程式为:N2H4+4OH--4e-═N2+4H2O | |
| C. | 用该燃料电池作为装置图(2)的直流电,吸收1 molSO2至少需要通人 0.5 mol N2H4 | |
| D. | 图(1)中OH-由阴离子交换膜从左流向右,图(2)中H+由阳离子交换膜从右流向左 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
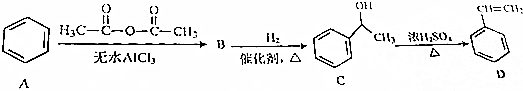
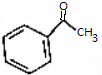 .
.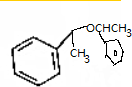
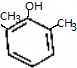 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C3H8是折线形极性分子 | |
| B. | 只有过渡金属才能接受电子对形成配合物 | |
| C. | 乳酸[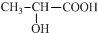 ]中存在一个手性碳原子 ]中存在一个手性碳原子 | |
| D. | 已知酸性:H3PO4>HClO,是因为H3PO4分子中有1个非羟基氧原子,而HClO中非羟基氧原子个数为0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 12C和14C | B. | O2与O3 | ||
| C. | 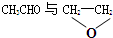 | D. | CH3CH2CH2CH3与CH3CH2CH2CH2CH3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com