
”¾ĢāÄæ”æA”¢B”¢C”¢D”¢E”¢FĮłÖÖŌŖĖŲĪŖŌ×ÓŠņŹżŅĄ“ĪŌö“óµÄ¶ĢÖÜĘŚŌŖĖŲ”£AĪŖŌ×Ó°ė¾¶×īŠ”µÄŌŖĖŲ£¬AŗĶBæÉŠĪ³É4Ō×Ó10µē×ӵķÖ×ÓX£»CµÄ×īĶā²ćµē×ÓŹżŹĒÄŚ²ćµÄ3±¶£»DŌ×ÓµÄ×īĶā²ćµē×ÓŹżŹĒ×īÄŚ²ćµē×ÓŹżµÄŅ»°ė£»EŹĒµŲæĒÖŠŗ¬Įæ×ī¶ąµÄ½šŹōŌŖĖŲ£»FŌŖĖŲµÄ×īøßÕż¼ŪÓė×īµĶøŗ¼Ū“śŹżŗĶĪŖ6”£Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©AŗĶC°“Ō×ÓøöŹż±Č1”Ć1ŠĪ³É4Ō×Ó·Ö×ÓY£¬YµÄ½į¹¹Ź½ŹĒ___________”£
£Ø2£©·Ö×ÓXµÄµē×ÓŹ½ŹĒ__________£»DæÉŅŌŌŚŅŗĢ¬XÖŠ·¢ÉśĄąĖĘÓŚÓėA2CµÄ·“Ó¦,Š“³ö·“Ó¦µÄ»Æѧ·½³ĢŹ½_________________________________”£
£Ø3£©ŹµŃéÖ¤Ć÷£¬ČŪČŚµÄEF3 ²»µ¼µē£¬ĘäŌŅņŹĒ_______________________”£
£Ø4£©EµÄµ„ÖŹæÉČÜÓŚA”¢C”¢DŠĪ³ÉµÄ»ÆŗĻĪļZµÄĖ®ČÜŅŗÖŠ”£ĄĀü¹āĘ×Ö¤Źµ“Ė·“Ӧɜ³ÉµÄŅõĄė×ÓÖ÷ŅŖŅŌE(CA)4£ µÄŠĪŹ½“ęŌŚ£¬Š“³öEČÜÓŚZČÜŅŗµÄĄė×Ó·½³ĢŹ½£ŗ_____________________”£
£Ø5£©¹¤ŅµĘ·ZµÄČÜŅŗÖŠŗ¬ÓŠÄ³Š©ŗ¬ŃõĖįøłŌÓÖŹ£¬æÉÓĆĄė×Ó½»»»Ä¤·Øµē½āĢį“攣µē½ā²ŪČװӊŃōĄė×Ó½»»»Ä¤£ØÖ»ŌŹŠķŃōĄė×ÓĶعż£©£¬Ę乤×÷ŌĄķČēĶ¼ĖłŹ¾”£
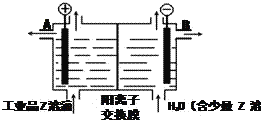
¢ŁøƵē½ā²ŪµÄŃō¼«·“Ó¦Ź½ŹĒ_________________”£
¢ŚĶصēæŖŹ¼ŗó£¬Ņõ¼«ø½½üČÜŅŗpH___________£Ø”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°²»±ä”±£©”£
¢Ū³żČ„ŌÓÖŹŗóµÄZČÜŅŗ“ÓŅŗĢå³öæŚ_________£ØĢīŠ“”°A”±»ņ”°B”±£©µ¼³ö”£
”¾“š°ø”æ H£O£O£H ![]() 2Na£«2NH3£½2NaNH2£«H2”ü AlCl3 ŌŚČŪČŚµÄדĢ¬ĻĀ²»·¢ÉśµēĄė£¬Ć»ÓŠ²śÉś×ŌÓÉŅĘ¶ÆµÄĄė×Ó 2Al£«2OH££«6H2O£½2Al(OH)4££«3H2”ü 4OH££4e££½2H2O£«O2”ü Ōö“ó B
2Na£«2NH3£½2NaNH2£«H2”ü AlCl3 ŌŚČŪČŚµÄדĢ¬ĻĀ²»·¢ÉśµēĄė£¬Ć»ÓŠ²śÉś×ŌÓÉŅĘ¶ÆµÄĄė×Ó 2Al£«2OH££«6H2O£½2Al(OH)4££«3H2”ü 4OH££4e££½2H2O£«O2”ü Ōö“ó B
”¾½āĪö”æA”¢B”¢C”¢D”¢E”¢FĮłÖÖŌŖĖŲĪŖŌ×ÓŠņŹżŅĄ“ĪŌö“óµÄ¶ĢÖÜĘŚŌŖĖŲ,AĪŖŌ×Ó°ė¾¶×īŠ”µÄŌŖĖŲ,ĪŖHŌŖĖŲ;AŗĶBæÉŠĪ³É4Ō×Ó10µē×ӵķÖ×ÓX,ŌņBĪŖNŌŖĖŲ;CµÄ×īĶā²ćµē×ÓŹżŹĒÄŚ²ćµÄ3±¶,ŌņCĪŖOŌŖĖŲ;DŌ×ÓµÄ×īĶā²ćµē×ÓŹżŹĒ×īÄŚ²ćµē×ÓŹżµÄŅ»°ė,ĪŖNaŌŖĖŲ;EŹĒµŲæĒÖŠŗ¬Įæ×ī¶ąµÄ½šŹōŌŖĖŲ,ĪŖAlŌŖĖŲ;FŌŖĖŲµÄ×īøßÕż¼ŪÓė×īµĶøŗ¼Ū“śŹżŗĶĪŖ6,ŌņFĪŖClŌŖĖŲ”£
(1)AŗĶC°“Ō×ÓøöŹż±Č1”Ć1ŠĪ³É4Ō×Ó·Ö×ÓYĪŖH2O2,Ęä½į¹¹Ź½ĪŖ, H£O£O£H Ņņ“Ė£¬±¾ĢāÕżČ·“š°øŹĒ: H£O£O£H ”£
(2)·Ö×ÓXŹĒ°±Ęų,°±Ęų·Ö×ÓÖŠĆæøöHŌ×ÓŗĶNŌ×ÓŠĪ³ÉŅ»¶Ō¹²ÓƵē×Ó¶Ō,µē×ÓŹ½ĪŖ![]() ;DŹĒNa,ÄĘŗĶ°±ĘųµÄ·“Ó¦Ļąµ±ÓŚŗĶĖ®µÄ·“Ó¦,øł¾ŻÄĘŗĶĖ®µÄ·“Ó¦Š“³öÄĘŗĶ°±Ęų·“Ó¦ĪŖ 2Na£«2NH3£½2NaNH2£«H2”ü,Ņņ“Ė£¬±¾ĢāÕżČ·“š°øŹĒ:
;DŹĒNa,ÄĘŗĶ°±ĘųµÄ·“Ó¦Ļąµ±ÓŚŗĶĖ®µÄ·“Ó¦,øł¾ŻÄĘŗĶĖ®µÄ·“Ó¦Š“³öÄĘŗĶ°±Ęų·“Ó¦ĪŖ 2Na£«2NH3£½2NaNH2£«H2”ü,Ņņ“Ė£¬±¾ĢāÕżČ·“š°øŹĒ:![]() ; 2Na£«2NH3£½2NaNH2£«H2”ü
; 2Na£«2NH3£½2NaNH2£«H2”ü
(3)ĀČ»ÆĀĮŹĒ·Ö×Ó¾§Ģå,ČŪȌדĢ¬ĻĀŅŌ·Ö×Ó“ęŌŚ,ČŪČŚµÄAlCl3 ²»µ¼µē,Ņņ“Ė£¬±¾ĢāÕżČ·“š°øŹĒ:AlCl3 ŌŚČŪČŚµÄדĢ¬ĻĀ²»·¢ÉśµēĄė,ƻӊ²śÉś×ŌÓÉŅĘ¶ÆµÄĄė×Ó”£
(4)AlµÄµ„ÖŹæÉČÜÓŚH”¢O”¢NaŠĪ³ÉµÄ»ÆŗĻĪļNaOHµÄĖ®ČÜŅŗÖŠ.ĄĀü¹āĘ×Ö¤Źµ“Ė·“Ӧɜ³ÉµÄŅõĄė×ÓÖ÷ŅŖŅŌAl(OH)4£µÄŠĪŹ½“ęŌŚ,øł¾Ż·“Ó¦ĪļŗĶÉś³ÉĪļŹéŠ“Ąė×Ó·½³ĢŹ½ĪŖ2Al£«2OH££«6H2O£½2Al(OH)4££«3H2”üŅņ“Ė£¬±¾ĢāÕżČ·“š°øŹĒ:2Al£«2OH££«6H2O£½2Al(OH)4££«3H2”ü
(5)¢ŁøƵē½ā²ŪµÄŃō¼«ÉĻĒāŃõøłĄė×ӷŵē,µē¼«·“Ó¦Ź½ĪŖ4OH££4e££½2H2O£«O2”ü,Ņņ“Ė£¬±¾ĢāÕżČ·“š°øŹĒ:4OH££4e££½2H2O£«O2”ü”£
¢ŚĶصēæŖŹ¼ŗó,Ņõ¼«ÉĻĖ®µĆµē×ÓÉś³ÉĒāĘųĶ¬Ź±Éś³ÉĒāŃõøłĄė×Ó,µ¼ÖĀŅõ¼«ø½½üĒāŃõøłĄė×ÓÅضČŌö“ó,ĖłŅŌpHŌö“ó,Ņņ“Ė£¬±¾ĢāÕżČ·“š°øŹĒ:Ōö“ó”£
¢ŪŌŚŅõ¼«ø½½üÉś³ÉĒāŃõøłĄė×Ó,ŃōĄė×ÓĶعż½»»»Ä¤½ųČėŅõ¼«ŹŅµĆµ½NaOH,ĖłŅŌŌŚŅõ¼«ŹŅµĆµ½NaOH,ĖłŅŌ“ÓB³öĄ“,Ņņ“Ė£¬±¾ĢāÕżČ·“š°øŹĒ:B.


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓŠČēĻĀŗĻ³ÉĀ·Ļߣ¬¼×¾¶ž²½×Ŗ»ÆĪŖ±ū£¬ĻĀĮŠŠšŹö²»ÕżČ·µÄŹĒ£Ø £© 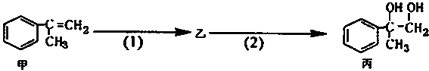
A.±ūÖŠæÉÄÜŗ¬ÓŠĪ“·“Ó¦µÄ¼×£¬æÉÓĆäåĖ®¼ģŃéŹĒ·ńŗ¬¼×
B.·“Ó¦£Ø1£©µÄĪŽ»śŹŌ¼ĮŹĒŅŗä壬Ģś×÷“߻ƼĮ
C.¼×ŗĶ±ū¾łæÉÓėĖįŠŌKMnO4ČÜŅŗ·¢Éś·“Ó¦
D.·“Ó¦£Ø2£©·“Ó¦ŹōÓŚČ”“ś·“Ó¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”涞ĀČ»Æķæ(SO2Cl2)ŹĒŅ»ÖÖÖŲŅŖµÄÓŠ»śŗĻ³ÉŹŌ¼Į£¬ŹµŃéŹŅæÉĄūÓĆSO2ÓėCl2·“Ó¦ÖĘȔɣĮæµÄSO2Cl2”£×°ÖĆČēĶ¼£ØÓŠŠ©Ö§³Ö×°ÖĆŹ”ĀŌĮĖ£©ĖłŹ¾”£
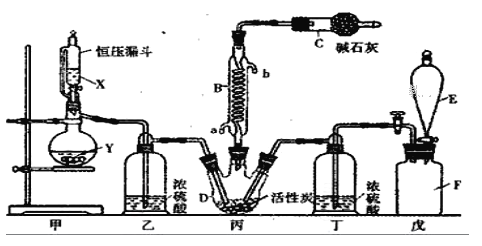
ŅŃÖŖSO2Cl2µÄČŪµćĪŖ-54.1”ę£¬·ŠµćĪŖ69. 1”ę£»³£ĪĀĻĀ±Č½ĻĪČ¶Ø£¬ŹÜČČŅ×·Ö½ā£¬ÓöĖ®ÄÜ·¢Éś¾ēĮŅµÄĖ®½ā·“Ó¦£¬²śĪļÖ®Ņ»ĪŖĀČ»ÆĒāĘųĢ唣
£Ø1£©ĪģŹĒÖüĘų×°ÖĆ£¬ FĘæÖŠµÄĘųĢåÄÜŹ¹ŹŖČóµÄÓŠÉ«²¼ĢõĶŹÉ«£¬ŌņFĘæÖŠµÄĘųĢåµÄŹµŃéŹŅÖĘ·ØŹĒ________________________________£ØÓĆ·½³ĢŹ½±ķŹ¾£©£»
£Ø2£©B“¦·“Ó¦¹ÜĄäČ“Ė®Ó¦“Ó__________(Ģī”°a”±»ņ”°b”±)½ÓæŚĶØČė£»CŅĒĘ÷µÄĆū³ĘĪŖ____________£¬¼īŹÆ»ŅµÄ×÷ÓĆĪŖ____________”£
£Ø3£©×°ÖĆŅŅŗĶ¶”µÄ×÷ÓĆŹĒ____________£»
£Ø4£©ŗćŃ¹Ā©¶·¾ßÓŠĢŲŹāµÄ½į¹¹£¬Ö÷ŅŖÄæµÄŹĒ___________£»
£Ø5£©Š“³ö¶žĀČ»Æķæ(SO2Cl2)Ė®½ā·“Ó¦µÄ·½³ĢŹ½________________£»
£Ø6£©SO2ČÜÓŚĖ®Éś³ÉŃĒĮņĖį£¬ŃĒĮņĖįµÄĖįŠŌĒæÓŚ“ĪĀČĖį£¬Ń”ÓĆĻĀĆęµÄ×°ÖĆŗĶŅ©Ę·Ģ½¾æŃĒĮņĖįÓė“ĪĀČĖįµÄĖįŠŌĒæČõ£ŗ

×°ÖĆĮ¬½ÓĖ³ŠņĪŖA”¢_______”¢______”¢______”¢D”¢F£¬ĘäÖŠEµÄ×÷ÓĆŹĒ____________£¬Ķعż________________ĻÖĻó¼“æÉÖ¤Ć÷ŃĒĮņĖįµÄĖįŠŌĒæÓŚ“ĪĀČĖį”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¹ŲÓŚNa2CO3ŗĶNaHCO3ŠŌÖŹµÄĖµ·ØÕżČ·µÄŹĒ
A. ŌŚĖ®ÖŠµÄČܽāŠŌ: NaHCO3>Na2CO3
B. ČČĪČ¶ØŠŌ£ŗNaHCO3<Na2CO3
C. ÓėĖį·“Ó¦µÄ¾ēĮŅ³Ģ¶Č: NaHCO3<Na2CO3,
D. Ö»ÄÜČĆNaHCO3×Ŗ»Æ³ÉNa2CO3
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĮņõ£ĀČ(SO2Cl2)³£×÷ĀČ»Æ¼Į»ņĀČč«»Æ¼Į£¬ÓĆÓŚÖĘ×÷Ņ©Ę·”¢Č¾ĮĻ”¢±ķĆę»īŠŌ¼ĮµČ”£ÓŠ¹ŲĪļÖŹµÄ²æ·ÖŠŌÖŹČēĻĀ±ķ£ŗ
ĪļÖŹ | ČŪµć/”ę | ·Šµć/”ę | ĘäĖüŠŌÖŹ |
SO2Cl2 | -54.1 | 69.1 |
¢ŚŅ×·Ö½ā£ŗSO2Cl2 SO2”ü+Cl2”ü |
H2SO4 | 10.4 | 338 | ¾ßÓŠĪüĖ®ŠŌĒŅ²»Ņ×·Ö½ā |
ŹµŃéŹŅÓĆøÉŌļ¶ų“æ¾»µÄ¶žŃõ»ÆĮņŗĶĀČĘųŗĻ³ÉĮņõ£ĀČ£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖSO2(g)+Cl2(g) ![]() SO2Cl2(l)”÷H=-97.3kJ/mol”£×°ÖĆČēĶ¼ĖłŹ¾£Ø¼Š³ÖŅĒĘ÷ŅŃŹ”ĀŌ£©£¬Ēė»Ų“šÓŠ¹ŲĪŹĢā£ŗ
SO2Cl2(l)”÷H=-97.3kJ/mol”£×°ÖĆČēĶ¼ĖłŹ¾£Ø¼Š³ÖŅĒĘ÷ŅŃŹ”ĀŌ£©£¬Ēė»Ų“šÓŠ¹ŲĪŹĢā£ŗ

£Ø1£©ŅĒĘ÷BµÄ×÷ÓĆŹĒ_____________________”£
£Ø2£©ČōĪŽ×°ÖĆŅŅĮņõ£ĀČ»į·¢ÉśĖ®½ā£¬ŌņĮņõ£ĀČĖ®½ā·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ________________”£
£Ø3£©Š“³ö¶”×°ÖĆÖŠ·¢Éś·“Ó¦µÄ»Æѧ·“Ó¦·½³ĢŹ½²¢±ź³öµē×ÓµÄ×ŖŅĘ__________________”£
£Ø4£©ĪŖĢįøß±¾ŹµŃéÖŠĮņõ£ĀČµÄ²śĀŹ£¬ŌŚŹµŃé²Ł×÷ÖŠŠčŅŖ×¢ŅāµÄŹĀĻīÓŠ_________(ĢīŠņŗÅ)
¢ŁĻČĶØĄäÄżĖ®£¬ŌŁĶØĘų ¢ŚæŲÖĘĘųĮ÷ĖŁĀŹ£¬ŅĖĀż²»ŅĖæģ
¢ŪČōČż¾±ÉÕĘæ·¢ĢĢ£¬æÉŹŹµ±½µĪĀ ¢Ü¼ÓČČČż¾±ÉÕĘæ
£Ø5£©ÉŁĮæĮņõ£ĀČŅ²æÉÓĆĀČ»ĒĖį(ClSO3H)·Ö½ā»ńµĆ£¬øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ________________________£¬“Ė·½·ØµĆµ½µÄ²śĘ·ÖŠ»į»ģÓŠĮņĖį”£“Ó·Ö½ā²śĪļÖŠ·ÖĄė³öĮņõ£Āȵķ½·ØŹĒ___________________”£
£Ø6£©¹¤ŅµÉĻ“¦ĄķSO2·ĻĘųµÄ·½·Øŗܶą£¬ĄżČēæÉŅŌÓĆFe2(SO4)3ĖįŠŌČÜŅŗ“¦Ąķ£¬Ę乤ŅÕĮ÷³ĢČēĻĀČÜŅŗ¢Ś×Ŗ»ÆĪŖČÜŅŗ¢Ū·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ__________________________ £»
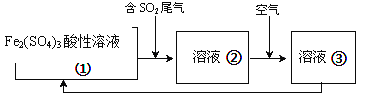
ÓŠµÄ¹¤³§ÓƵē½ā·Ø“¦Ąķŗ¬ÓŠSO2µÄĪ²Ęų£¬Ęä×°ÖĆČēĻĀĶ¼ĖłŹ¾£Øµē¼«²ÄĮĻ¾łĪŖ¶čŠŌµē¼«£©”£ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ_______
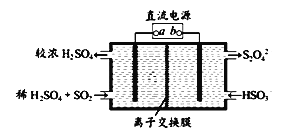
A£®µē¼«aĮ¬½ÓµÄŹĒµēŌ“µÄÕż¼«
B£®ČōµēĀ·ÖŠ×ŖŅĘ0.03mole-£¬ŌņĄė×Ó½»»»Ä¤×ó²ąČÜŅŗÖŠŌö¼Ó0.03molĄė×Ó
C£®Ķ¼ÖŠµÄĄė×Ó½»»»Ä¤ŹĒŃōĄė×Ó½»»»Ä¤
D£®Ņõ¼«µÄµē¼«·“Ó¦Ź½ĪŖ2HSO3-+2e-+2H+==S2O42-+2H2O
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”湤ŅµÉĻĄūÓƵē½ā±„ŗĶŹ³ŃĪĖ®Éś²śĀČĘų(Cl2)”¢ÉÕ¼īŗĶĒāĘųµÄ»Æѧ·½³ĢŹ½ŹĒ:2NaCl + 2H2O![]() 2NaOH + Cl2”ü+ H2”ü
2NaOH + Cl2ӟ+ H2ӟ
£Ø1£©ÓĆĖ«ĻßĒűķŹ¾³öµē×Ó×ŖŅʵķ½ĻņŗĶŹżÄæ______________£¬ĢāøÉÖŠ·“Ó¦øÄŠ“³ÉĄė×Ó·½³ĢŹ½ŹĒ___________________________________
£Ø2£©µē½āŹ³ŃĪĖ®µÄ¹ż³ĢÖŠ£¬Ńõ»Æ²śĪļŹĒ__________________________________
£Ø3£©µē½āŹ³ŃĪĖ®ŅŖĒó¶Ō“ÖŹ³ŃĪĖ®½ųŠŠ¾«ÖĘ£¬ŅŌ³żČ„“ÖŹ³ŃĪĖ®ÖŠŗ¬ÓŠµÄÄąÉ³ŗĶSO42-”¢Ca2+,Mg2+µČŌÓÖŹĄė×Ó”£¾«ÖĘŹ±ŅĄ“Ī¼ÓČėĀČ»Æ±µČÜŅŗ”¢“æ¼ī”¢ÉÕ¼ī£¬³ä·Ö·“Ó¦ŗó¹żĀĖ£¬ŌŚĀĖŅŗÖŠ¼ÓČėŃĪĖįÖŠŗĶÖĮÖŠŠŌ”£ŃĪĖįÓėĀĖŅŗ·“Ó¦µÄĄė×Ó·½³ĢŹ½:____________________________
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æA”¢B”¢C”¢D”¢EĪåÖÖŌŖĖŲµÄŌ×ÓŠņŹżŅĄ“ĪŌö“ó£¬AŌ×ÓĪŽÖŠ×Ó£¬BµÄµ„ÖŹŌŚæÕĘųÖŠŗ¬Įæ×ī¶ą£¬C”¢DŌŖĖŲĶ¬Ö÷×åĒŅŌ×ÓŠņŹżDĪŖCµÄ¶ž±¶£¬EŌŖĖŲµÄ¼Ūµē×ÓÅŲ¼Ź½ĪŖ£Øn©l£©d10+6ns1 £¬ »Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ŌŖĖŲBŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆŹĒ £®
£Ø2£©DŌŖĖŲ»łĢ¬Ō×ÓµÄĶāĪ§µē×ÓÅŲ¼Ź½ĪŖ £®
£Ø3£©BC ![]() µÄĮ¢Ģå¹¹ŠĶĪŖ £®
µÄĮ¢Ģå¹¹ŠĶĪŖ £®
£Ø4£©AŌŖĖŲÓėCŌŖĖŲŠĪ³ÉĮ½ÖÖ³£¼ūµÄ»ÆŗĻĪļ£¬ĘäŌ×ÓøöŹż±Č·Ö±šĪŖ2£ŗ1ŗĶ1£ŗ1£¬Į½ÖÖ»ÆŗĻĪļæÉŅŌČĪŅā±Č»„ČÜ£¬ŌŅņŹĒ£»ĘäÖŠŅ»ÖÖ»ÆŗĻĪļæÉŌŚĖįŠŌĢõ¼žĻĀ½«KMnO4»¹ŌĪŖMn2+ £¬ Š“³öĻą¹Ų·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ
£Ø5£©½«¹żĮæBA3ĘųĢåĶØČėŗ¬E2+ČÜŅŗÖŠ³ä·Ö·“Ó¦ŗóÉś³ÉµÄ¶ž¼ŪŃōĄė×ÓŹĒ£ØĢīĄė×Ó·ūŗÅ£©£¬ImoløĆĄė×ÓÖŠŗ¬¦Ņ¼üĪŖmol£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓŠ»śĪļAŹĒŅ»ŌŖōČĖį£¬ÓÉC£¬H£¬OŌŖĖŲ×é³É£¬ÖŹĮæ·ÖŹż£ŗC%40%£»H 6.67%£»Č”0.60g AÅä³ÉČÜŅŗ£¬ÓĆŗ¬0.01mol NaOH µÄČÜŅŗÄÜĒ”ŗĆĶźČ«ÖŠŗĶ£®
£Ø1£©AµÄ×ī¼ņŹ½ĪŖ£»×ī¼ņŹ½ĮæĪŖ £®
£Ø2£©AµÄĻą¶Ō·Ö×ÓÖŹĮæĪŖ£»·Ö×ÓŹ½ĪŖ £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠÓŠ¹ŲŃõ»Æ»¹Ō·“Ó¦µÄŠšŹö“ķĪóµÄŹĒ
A.ø“·Ö½ā·“Ó¦Ņ»¶Ø²»ŹĒŃõ»Æ»¹Ō·“Ó¦
B.Ńõ»Æ»¹Ō·“Ó¦Ņ»¶ØÓŠŌŖĖŲ»ÆŗĻ¼ŪµÄÉż½µ
C.Ńõ»Æ»¹Ō·“Ó¦ÖŠŃõ»Æ¼ĮŗĶ»¹Ō¼ĮæÉÄÜŹĒĶ¬Ņ»ÖÖĪļÖŹ
D.Ńõ»Æ¼ĮŹ§µē×Ó£¬±»»¹Ō
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com