
【题目】以苯酚经下列反应可制香料M和高分子化合物N(部分产物及反应条件已略去)
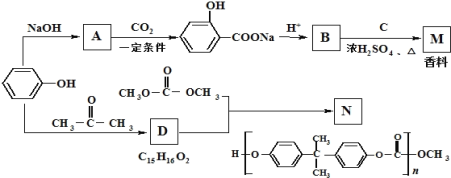
(1)已知C的分子式为C5H12O,C能与金属Na反应,C的一氯代物有2种,则C的结构简式为 ________.
(2)由D生成N的反应类型是_________.
(3)由苯酚生成D的化学方程式是_________.
(4)F是分子量比B大14的同系物,则F的分子式是__________________ .F有多种同分异构体,符合下列条件的F的同分异构体有_______ 种
①遇FeCl3溶液显紫色,且能水解②苯环上有两个取代基,且苯环上的一溴代物只有两种。
(5)已知: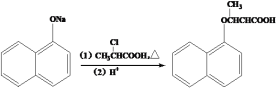 ,写出以苯酚、乙醇和CH2ClCOOH为原料制备
,写出以苯酚、乙醇和CH2ClCOOH为原料制备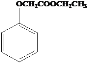 的合成路线流程图(无机试剂任用)_________。
的合成路线流程图(无机试剂任用)_________。
【答案】![]() 缩聚反应
缩聚反应 ![]()
![]() C8H8O3 3
C8H8O3 3 
【解析】
![]() 与NaOH反应生成苯酚钠和H2O,A的结构简式为
与NaOH反应生成苯酚钠和H2O,A的结构简式为![]() ;
;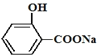 酸化生成B,B的结构简式为
酸化生成B,B的结构简式为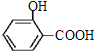 ;C的分子式为C5H12O,C能与金属Na反应,C属于饱和一元醇,C的一氯代物有2种,C的结构简式为
;C的分子式为C5H12O,C能与金属Na反应,C属于饱和一元醇,C的一氯代物有2种,C的结构简式为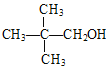 ;B与C发生酯化反应生成香料M,M的结构简式为
;B与C发生酯化反应生成香料M,M的结构简式为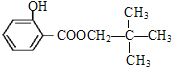 ;
;![]() 与
与![]() 反应生成D,D的分子式为C15H16O2,D的不饱和度为8,D与
反应生成D,D的分子式为C15H16O2,D的不饱和度为8,D与![]() 发生缩聚反应生成N,由N的结构简式可逆推出D的结构简式为
发生缩聚反应生成N,由N的结构简式可逆推出D的结构简式为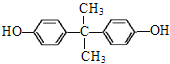 ;根据上述推断作答。
;根据上述推断作答。
![]() 与NaOH反应生成苯酚钠和H2O,A的结构简式为
与NaOH反应生成苯酚钠和H2O,A的结构简式为![]() ;
; 酸化生成B,B的结构简式为
酸化生成B,B的结构简式为 ;C的分子式为C5H12O,C能与金属Na反应,C属于饱和一元醇,C的一氯代物有2种,C的结构简式为
;C的分子式为C5H12O,C能与金属Na反应,C属于饱和一元醇,C的一氯代物有2种,C的结构简式为 ;B与C发生酯化反应生成香料M,M的结构简式为
;B与C发生酯化反应生成香料M,M的结构简式为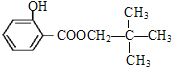 ;
;![]() 与
与![]() 反应生成D,D的分子式为C15H16span>O2,D的不饱和度为8,D与
反应生成D,D的分子式为C15H16span>O2,D的不饱和度为8,D与![]() 发生缩聚反应生成N,由N的结构简式可逆推出D的结构简式为
发生缩聚反应生成N,由N的结构简式可逆推出D的结构简式为 。
。
(1)C的分子式为C5H12O,C能与金属Na反应,C属于饱和一元醇,C的一氯代物有2种,C的结构简式为 。
。
(2)D的结构简式为 ,D生成N的反应类型为缩聚反应。
,D生成N的反应类型为缩聚反应。
(3)苯酚生成D的化学方程式是2![]() +
+![]() →
→ +H2O。
+H2O。
(4)B的结构简式为 ,B中的官能团为酚羟基和羧基,B的分子式为C7H6O3;F是分子量比B大14的同系物,F分子组成上比B多一个“CH2”,F的分子式为C8H8O3。F的同分异构体遇FeCl3显紫色,且能水解,F的同分异构体中含酚羟基和酯基;F的同分异构体苯环上有两个取代基且苯环上的一溴代物只有两种,苯环上的两个取代基处于对位,苯环上的两个取代基为:①—OH和—OOCCH3、②—OH和—COOCH3、③—OH和—CH2OOCH;符合条件的F的同分异构体有3种。
,B中的官能团为酚羟基和羧基,B的分子式为C7H6O3;F是分子量比B大14的同系物,F分子组成上比B多一个“CH2”,F的分子式为C8H8O3。F的同分异构体遇FeCl3显紫色,且能水解,F的同分异构体中含酚羟基和酯基;F的同分异构体苯环上有两个取代基且苯环上的一溴代物只有两种,苯环上的两个取代基处于对位,苯环上的两个取代基为:①—OH和—OOCCH3、②—OH和—COOCH3、③—OH和—CH2OOCH;符合条件的F的同分异构体有3种。
(5)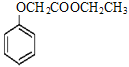 中含酯基和醚键,
中含酯基和醚键,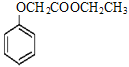 可由
可由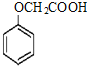 与CH3CH2OH发生酯化反应制得;
与CH3CH2OH发生酯化反应制得; 中含醚键和羧基,对比
中含醚键和羧基,对比 与苯酚、ClCH2COOH的结构简式,结合题给已知,应由
与苯酚、ClCH2COOH的结构简式,结合题给已知,应由![]() 与NaOH反应生成
与NaOH反应生成![]() ,
,![]() 与ClCH2COOH发生题给已知的反应生成
与ClCH2COOH发生题给已知的反应生成 ,合成路线流程图为
,合成路线流程图为 。
。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】工业上常利用含硫废水生产Na2S2O35H2O,实验室可用如下装置模拟生成过程。
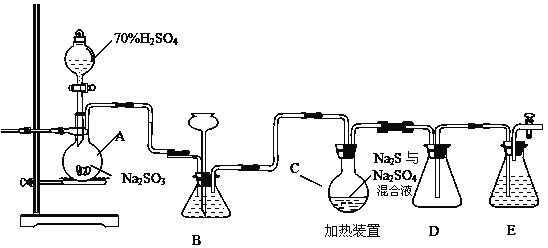
烧瓶C中发生反应如下:
Na2S(aq)+H2O(l)+SO2(g)=Na2SO3(aq)+H2S(aq) (I)
2H2S(aq)+SO2(g)=3S(s)+2H2O(l) (II)
S(s)+Na2SO3(aq)![]() Na2S2O3(aq) (III)
Na2S2O3(aq) (III)
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液注,若 __________________________,则整个装置气密性良好。装置D的作用是___________________________。装置E中为___________溶液。
(2)为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为______________。
(3)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择__________ 。
a.蒸馏水 b.饱和Na2SO3溶液
c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
(4)实验中,为使SO2缓慢进入烧瓶C,采用的操作是____________。
(5)已知反应(III)相对较慢,则烧瓶C中反应达到终点的现象是_______________。反应后期可用酒精灯适当加热烧瓶A,实验室用酒精灯加热时必须使用石棉网的仪器含有___________________。
a .烧杯 b .蒸发皿 c.试管 d .锥形瓶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一种瓦斯分析仪(下图甲)能够在煤矿巷道中的甲烷达到一定浓度时,通过传感器显示出来。该瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如下图乙所示,其中的固体电解质是Y2O3-Na2O,O2-可以在其中自由移动。下列有关叙述正确的的是( )
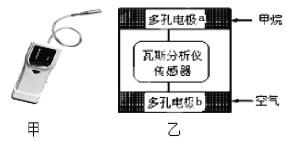
A. 瓦斯分析仪工作时,电池内电路中电子由电极b流向电极a
B. 电极a的反应式为:CH4+5O2-―8e-=CO32- +2H2O
C. 电极b是正极, O2-由电极a流向电极b
D. 当固体电解质中有1 mol O2-通过时,电子转移4 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化硼(BN)是一种重要的功能陶瓷材料以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如下图所示:
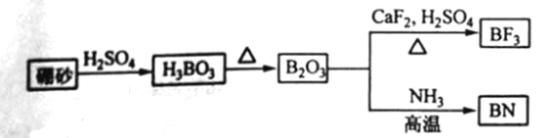
请回答下列问题:
(1) 由B2O3制备BF3、BN的化学方程式依次是_________、__________;
(2) 基态B原子的电子排布式为_________;B和N相比,电负性较大的是_________,BN中B元素的化合价为_________;
(3) 在BF3分子中,F-B-F的建角是_______,B原子的杂化轨道类型为_______,BF3和过量NaF作用可生成NaBF,BF的立体结构为_______;
(4) 在与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为________,层间作用力为________;
(5)六方氢化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,硬度与金刚石相当,晶苞边长为361.5pm,立方氮化硼晶苞中含有______各氮原子、________各硼原子,立方氮化硼的密度是_______g·![]() (只要求列算式,不必计算出数值,阿伏伽德罗常数为NA)。
(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】800℃时在2L密闭容器内反应:2NO(g)+O2(g)![]() 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)达平衡时NO的转化率_________________。
(2)下图中表示NO2的变化的曲线是________,用O2表示从0~2s内该反应的平均速率v(O2)=____________。

(3)能说明该反应一定达到平衡状态的是_____________。
a.v(NO2)=2v(O2) b.容器内颜色保持不变
c.2v逆(NO)=v正(O2) d.容器内压强保持不变
(4)能增大该反应的反应速率的是___________________。
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁、稀盐酸、澄清石灰水、氯化铜溶液是常见的物质,四种物质间的反应关系如图所示。图中两圆相交部分(A、B、C、D)表示物质间的反应,其中对应反应的离子方程式书写正确的是( )
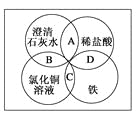
A. OH-+HCl===H2O+Cl-
B. Ca(OH)2+Cu2+===Ca2++Cu(OH)2
C. Fe+Cu2+===Cu+Fe2+
D. Fe+2H+===Fe3++H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用树状分类法对下列9种物质进行分类,然后按要求回答问题:
(1)进行分类(将各物质序号填入相应方框中),并在相应空格处作答_________。
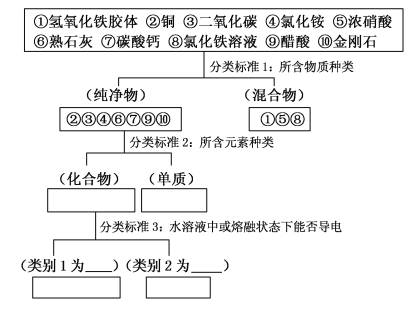
(2)氢氧化铁胶体和氯化铁溶液从外观上很难进行区分,你认为可通过什么实验来区分?__________(简要说明实验方法和判断依据)。
(3)写出上述10种物质中的强酸强碱混合,发生中和反应的化学方程式:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知非金属单质硫(S)是淡黄色固体粉末,难溶于水。为了验证氯元素的非金属性比硫元素的非金属性强(提示:Na2S +2HCl = 2NaCl+ H2S↑),某化学实验小组设计了如下实验,请回答下列问题:
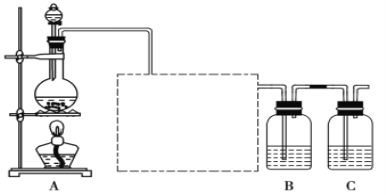
(1)画出虚线框内的实验装置图____,所加试剂为___________,该装置的作用是__________。
(2)装置B中盛放的试剂是____(填序号),
A.Na2S溶液B.Na2SO3溶液C.Na2SO4溶液
B装置中发生反应的离子方程式为___________________________。
(3)已知:①硫原子与氯原子的电子层数相同,氯的原子半径小于硫原子。②高氯酸的酸性比硫酸强;③铁与氯气在加热条件下反应生成三氯化铁,铁与硫在加热条件下反应生成硫化亚铁;④HCl比H2S稳定;⑤硫酸比次氯酸稳定;能说明氯的非金属性比硫强的是____(填序号)。
A.全部 B. ①②③④ C.①②④⑤ D. ①③④⑤
(4)装置C中盛放烧碱溶液,目的是吸收反应后剩余的气体,防止污染空气,写出该装置中所发生反应的离子方程式:_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】被誉为“矿石熊猫”的香花石,由我国地质学家首次发现,它由前20号元素中的6种组成,分别为X、Y、Z、W、R、T。其中Ⅹ、Y、Z为金属元素,Z的最外层电子数与次外层电子数相等,X、Z位于同族,Y、Z、R、T位于同周期,R最外层电子数是次外层的3倍,T无正价,X与R原子序数之和是W的2倍。下列说法错误的是
A. 原子半径:Y>Z>R>T
B. 气态氢化物的稳定性:W<R<T
C. 最高价氧化物对应的水化物的碱性:X>Z
D. XR2、WR2两种化合物中R的化合价相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com