


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
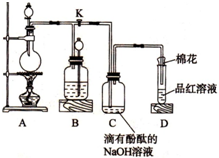 为探究铜跟浓硫酸的反应情况,用如图所示装置进行有关实验,请回答:
为探究铜跟浓硫酸的反应情况,用如图所示装置进行有关实验,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、银镜反应采用水浴加热 |
| B、取1mol?L-1的硫酸铜溶液2mL和0.4mol?L-1的氢氧化钠溶液4mL混合后加入0.5mol 40%的乙醛溶液,加热至沸腾,以验证乙醛的还原性 |
| C、在乙醛还原新制的Cu(OH)2悬浊液的实验中,制Cu(OH)2悬浊液时应加入过量的NaOH溶液,可直接加热 |
| D、配制银氨溶液时,将稀氨水逐滴加入AgNO3溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
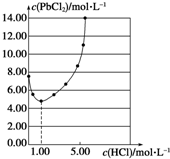 25℃时,PbCl2固体在不同浓度盐酸中的溶解度如图.在制备PbCl2的实验中,洗涤PbCl2固体最好选用( )
25℃时,PbCl2固体在不同浓度盐酸中的溶解度如图.在制备PbCl2的实验中,洗涤PbCl2固体最好选用( )| A、蒸馏水 |
| B、1.00 mol?L-1盐酸 |
| C、5.00 mol?L-1盐酸 |
| D、10.00 mol?L-1盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钢铁发生吸氧腐蚀时的正极反应:O2+4e-+4H+═2H2O |
| B、小苏打水解反应的离子方程式:HCO3-+H2O?CO32-+H3O+ |
| C、氯碱工业和工业冶炼金属钠的阳极反应均为:2Cl--2e-═Cl2↑ |
| D、NaAlO2溶液中通入足量CO2的离子方程式:2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com