

分析 正盐A可跟酸反应,又可与碱反应,生成两种气体,且两种气体能反应,由C+氨水→A,D+C的溶液→A,知D为NH3,则A为铵盐,由A可跟酸反应,又可与碱反应,A为弱酸弱碱盐,由A的溶液+浓H2SO4→B+C,知B是(NH4)2SO4,推知F为K2SO4,由A的溶液+KOH→E+D,知E为K2SO3,C为SO2,A为(NH4)2SO3,满足C(SO2)为形成酸雨的气体之一,以此解答该题.
解答 解:A可跟酸反应,又可与碱反应,生成两种气体,且两种气体能反应,由C+氨水→A,D+C的溶液→A,知D为NH3,则A为铵盐,由A可跟酸反应,又可与碱反应,A为弱酸弱碱盐,由A的溶液+浓H2SO4→B+C,知B是(NH4)2SO4,推知F为K2SO4,由A的溶液+KOH→E+D,知E为K2SO3,C为SO2,A为(NH4)2SO3,
(1)由以上分析可知A为(NH4)2SO3,B为(NH4)2SO4,C为SO2,D为NH3,E为K2SO3,F为K2SO4,
故答案为:(NH4)2SO3;(NH4)2SO4;SO2;NH3;K2SO3;K2SO4;
(2)E为K2SO3,SO32-具有还原性,与具有氧化性的Cl2发生氧化还原反应生成SO42-和Cl-,反应的化学方程式为:K2SO3+Cl2+H2O=K2SO4+2HCl,离子方程式为:SO32-+Cl2+H2O=SO42-+2Cl-+2H+,
故答案为:SO32-+Cl2+H2O=SO42-+2Cl-+2H+.
点评 本题考查了无机物的推断,为高频考点,侧重于学生的分析能力的考查,解答无机框图题,须找到解题突破口,本题注意A可跟酸反应,又可与碱反应,为解答该题的关键,题目难度中等.


科目:高中化学 来源: 题型:解答题
 四种短周期元素在周期表中的相对位置如下所示,其中Y元素原子最外层电子数是其电子层数的3倍.
四种短周期元素在周期表中的相对位置如下所示,其中Y元素原子最外层电子数是其电子层数的3倍.| X | Y | |
| Z | W |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 重铬酸钾(K2Cr2O7)是一种重要的氧化剂,可以检验司机是否酒后驾驶.
重铬酸钾(K2Cr2O7)是一种重要的氧化剂,可以检验司机是否酒后驾驶.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定含有甲烷 | B. | 一定含有乙烯 | ||
| C. | 可能是乙烷和甲烷的混合气体 | D. | 一定含有乙烯,不一定含有甲烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在c(H+)=1.0×10-13 mol•L-1的溶液中:Na+、S2-、AlO2-、SO32- | |
| B. | pH<7的溶液中:SO42-、CO32-、Na+、K+ | |
| C. | 有NO3-存在的强酸性溶液中:NH4+、Ba2+、Fe2+、Br- | |
| D. | 在pH=1的溶液中:NH4+、K+、ClO-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
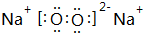 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 价格便宜,不易生锈 | |
| B. | 铁锅只含有铁元素 | |
| C. | 烹调的食物中留有人体需要的铁元素 | |
| D. | 传热慢,保温性能好 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com