
将AgCl分别加入盛有:①5 mL水;②6 mL 0.5 mol·L-1 NaCl溶液;③10 mL 0.2 mol·L-1 CaCl2溶液;④50 mL 0.1 mol·L-1盐酸的烧杯中,均有固体剩余,各溶液中c(Ag+)从大到小的顺序排列正确的是 ( )。
A.④③②① B.②③④① C.①④③② D .①③②④
.①③②④
科目:高中化学 来源: 题型:
为增强铝的耐腐蚀性,现以铅蓄电池为外电源,以Al作阳极、Pb作阴极,电解稀硫酸,使铝表面的氧化膜增厚。反应原理如下:
电池:Pb(s)+PbO2(s)+2H2SO4(aq)= ==2PbSO4(s)+2H2O(l)
==2PbSO4(s)+2H2O(l)
电解池:2Al+3H2O电解,Al2O3+3H2↑
电解过程中,以下判断正确的是 ( )
| 电池 | 电解池 | |
| A | H+移向Pb电极 | H+移向Pb电极 |
| B | 每消耗3 mol Pb | 生成2 mol Al2O3 |
| C | 正极:PbO2+4H++2e-===Pb2++2H2O | 阳极:2Al+3H2O-6e-===Al2O3+6H+ |
| D |
|
|
查看答案和解析>>
科目:高中化学 来源: 题型:
用下图所示实验装置制取乙酸乙酯。回答以下问题:(共12分)
(1)在大试管中配制一定比例的乙醇、乙酸和浓硫酸的混合液的方法是:将 ,然后轻轻振荡试管,使之混合均匀。(2分)
(2)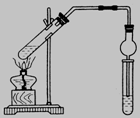 加入浓硫酸的目的是: 。(2分)
加入浓硫酸的目的是: 。(2分)
(3)饱和碳酸钠溶液的作用是: (2分)
(4)若实验中反应温度不当,使反应温度维持在140℃左
右,此时副反应的主要有机产物是 。(2分)
(5)与书中采用的实验装置的不同之处是:本实验采用了球形干燥管代替了长导管,并将干燥管的末端插入了饱和碳酸钠溶液中。在此处球形干燥管的作用有:
① ,② 。(4分)
查看答案和解析>>
科目:高中化学 来源: 题型:
已知HCO3―+AlO2― +H2O=CO32― +Al(OH)3↓;将足量的KHCO3溶液不断滴入含等物质的量的KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀的物质的量与滴入的KHCO3溶液体积的关系可表示为

查看答案和解析>>
科目:高中化学 来源: 题型:
为研究铁质材料与热浓硫酸的反应,某学习小组用碳素钢(即铁和碳的合金)进行了以下探究活动:
[探究一](1)将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是 。
(2)称取碳素钢6.0 g放入15.0 mL浓硫酸中,加热,充分反应后得到溶液X并收集到混合气体Y。
①甲同学认为X中除Fe3+之外还可能含有Fe2+。若要确认其中的Fe2+,应选用 (选填序号)。
A.KSCN溶液和氯水 B.铁粉和KSCN溶液
C.浓氨水 D.酸性KMnO4溶液
②乙同学取560 mL(标准状况)气体Y通入足量溴水中,然后加入足量BaCl2溶液,经适当操作后得干燥固体4.66 g。由此推知气体Y中SO2的体积分数为 。
[探究二]根据上述实验中SO2体积分数的分析,丙同学认为气 体Y中还可能含有Q1和Q2两种气体,其中Q1气体,在标准状况下,密度为0.0893 g·L-1。为此设计了下列探究实验装置(假设有关气体完全反应)。
体Y中还可能含有Q1和Q2两种气体,其中Q1气体,在标准状况下,密度为0.0893 g·L-1。为此设计了下列探究实验装置(假设有关气体完全反应)。

(3)装置B中试剂的作用是 。
(4)分析Y气体中的Q2气体是如何生成的 (用化学方程式表示)。
(5)已知洗气瓶M中盛装澄清石灰水,为确认Q2的存在,需在装置中添加洗气瓶M于
(填序号)。
A.A之前 B.A—B间
C.B—C间 D.C—D间
(6)如果气体Y中含有Q1,预计实验现象应是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
据报道,有一种叫Thibacillus Ferroxidans的细菌在氧气存在下的酸性溶液中,能将黄铜矿(CuFeS2)氧化成硫酸盐,发生的反应为:
4CuFeS2+2H2SO4+17O2===4CuSO4+2Fe2(SO4)3+2H2O
(1)CuFeS2中Fe的化合价为+2,上述反应中被氧化的元素是________。
(2)工业生产中利用上述反应后的溶液,按如下流程可制备胆矾(CuSO4·5H2O):
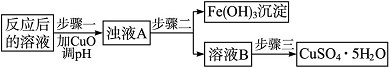
①分析下列表格(其中Ksp是相应金属氢氧化物的沉淀溶解平衡常数):
| Ksp | 氢氧化物开始 沉淀时的pH | 氢氧化物沉淀 完全时的pH | |
| Fe3+ | 2.6×10-39 | 1.9 | 3.2 |
| Cu2+ | 2.2×10-20 | 4.7 | 6.7 |
步骤一应调节溶液的pH范围是__________,请运用沉淀溶解平衡的有关理论解释加入CuO能除去CuSO4溶液中Fe3+的原因________________________________________________
________________________________________________________________________。
②步骤三中的具体操作方法是_________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在下列给定条件的溶液中,一定能大量共存的离子组是 ( )。
A.无色溶液:Ca2+、H+、Cl-、HSO3-
B.能使pH试纸呈红色的溶液:Na+、NH4+、I-、NO3-
C.FeCl2溶液:K +、Na+、SO42-、AlO2-
+、Na+、SO42-、AlO2-
D.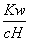 =0.1 mol·L-1的溶液:Na+、K+、SiO32-、NO3-
=0.1 mol·L-1的溶液:Na+、K+、SiO32-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物的结构简式如右图,
则此有机物可发生的反应类型有:
①取代 ②加成 ③消去 ④酯化 ⑤水解⑥氧化 ⑦中和( )
A.①②③⑤⑥ B.②③④⑤⑥ C.①②③④⑤⑥ D.①②③④⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组性质的比较中正确的是( )
A.酸性 HClO4<HBrO4<HIO4 B.碱性 Ba(OH)2>Ca(OH)2>Mg(OH)2
C.稳定性 HCl>PH3>H2S D.还原性 Cl->Br->I-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com