
【题目】下图为从海带中提碘生产的实验室模拟流程。试回答下列问题:
(1)实验操作中所用玻璃仪器为酒精灯、烧杯、普通漏斗、牛角管、锥形瓶、蒸馏烧瓶等。若要完成操作1,还缺少的玻璃仪器有 ,该仪器的作用为 ;操作2的名称为 ;若要完成操作3,还缺少的玻璃仪器有 。
(2)实验室用二氧化锰制氯气的化学方程式为 。
(3)弃液B中滴入淀粉液,溶液呈蓝色,但通入二氧化硫后蓝色褪去,写出该过程中发生反应的化学方程式并用双线桥标明电子转移的方向和数目 。
【答案】(1)玻璃棒 引流;萃取(分液);温度计、冷凝管(8分)
(2)MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O (2分)
MnCl2+Cl2↑+2H2O (2分)
(3)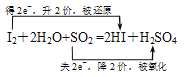 (2分)
(2分)
【解析】
试题分析:(1)由流程可知,将海带烧成灰,向灰中加水搅拌,操作1为分离固体和液体,即为过滤操作,过滤操作用到的玻璃仪器有:烧杯、玻璃棒、漏斗,完成操作1,还缺少的玻璃仪器有玻璃棒,其作用为引流;溶液A中含碘离子,加氯水发生氧化还原反应生成碘,操作2为萃取,溶液B为含碘的有机溶液,则操作3为蒸馏得到碘单质,蒸馏操作用到的仪器有,酒精灯、蒸馏烧瓶、冷凝管、牛角管、锥形瓶、温度计, 完成操作3,还缺少的玻璃仪器有温度计、冷凝管。
(2)实验室用二氧化锰和浓盐酸反应制氯气,反应的化学方程式为MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。
(3)在弃液中滴入淀粉溶液,溶液呈蓝色,说明在弃液中含有碘,该溶液中通入二氧化硫,发现蓝色褪去,发生的反应为 。
。


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
【题目】将足量CO2通入NaOH和Ba(OH)2的混合稀溶液中,生成沉淀的物质的量(n)和通入CO2体积(V)的关系如图,图中AB段表示的先后离子方程式是
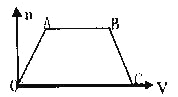
CO2+OH-=HCO3-
CO2+2OH-=CO32-+H2O
CO32-+Ba2+=BaCO3↓
④BaCO3+CO2+H2O=Ba2++2HCO3-
⑤CO32-+CO2+H2O=2HCO3-
A.②⑤ B.⑤④ C.④② D.④①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用氯化铁溶液作为“腐蚀液”腐蚀铜印刷电路板后,所得溶液中Cu2+和Fe3+的物质的量浓度恰好相等。则已反应的Fe3+和反应前Fe3+物质的量之比为
A. 1∶2 B. 1∶3 C. 2∶3 D. 3∶5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,能说明SO2是酸性氧化物的是
A. SO2+H2O2 ==H2SO4 B. SO2+Ca(OH)2==CaSO3+H2O
C. SO2+Cl2+2H2O==H2SO4+2HCl D. SO2+2H2S==3S↓+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中Cl﹣浓度最大的是
A.200mL 2mol/L MgCl2溶液
B.1000mL 2.5mol/L NaCl溶液
C.10g AgCl固体加入 300mL水充分搅拌
D.250mL 1mol/L AlCl3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸生产中存在炉气转化反应:2SO2(g)+O2(g)![]() 2SO3(g)。研究发现,SO3的体积分数随温度(T)的变化如曲线I所示。下列判断正确的是
2SO3(g)。研究发现,SO3的体积分数随温度(T)的变化如曲线I所示。下列判断正确的是

A.该反应的正反应为吸热反应
B.反应达到B点时,2υ正(O2)=υ逆(SO3)
C.曲线I上A、C两点反应速率的关系:υA>υC
D.已知V2O5的催化效果比Fe2O3好,若I表示用V2O5作催化剂时的曲线,则II是Fe2O3作催化剂时的曲线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.火箭升空需要高能的燃料,通常用肼(N2H4)作为燃料,N2O4做氧化剂。
(1)已知:N2(g)+2O2(g)=2NO2(g) △H=+67.7kJ·mol-1
N2H4(g)+O2(g)=N2(g)+2H2O(g) △H=-534.0kJ·mol-1
2NO2(g)![]() N2O4(g) △H=-52.7kJ·mol-1
N2O4(g) △H=-52.7kJ·mol-1
试写出气态肼在气态四氧化二氮中燃烧生成氮气和气态水的热化学方程式:__________________。
(2)工业上可用次氯酸钠与过量的氨反应制备肼,该反应的化学方程式为: 。
Ⅱ、(1)一定条件下,在2L密闭容器中起始投入2 mol NH3和4 mol O2发生反应:4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) ΔH<0
4NO(g)+6H2O(g) ΔH<0
测得平衡时数据如下:
平衡时物质的量(mol) | n(NO) | n(H2O) |
温度T1 | 1.6 | 2.4 |
温度T2 | 1.2 | 1.8 |
在温度T1下,若经过10min反应达到平衡,则10min内反应的平均速率v(NH3)= 。
②温度T1和T2的大小关系是T1 T2(填“>”、 “<”或“=”)。
(2)电解KOH溶液,如果某段时间内氢氧储罐中共收集到33.6L气体已折算成标况),则该段时间内水电解系统中转移电子的物质的量为__________mol。
(3)在载人航天器的生态系统中,不仅要求分离去除CO2,还要求提供充足的O2。某种电化学装置可实现如下转化:2CO2=2CO+O2,CO可用作燃料。已知该反应的阳极反应为:![]() =O2↑+2H2O,则阴极反应为 。有人提出,可以设计反应2CO=2C+O2(△H>0)来消除CO的污染。请你判断上述反应是否能自发进行并说明理由 。
=O2↑+2H2O,则阴极反应为 。有人提出,可以设计反应2CO=2C+O2(△H>0)来消除CO的污染。请你判断上述反应是否能自发进行并说明理由 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中化学键的类型相同的是( )
A.HCl MgCl2 NH4Cl
B.H2O Na2O CO2
C.CaCl2 NaOH H2S
D.NH3 H2O CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备硝基苯的方法是将苯与浓硫酸和浓硝酸的混合液加热到 50~60℃反应。已知苯与硝基苯的基本物理性质如下表所示:


(1)要配制浓硫酸和浓硝酸的混合酸的注意事项是_________________。
(2)分离硝基苯和水的混合物的方法是_____________;分离硝基苯和苯的方法是_____________。
(3)某同学用如图装置制取硝基苯:
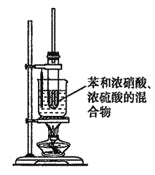
①用水浴加热的优点是_________________;
②被水浴加热的试管口部都要带一长导管,其作用是_________________。
(4)写出此反应的化学方程式____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com