
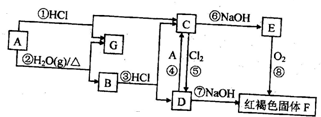
分析 A、B、C、D、E、F均含有同一种元素,单质A与盐酸反应生成C与G,C与氢氧化钠反应生成E,E与氧气反应生成红褐色沉淀F,则A为Fe,G为 H2,C为FeCl2,E为Fe(OH)2,结合转化关系可知F为Fe(OH)3,B为Fe3O4,D为FeCl3.
解答 解:A、B、C、D、E、F均含有同一种元素,单质A与盐酸反应生成C与G,C与氢氧化钠反应生成E,E与氧气反应生成红褐色沉淀F,则A为Fe,G为 H2,C为FeCl2,E为Fe(OH)2,结合转化关系可知F为Fe(OH)3,B为Fe3O4,D为FeCl3.
(1)由上述分析可知,G为 H2,D为FeCl3,
故答案为:H2;FeCl3;
(2)在①-⑧的化学反应中,不属于氧化还原反应的有:③⑥⑦,
故答案为:③⑥⑦;
(3)E转化为F的过程中的变化现象:白色沉淀迅速变为灰绿色,最终变为红褐色,
故答案为:白色沉淀迅速变为灰绿色,最终变为红褐色;
(4)反应⑤的离子方程式:2Fe2++Cl2=2Fe3++2Cl-,
故答案为:2Fe2++Cl2=2Fe3++2Cl-;
(5)反应③的化学方程式:Fe3O4+8HCl=FeCl2+2FeCl3+4H2O,
故答案为:Fe3O4+8HCl=FeCl2+2FeCl3+4H2O;
(6)刻制印刷电路时,要用D溶液作为“腐蚀液”来“腐蚀”铜箔制成线路板.相关的化学方程式:2FeCl3+Cu=2FeCl2+CuCl2,
故答案为:2FeCl3+Cu=2FeCl2+CuCl2.
点评 本题考查无机物的推断,涉及Fe元素单质化合物性质与转化,F为红褐色固体为推断突破口,再结构转化关系推断,熟练掌握元素化合物性质,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
 为探究乙炔与溴的加成反应,甲同学设计并进行了如下实验:先取一定量工业用电石与水反应,将生成的气体通入溴水中,发现溶液褪色,即证明乙炔与溴水发生了加成反应.乙同学发现在甲同学的实验中,褪色后的溶液里有少许淡黄色浑浊,推测在制得的乙炔中还可能含有少量还原性的杂质气体,由此他提出必须先除去,再与溴水反应.请你回答下列问题:
为探究乙炔与溴的加成反应,甲同学设计并进行了如下实验:先取一定量工业用电石与水反应,将生成的气体通入溴水中,发现溶液褪色,即证明乙炔与溴水发生了加成反应.乙同学发现在甲同学的实验中,褪色后的溶液里有少许淡黄色浑浊,推测在制得的乙炔中还可能含有少量还原性的杂质气体,由此他提出必须先除去,再与溴水反应.请你回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
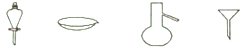
| A. | 蒸馏、蒸发、萃取、过滤 | B. | 蒸馏、过滤、萃取、蒸发 | ||
| C. | 过滤、蒸发、萃取、蒸馏 | D. | 萃取、蒸发、蒸馏、过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中国化学家侯德榜研究了“侯氏联合制碱法”,为我国化工发展做出贡献 | |
| B. | 瑞典化学家舍勒发现软锰矿(含MnO2)与浓盐酸混合加热制得氯气 | |
| C. | 意大利物理甲阿伏伽德罗发现当光束通过胶体时可见一条光路 | |
| D. | 德国化学家哈伯在合成氨的研究中做出了巨大贡献 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②③⑤ | C. | ③④⑤ | D. | ①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
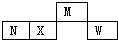 短周期主族元素M、N、X、W在元素周期表中的相对位置如图所示,N元素的单质常用作半导体材料.下列判断正确的是( )
短周期主族元素M、N、X、W在元素周期表中的相对位置如图所示,N元素的单质常用作半导体材料.下列判断正确的是( )| A. | 原子半径的大小:W>X>M | |
| B. | 气态氢化物的稳定性:N>X>M | |
| C. | 对应的含氧酸的酸性强弱:W>X>N | |
| D. | W分别与N、X形成的化合物中的化学键均为极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A.烟花的颜色 | B.贴春联 | C.鞭炮的燃放 | D.包饺子 |
 |  |  |  |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 某无色溶液中阴离子为Cl-,阳离子可能含有下列离子中的一种或几种:H+、K+、Al3+、NH4+、Fe3+,向该溶液中逐滴加入NaOH溶液,产生沉淀的物质的量(n)与加入NaOH 溶液的体积(V)的关系如图所示.
某无色溶液中阴离子为Cl-,阳离子可能含有下列离子中的一种或几种:H+、K+、Al3+、NH4+、Fe3+,向该溶液中逐滴加入NaOH溶液,产生沉淀的物质的量(n)与加入NaOH 溶液的体积(V)的关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com