
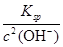 =
=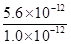 =5.6×10-10(mol·L-1)。
=5.6×10-10(mol·L-1)。

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:问答题
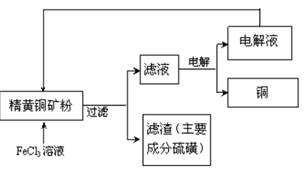
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
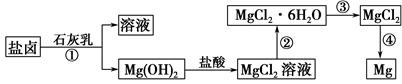
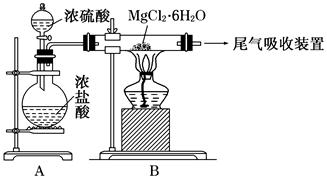
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.125 mL | B.200 mL | C.250 mL | D.560 mL |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

| A.粉碎固体混合物 | B.降低温度 | C.不断搅拌 | D.缩短浸泡时间 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氨水中沉淀一定比NaOH溶液中的多 |
| B.氨水中沉淀一定比NaOH溶液中的少 |
| C.氨水中沉淀可能比NaOH溶液中的多 |
| D.氨水中和NaOH溶液中的沉淀不可能一样多 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
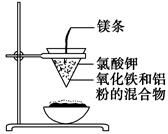
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氯化铝溶液中加入过量氨水反应实质是: Al3++3NH3·H2O=Al(OH)3↓+3NH4+ |
| B.在加入铝粉能放出氢气的溶液中:K+、NH4+、CO32—、Cl-一定能够大量共存 |
| C.镁铝合金既可完全溶于过量盐酸又可完全溶于过量NaOH溶液 |
D.依据铝热反应原理,能发生反应:2Al+3MgO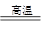 3Mg+Al2O3 3Mg+Al2O3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
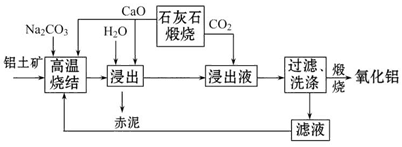
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com