
(1)如下图所示,组成一种原电池.试回答下列问题(灯泡功率合适):
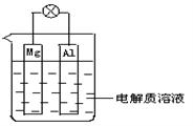
①电解质溶液为稀H2SO4时上述装置中灯泡亮,此时Al电极上发生反应的电极反应式为: ___ ;
②电解质溶液为NaOH溶液时,灯泡______(填“亮”或“不亮”, 填“亮”做a题,填“不亮”做b题)。
a.若灯泡亮,则Mg电极上发生的电极反应式为:_______________ ;
Al电极上发生反应的电极反应式为:_______________ ;
b.若灯泡不亮,其理由为:________________________ 。
(2)原电池原理的应用之一是可以设计原电池。请利用反应“Cu+2Fe3+ =2Fe2+ +Cu2+ ”设制一个原电池(正极材料用碳棒)则该电池的负极材料是__________,若导线上转移电子1.5 mol,则溶解铜的质量是__________。另外的重要应用是实验室在用锌与稀硫酸反应制备氢气时,可向溶液中滴加少量硫酸铜溶液。其作用是: ______________________________。
(3)氢氧燃料电池(电解质为KOH溶液,惰性材料作电极)负极反应的电极反应式为:______________________________。
(1)①2H+ + 2e- = H2↑;
②亮 a. 6H2O + 6e- = 6OH- + 3H2↑;2Al – 6e- + 8OH- =2AlO2- + 4H2O。
(2)Cu;48g;形成了Zn—Cu原电池,加快了化学反应的速率(注:必须强调形成Zn—Cu原电池,否则不得分);(3)H2 +2 OH- - 2e-=2H2O
【解析】
试题分析:(1)①分析题给装置图,当电解质溶液为稀H2SO4时上述装置中灯泡亮,则形成原电池,镁较活泼,作原电池的负极,Al片作原电池的正极,电极反应式:2H+ + 2e- = H2↑;②电解质溶液为NaOH溶液时,Al片作负极,Mg片作正极,灯光亮,Mg电极上发生的电极反应式为a. 6H2O + 6e- = 6OH- + 3H2↑;Al电极上发生反应的电极反应式为:2Al – 6e- + 8OH- =2AlO2- + 4H2O;(2)结合Cu+2Fe3+ =2Fe2+ +Cu2+知,铜片发生氧化反应,负极材料是Cu片,电极反应式为Cu-2e- =Cu2+ ,若导线上转移电子1.5 mol,则溶解铜的质量是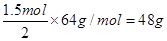 ,实验室在用锌与稀硫酸反应制备氢气时,可向溶液中滴加少量硫酸铜溶液的作用是形成了Zn—Cu原电池,加快了化学反应的速率;(3)氢氧燃料电池(电解质为KOH溶液,惰性材料作电极)负极反应的电极反应式为H2 +2 OH- - 2e-=2H2O。
,实验室在用锌与稀硫酸反应制备氢气时,可向溶液中滴加少量硫酸铜溶液的作用是形成了Zn—Cu原电池,加快了化学反应的速率;(3)氢氧燃料电池(电解质为KOH溶液,惰性材料作电极)负极反应的电极反应式为H2 +2 OH- - 2e-=2H2O。
考点:考查原电池原理、燃料电池。


 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源:2013-2014吉林省白城市高一上学期期末考试化学(A卷)试卷(解析版) 题型:选择题
某溶液中大量存在以下五种离子:NO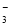 、SO42-、Fe3+、H+、M,其物质的量之比为
、SO42-、Fe3+、H+、M,其物质的量之比为
n(NO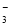 )∶n(SO42-)∶n(Fe3+)∶n(H+)∶n(M)=2∶3∶1∶3∶1,则 M可能为( )
)∶n(SO42-)∶n(Fe3+)∶n(H+)∶n(M)=2∶3∶1∶3∶1,则 M可能为( )
A.Cl- B.Mg2+ C.Ba2+ D.Na+
查看答案和解析>>
科目:高中化学 来源:2013-2014吉林省高二下学期期末考试化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.强电解质溶液一定比弱电解质溶液的导电性强
B.强电解质的水溶液中不存在电解质分子
C.强电解质都是离子化合物,弱电解质都是共价化合物
D.不同的弱电解质只要物质的量浓度相同,电离程度也就相同
查看答案和解析>>
科目:高中化学 来源:2013-2014吉林省高二5月月考化学试卷(解析版) 题型:选择题
在一条鱼虾绝迹的小河边,从上游到下游依次有四座工厂:甲、乙、丙、丁.它们排出的废液里,每厂只含有Na2CO3、FeCl3、Ca(OH)2、HCl中的一种.某中学环保小组对河水监测时发现:(1)甲处河水呈乳白色;(2)乙处河水呈褐色;(3)丙处河水由浑变清;(4)丁处河水产生气泡,河水仍清.下列四厂排出废液里所含污染物推断正确的为( )
A.甲含HCl B.乙含FeCl3 C.丙含Na2C03 D.丁含Ca(OH)2
查看答案和解析>>
科目:高中化学 来源:2013-2014吉林省高二5月月考化学试卷(解析版) 题型:选择题
随着社会的发展,人们日益重视环境问题,下列做法或说法不正确的是( )
A.绿色化学的核心是利用化学原理从头上减少和消除工农业生产等对环境的污染
B.将工业废水“再生”处理,用于城市道路保洁、喷泉和浇花用水
C.大力实施矿物燃料“脱硫、脱硝技术”,减少硫和氮的氧化物对环境的污染
D.PM2.5是指大气中直径接近于2.5×10-6m的颗粒物,也称细颗粒物,这些细颗粒物
分散在空气中形成混合物具有丁达尔效应
查看答案和解析>>
科目:高中化学 来源:2013-2014吉林省高一下学期期末考试化学试卷(解析版) 题型:填空题
下列各个曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质)。把与下面元素有关的性质相符的曲线标号填入相应的空格中:
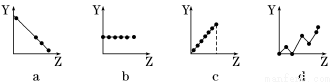
(1)ⅡA族元素的最外层电子数________;
(2)第3周期元素的最高化合价________;
(3)F-、Na+、Mg2+、Al3+的离子半径________。
查看答案和解析>>
科目:高中化学 来源:2013-2014吉林省高一下学期期末考试化学试卷(解析版) 题型:选择题
手性分子是指在分子结构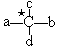 中,当a、b、c、d为彼此互不相同的原子或原子团时,称此分子为手性分子,中心碳原子为手性碳原子。下列分子中指定的碳原子(用★标记)属于手性碳原子的是
中,当a、b、c、d为彼此互不相同的原子或原子团时,称此分子为手性分子,中心碳原子为手性碳原子。下列分子中指定的碳原子(用★标记)属于手性碳原子的是
A.降冰片烯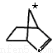 B.乳酸
B.乳酸
C.苯甲醇 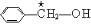 D.甘油
D.甘油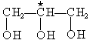
查看答案和解析>>
科目:高中化学 来源:2013-2014吉林省高一5月月考化学试卷(解析版) 题型:填空题
指出下列中反应的反应类型。
(1)CH2===CH2+Br2―→CH2BrCH2Br,反应类型:__________。
(2)CH3CH3+2Cl2 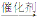 CH2ClCH2Cl+2HCl反应类型:________。
CH2ClCH2Cl+2HCl反应类型:________。
(3)C2H4+3O2 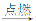 2CO2+2H2O,反应类型:___________。
2CO2+2H2O,反应类型:___________。
查看答案和解析>>
科目:高中化学 来源:2013-2014吉林省下学期期中考试高一化学试卷(解析版) 题型:计算题
(1)下列四种粒子中,半径按由大到小的排列顺序是 。
①基态X的原子结构示意图:○+16
②基态Y的价电子排布式:3s23p5
③基态Z2-的电子排布图:
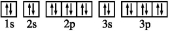
④W基态原子有2个能层,电子式:∶∶
(2)已知An+、B(n+1)+、Cn-、D(n+1)-都具有相同的电子层结构,则A、B、C、D的原子半径由大到小的顺序是 ,离子半径由大到小的顺序是 ,原子序数由大到小的顺序是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com