
分析 金属单质的熔点取决于金属键的强弱,而金属强弱取决于金属阳离子半径大小,原子半径越小金属键越强,熔点越高;
钢铁中含有杂质碳,能够形成原电池而发生电化学腐蚀,加快金属铁的腐蚀速率;
分子晶体熔沸点较低,受热容易发生升华.
解答 解:铁与钙同周期,铁排在钙的后面,原子半径小于钙,金属键强于钙,所以熔点高于钙;
钢铁中含有杂质碳,能够形成原电池而发生电化学腐蚀,加快金属铁的腐蚀速率,而纯铁中不含杂质,不容易发生电化学腐蚀;
化铁受热会发生升华现象说明氯化铁沸点低,为分子晶体,氯化铁存在分子为铁原子与氯原子通过共价键形成的共价化合物;
故答案为:强;不会发生电化学腐蚀;共价.
点评 本题考查了不同类型晶体的熔沸点规律、金属腐蚀的原理,明确决定不同类型晶体熔沸点作用力,熟悉原电池形成条件是解题关键,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 膳食纤维具有突出的保健功能,是人体的“第七营养素”.木质素是一种非糖类膳食纤维.其单体之一是芥子醇,结构简式如图所示.下列有关芥子醇的说法正确的是( )
膳食纤维具有突出的保健功能,是人体的“第七营养素”.木质素是一种非糖类膳食纤维.其单体之一是芥子醇,结构简式如图所示.下列有关芥子醇的说法正确的是( )| A. | 芥子醇的分子式是C11H14O4,属于芳香烃 | |
| B. | 芥子醇分子中所有碳原子不可能在同一平面上 | |
| C. | 芥子醇不能使酸性KMnO4溶液褪色 | |
| D. | 芥子醇可以发生氧化反应、取代反应、加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
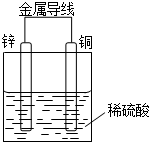 某同学设计出如下原电池原理和实验装置来证明Cu和Zn的金属活动性顺序.请你完成下列实验报告
某同学设计出如下原电池原理和实验装置来证明Cu和Zn的金属活动性顺序.请你完成下列实验报告查看答案和解析>>
科目:高中化学 来源: 题型:解答题
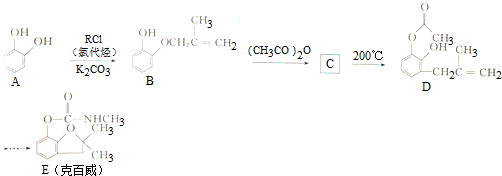
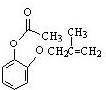 .
.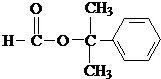 .
.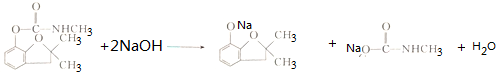 .
. 的两步化学方程式
的两步化学方程式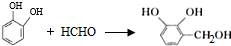 、
、 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
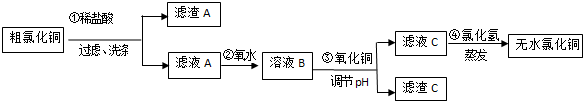
| 离子符号 | Fe3+ | Fe2+ | Cu2+ |
| 氢氧化物开始沉淀时的pH | 2.5 | 7.0 | 4.7 |
| 氢氧化物完全沉淀时的pH | 3.2 | 9.7 | 6.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在K2SO4与BaCl2两溶液反应时,增大压强 | |
| B. | Fe与稀硫酸反应制取H2时,改用浓硫酸 | |
| C. | Al在氧气中燃烧生成A12O3,将Al片改成Al粉 | |
| D. | Na与水反应时增大水的用量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径比较:X<Y<Z<W | |
| B. | X的氢化物沸点一定低于Y的氢化物 | |
| C. | Y的氢化物稳定性一定弱于W的氢化物 | |
| D. | 短周期所有元素中,Z的最高价氧化物的水化物碱性最强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 短周期元素形成离子后,最外层电子达到都达到8电子稳定结构 | |
| B. | 所有主族元素的正化合价数等于它的族序数 | |
| C. | 第3、4、5、6周期元素的数目分别是8、18、32、32 | |
| D. | 第4周期由左至右第8、9、10三列中没有非金属元素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com